punto de incendio de un combustible es la temperatura más baja a la que el vapor de ese combustible continuará quemándose durante al menos 5 segundos después de la ignición por una llama abierta. En el punto de inflamación , a una temperatura más baja, una sustancia se encenderá brevemente, pero el vapor podría no producirse a una velocidad para sostener el fuego. La mayoría de las tablas de propiedades de material solo enumerarán los puntos de inflamación del material. Aunque en general se puede suponer que los puntos de incendio son aproximadamente 10 ° C más altos que los puntos de inflamación [1], esto no sustituye las pruebas si el punto de incendio es crítico para la seguridad. [1]
la primera ley de la termodinámica es una expresión de la conservación de la energía total de un sistema. El aumento de la energía de un sistema es igual a la suma del trabajo realizado en el sistema y el calor agregado a ese sistema:
dónde
- Es la energía total de un sistema.
- es el trabajo realizado en él.
- Es el calor agregado a ese sistema.
dónde
- Es el tensor de estrés de Cauchy .
- Es la velocidad del flujo .
- y Es el vector de flujo de calor .
Debido a que expresa la conservación de la energía total, esto a veces se conoce como la ecuación de balance de energía de los medios continuos. La primera ley se usa para derivar la forma de no conservación de las ecuaciones de Navier-Stokes .
Nota [ editar ]
Dónde
- es la presion
- es la matriz de identidad
- es el tensor de estrés desviador
Es decir, tirar es un estrés positivo y empujar es un estrés negativo.
Líquido compresible [ editar ]
Para un fluido compresible, el lado izquierdo de la ecuación se convierte en:
porque en general
Forma integral [ editar ]
Es decir, el cambio en la energía interna de la sustancia dentro de un volumen es el negativo de la cantidad extraída del volumen por el flujo de material a través del límite más el trabajo realizado al comprimir el material en el límite menos el flujo de calor hacia afuera. a través del límite. Más en general, es posible incorporar términos fuente. [2]
Representación alternativa [ editar ]
dónde es entalpia específica, Es función de disipación y es la temperatura Y donde
es decir, la energía interna por unidad de volumen es igual a la densidad de masa multiplicada por la suma de: energía adecuada por unidad de masa, energía cinética por unidad de masa y energía potencial gravitatoria por unidad de masa.
es decir, el cambio en el calor por unidad de volumen (divergencia negativa del flujo de calor) es igual a la divergencia de la conductividad del calor por el gradiente de la temperatura.
es decir, la divergencia del trabajo realizado contra el estrés es igual al flujo de los tiempos del material divergencia del esfuerzo más la tensión del flujo del material.
es decir, la divergencia de los tiempos de tensión del flujo de material es igual a la divergencia de los tiempos del tensor de tensión desviada del flujo de material menos la presión de los flujos de material.
es decir, la entalpía por unidad de masa es igual a la energía adecuada por unidad de masa más la presión por volumen de unidad por unidad de masa (recíproco de densidad de masa).
Datos de forma alternativa [ editar ]
- lado izquierdo de las ecuaciones de Navier-Stokes menos la fuerza del cuerpo (por unidad de volumen) que actúa sobre el fluido.
- esta relación se deriva utilizando esta relación que es una forma alternativa de ecuación de continuidad
Un flashover es el encendido casi simultáneo de la mayoría del material combustible expuesto directamente en un área cerrada. Cuando ciertos materiales orgánicos se calientan, sufren una descomposición térmica y liberan gases inflamables. El destello ocurre cuando la mayoría de las superficies expuestas en un espacio se calientan a su temperatura de autoignición y emiten gases inflamables (vea también el punto de inflamación ). Normalmente, la descarga repentina ocurre a 500 ° C (932 ° F) o 590 ° C (1,100 ° F) para combustibles ordinarios, y un flujo de calor incidente a nivel del suelo de 20 kilovatios por metro cuadrado (2.5 hp / pies cuadrados).
Un ejemplo de flashover es el encendido de un mueble en una habitación doméstica. El fuego que involucra el mueble inicial puede producir una capa de humo caliente que se extiende por el techo de la habitación. La capa de humo flotante caliente crece en profundidad, ya que está delimitada por las paredes de la habitación. El calor irradiado de esta capa calienta las superficies de los materiales combustibles directamente expuestos en la habitación, lo que hace que emitan gases inflamables a través de la pirólisis . Cuando las temperaturas de los gases evolucionados se vuelven lo suficientemente altas, estos gases se encenderán en toda su extensión.
Tipos [ editar ]
La terminología original sueca relacionada con el término 'flashover' ha sido modificada en su traducción para cumplir con las definiciones [científicas] actuales aceptadas en Europa y Norteamérica como sigue:
- Un flashover magro (a veces llamado reinversión ) es el encendido de la capa de gas debajo del techo, lo que lleva a la participación total del compartimiento. La relación combustible / aire se encuentra en la región inferior del rango de inflamabilidad ( es decir, magra).
- Un flashover rico ocurre cuando los gases inflamables se encienden en la región superior del rango de inflamabilidad ( es decir, rico). Esto puede suceder en habitaciones donde el fuego disminuyó debido a la falta de oxígeno. La fuente de ignición puede ser un objeto ardiente o la agitación de las brasas por la vía aérea. Tal evento es conocido como ' backdraft ' .
- Un flashover demorado ocurre cuando la nube de humo gris más fría se enciende después de congregarse fuera de su sala de origen. Esto resulta en una situación volátil, y si la ignición ocurre en la mezcla ideal, el resultado puede ser una explosión violenta de humo . Esto se conoce como explosión de humo o ignición de gas de incendio dependiendo de la severidad del proceso de combustión.
- Un flashover rico en caliente ocurre cuando el humo caliente con una relación de gas inflamable por encima del límite superior del rango de inflamabilidad y la temperatura más alta que la temperatura de ignición sale del compartimiento. Al diluirse con aire, puede encenderse espontáneamente, y la llama resultante puede propagarse nuevamente dentro del compartimiento, lo que resulta en un evento similar a un rico destello. La definición común de este proceso se conoce como autoignición, que es otra forma de ignición por gas de incendio .
Peligros [ editar ]
El flashover es uno de los fenómenos más temidos entre los bomberos . A los bomberos se les enseña a reconocer los signos y síntomas de vuelcos y flashovers y a evitar los errores. Por ejemplo, tienen ciertas rutinas para abrir puertas cerradas a edificios y compartimientos en llamas, conocidos como procedimientos de entrada, lo que garantiza la seguridad de la tripulación de incendios cuando sea posible.
Indicadores [ editar ]
Esta sección necesita citas adicionales para su verificación . (agosto de 2016 ) ( Aprenda cómo y cuándo eliminar este mensaje de plantilla )
|
Las siguientes son algunas de las señales que los bomberos están buscando cuando intentan determinar si es probable que ocurra un flashover.
- El fuego está en un compartimento ventilado, por lo que no hay escasez de oxígeno en la habitación. [ cita requerida ]
- El plano neutral se está moviendo hacia el piso. En esta situación, un flashover es plausible. [ cita requerida ]
- Todos los materiales combustibles directamente expuestos están mostrando signos de pirólisis . [ cita requerida ]
- Los bomberos aparecen " vuelcos " o lenguas de fuego (conocidos como "dedos de ángel" a los bomberos) a medida que los gases alcanzan sus temperaturas de autoignición. [ cita requerida ]
- Hay una rápida acumulación (o "aumento") de la temperatura debido al efecto compuesto de los gases que arden rápidamente (es decir, a la deflagración) y al ciclo térmico que producen. Esta es generalmente la mejor indicación de un flashover. [ cita requerida ]
Los bomberos memorizan un canto para recordar esto durante el entrenamiento: "Humo oscuro y espeso, calor intenso, vuelco, quema libre". [ cita requerida ]
El color del humo a menudo también se considera, pero no existe una conexión entre el color del humo y el riesgo de flashovers. Tradicionalmente, el humo negro y denso se consideraba particularmente peligroso, pero la historia muestra que este es un indicador poco confiable. Por ejemplo, hubo un incendio en una fábrica de colchones de goma en Londres en 1975 que produjo humo blanco. El humo blanco no se consideraba peligroso, por lo que los bomberos decidieron ventilar , lo que causó una explosión de humo y mató a dos bomberos. El humo blanco de la pirólisis de la goma resultó ser extremadamente inflamable.
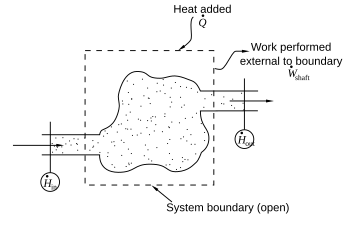
La región del espacio encerrada por los límites del sistema abierto generalmente se denomina volumen de control . Puede o no corresponder a muros físicos. Es conveniente definir la forma del volumen de control para que todo el flujo de materia, dentro o fuera, se produzca perpendicular a su superficie. Uno puede considerar un proceso en el cual la materia que fluye dentro y fuera del sistema es químicamente homogénea. [1] Luego, el material de entrada realiza el trabajo como si estuviera impulsando un pistón de fluido en el sistema. Además, el sistema realiza el trabajo como si estuviera expulsando un pistón de fluido. A través de las paredes del sistema que no pasan la materia, calor ( δ Q ) y el trabajo ( δ W ) transferencias pueden ser definidos, incluyendo el trabajo de eje.
La termodinámica clásica considera procesos para un sistema que inicialmente y finalmente se encuentra en su propio estado interno de equilibrio termodinámico, sin flujo. Esto también es factible bajo ciertas restricciones, si el sistema es una masa de fluido que fluye a una velocidad uniforme. Entonces, para muchos propósitos, un proceso, llamado proceso de flujo, puede considerarse de acuerdo con la termodinámica clásica como si la regla clásica de no flujo fuera efectiva. [2] Para la presente introducción, se supone que la energía cinética del flujo y la energía potencial de elevación en el campo de gravedad no cambian y que las paredes, aparte de la entrada y salida de materia, son rígidas y inmóvil.
En estas condiciones, la primera ley de la termodinámica para un proceso de flujo dice: el aumento en la energía interna de un sistema es igual a la cantidad de energía agregada al sistema por la materia que fluye y por el calentamiento, menos la cantidad perdida por la materia que fluye. Fuera y en la forma de trabajo realizado por el sistema. Bajo estas condiciones, la primera ley para un proceso de flujo se escribe:
donde U in y U out denotan la energía interna promedio que ingresa y sale del sistema con la materia que fluye.
Luego se realizan dos tipos de trabajo: el "trabajo de flujo" descrito anteriormente, que se realiza en el fluido en el volumen de control (a menudo también se denomina " trabajo de PV "), y el "trabajo de eje", que puede ser realizado por Fluido en el volumen de control en algún dispositivo mecánico con un eje. Estos dos tipos de trabajo se expresan en la ecuación:
La sustitución en la ecuación anterior para el volumen de control cv produce:
La definición de entalpía , H = U + PV , nos permite utilizar este potencial termodinámico para explicar conjuntamente la energía interna U y el trabajo PV en fluidos para un proceso de flujo:
Durante la operación de estado estable de un dispositivo ( ver turbina , bomba y motor ), cualquier propiedad del sistema dentro del volumen de control es independiente del tiempo. Por lo tanto, la energía interna del sistema encerrado por el volumen de control permanece constante, lo que implica que d U cv en la expresión anterior se puede establecer igual a cero. Esto produce una expresión útil para la generación de energía o el requisito para estos dispositivos con homogeneidad química en ausencia de reacciones químicas :
Esta expresión se describe en el diagrama de arriba.



































No hay comentarios:
Publicar un comentario