Nematodiasis
La ascariasis es una enfermedad humana causada por el parásito intestinal conocido como Ascaris. Esta enfermedad afecta a la cuarta parte de la población mundial, convirtiéndose en la infección helmíntica más común a nivel mundial, con una alta prevalencia en regiones tropicales y subtropicales y áreas con inadecuadas medidas higiénicas.
Historia
Existen evidencias de la enfermedad desde la Antigüedad. Se han encontrado momias del antiguo Egipto infectadas con este parásito, 2 así como también huevos de A. lumbricoides en coprolitos humanos en Perú que datan aproximadamente del año 2277 a. C.3
Dado el gran tamaño de éste gusano, su existencia debe haber sido bastante obvia, y existen muchos escritos antiguos que hacen referencia a esta infección. El papiro Ebers, del Siglo XV a. C., comenta su existencia y su tratamiento, 4 y tanto Hipócrates como médicos chinos, árabes y romanos escribieron en su momento al respecto.5
Durante muchos años se tenía cierta confusión entre Ascaris lumbricoides y la lombriz de tierra, pero no fue si no hasta el siglo 19, cuando el médico y anatomistabritánico Edward Tyson describió la anatomía comparada entre el parásito y la lombriz de tierra.4
La manera de infectarse no fue muy comprendida hasta el año 1862, cuando el médico francés Casimir Davaine demostró que estaba dada por la ingestión de los huevos, trabajo que fue apoyado por el del naturalista italiano Giovanni Battista Grassi, el que ingirió experimentalmente huevos de A. lumbricoides, y posteriormente encontró huevos del mismo parásito en sus heces.5 Para 1915, Stewart describió el ciclo vital del helminto, incluyendo su paso por los pulmones,6 y en 1922, Koino enJapón ingirió experimentalmente 2000 huevos de Ascaris lumbricoides, 11 días después encontró larvas en su esputo, y días después eliminó 667 gusanos por lasdeposiciones al administrarse un antihelmíntico, estableciendo el ciclo completo.7 8
Características
- Adulto femenino: 20 – 35 cm
- Adulto masculino: 15 – 30 cm
Fisiopatología
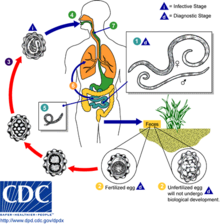
Ciclo vital
Una hembra puede producir alrededor de 200 000 huevos por día, los que son eliminados en las heces. Los huevos no fertilizados al ser ingeridos, no son infecciosos. Los huevos embrionados fértiles se convierten en infecciosos en el ambiente, en un período que va desde los 18 días hasta varias semanas, dependiendo de las condiciones ambientales de humedad ytemperatura
Al ingerir los huevos fértiles, las larvas eclosionan, invaden la mucosa intestinal, atraviesan hacia la circulación porta, y llegan por circulación sistémica a los pulmones y penetran los alvéolos. Las larvas maduran más en los pulmones (10 a 14 días), y luego migran al árbol bronquial y de aquí a la garganta en donde son ingeridos de vuelta al intestino. En el intestino delgado, se convierten en gusanos adultos, los que pueden vivir de 1 a 2 años.4
Causas
La ascariasis es causada por consumir alimentos o bebidas contaminados con huevos de Ascaris. Se encuentra asociada con una higiene personal deficiente, condiciones sanitarias precarias y lugares en los que se utilizan heces humanas como fertilizante.
Mecanismo de daño
Los efectos que provoque en el organismo dependen del lugar donde se encuentre y de su forma evolutiva. Las formas larvarias al atravesar los pulmones pueden provocar hemorragia e inflamación, lo que en forma masiva se conoce como síndrome de Löffler. Eventualmente las larvas podrían no llegar al pulmón y alojarse en otros órganos, provocando una reacción granulomatosa.4
En la mucosa intestinal producen irritación debido a su tamaño y movimiento. También pueden ocurrir complicaciones graves como obstrucción intestinal, e incluso migración de individuos adultos a otros órganos del cuerpo, como el colédoco y las vías biliares. 9
Manifestaciones clínicas
Los gusanos adultos generalmente no causan síntomas agudos, sin embargo, infestaciones por un gran número de individuos pueden causar dolor abdominal agudo yobstrucción intestinal, cuando estos se anudan entre si, y forman un gran bolo. La migración de gusanos adultos puede causar síntomas de oclusión de las vías biliares (colestasis) o expulsión oral. La permanencia de los gusanos en el intestino puede generar diarrea, dolor abdominal difuso, náuseas y vómitos. También pueden causarmalabsorción y anorexia, lo que lleva a la desnutrición. Los niños de 2 a 3 años con ascariasis son al rededor de 2 centímetros más bajos que sus pares no infectados.10
Durante la fase pulmonar de la migración de larvas, síntomas pulmonares pueden ocurrir: tos, disnea, hemoptisis, neumonitis eosinofílica.
Diagnóstico de Laboratorio
El método diagnóstico de ascariasis intestinal es la Identificación microscópica de los huevos en las heces, el examen directo al fresco detecta infecciones de moderadas a fuertes. Para evaluaciones cuantitativas de la infección, se utilizan métodos, como el Kato-Katz.
Las larvas se pueden identificar en el esputo o en el aspirado gástrico durante la fase de la migración pulmonar. Gusanos adultos a veces pasan en las heces o por la boca o la nariz y son reconocibles por sus características macroscópicas.
El diagnóstico de una obstrucción intestinal por Ascaris se logra siguiendo los parámetros de un abdomen agudo. Por lo general se presenta en sujetos con antecedentes de expulsión del gusano. La exploración del paciente demuestra dolor abdominal, vómitos, ausencia de evacuaciones y fiebre con la palpación de ovillos intestinales. La radiología abdominal suele ser necesaria para confirmar el diagnóstico.
Tratamiento
El tratamiento incluye medicamentos de la familia de los benzimidazólicos, la droga de elección es el albendazol a una dosis de 400 mg como dosis única.
Prevención
El acceso a los servicios de agua potable, saneamiento y el mejoramiento de las prácticas de higiene pueden reducir este parásito.
Cómo se contagia la ascariasis?
El gusano áscaris vive en el intestino y sus huevos viajan en las heces de personas infectadas. Si la persona infectada defeca fuera de un inodoro (arbustos cerca, en un jardín o terreno), o si las heces de una persona infectada se utilizan como fertilizante los huevos se depositan en el suelo. A continuación, pueden madurar en una forma que es infecciosa.
La ascariasis es causada por la ingestión de huevos infectantes. Esto puede suceder cuando las manos o los dedos que se han contaminado con la tierra sucia se ponen en contacto con la boca o por el consumo de verduras o frutas que no han sido completamente cocinadas, lavadas o peladas.
Quién está en riesgo de infección?
La infección se produce en todo el mundo en climas cálidos y húmedos, donde el saneamiento y la higiene son pobres, en particular en las zonas templadas durante los meses más cálidos. Las personas en estas áreas están en riesgo si la tierra contaminada con heces humanas entra a la boca o si comen verduras o frutas que no han sido lavados, pelados o cocinados con cuidado.
Cuáles son los síntomas de ascariasis?
Las personas infectadas por Ascaris no muestran síntomas. Si se presentan síntomas, estos pueden ser ligeros e incluyen malestar abdominal. Las infecciones graves pueden causar una obstrucción intestinal y afectar el crecimiento en los niños. Otros síntomas como la tos se deben a la migración de los gusanos a través del cuerpo.
Cómo se diagnostica la ascariasis?
Los médicos pueden diagnosticar ascariasis tomando una muestra de materia fecal y utilizando un microscopio para buscar la presencia de huevos. Algunas personas se dan cuenta que tienen infección cuando encuentran un gusano en sus heces o si al toser se expulsa un gusano (cuando los gusanos migraron del intestino). Si esto le sucediera, guarde el gusano en un recipiente limpio y llévelo a su médico para el diagnóstico.
Cómo puedo prevenir la infección?
- Evite el contacto con el suelo que pudiera estar contaminado con heces humanas, incluso con materia fecal humana ("excrementos") que en algunos lugares se utiliza para fertilizar los cultivos.
- Lávese las manos con agua tibia y jabón antes de manipular alimentos.
- Enseñe a los niños la importancia de lavarse las manos para prevenir infecciones.
- Lavar, pelar o cocinar todos los vegetales y frutas crudos antes de comerlos, particularmente aquellos que se han cultivado en suelo que ha sido fertilizado con estiércol.
La transmisión de la infección a otras personas se puede prevenir de las siguientes maneras:
- No defecar al aire libre
- Utilizando sistemas de eliminación de aguas servidas (negras) eficaces.
Cuál es el tratamiento para la ascariasis?
Medicamentos (drogas antihelmínticas que librar el cuerpo de los gusanos parásitos), como albendazol y mebendazol, son los fármacos de elección para el tratamiento. Las infecciones se tratan por lo general de 1 a 3 días. Los medicamentos recomendados son eficaces.
Cuál es el tratamiento preventivo?
En los países en desarrollo, los grupos con mayor riesgo de infecciones por helmintos transmitidos por el suelo (anquilostomas, Ascaris y triquina) se tratan a menudo sin un examen de heces previo. El tratamiento de esta manera se llama tratamiento preventivo (o "quimioterapia preventiva").
Los grupos de alto riesgo identificados por la Organización Mundial de la Salud son niños de preescolar y niños en edad escolar, mujeres en edad fértil (incluidas las mujeres embarazadas en los trimestres segundo y tercero y madres lactantes) y los adultos en ocupaciones en las que existe un alto riesgo de infecciones graves. Los niños en edad escolar a menudo se tratan por medio de programas de salud escolar y los niños en edad preescolar y mujeres embarazadas en las visitas a las clínicas de salud.
Qué es la administración masiva de medicamentos (MDA)?
El helmintos transmitidos por el suelo (anquilostomiasis, Ascaris y triquina) y otras cuatra "enfermedades tropicales desatendidas" (oncocercosis, la filariasis linfática, la esquistosomiasis y tracoma) a veces se tratan a través de las administraciones masiva de medicamentos. Dado que los medicamentos utilizados son seguros y de bajo costo o donados, se puede ofrecer a los grupos de riesgo tratamientos preventivos.
La administración masiva de medicamentos se lleva a cabo periódicamente (frecuencia anual), comúnmente con los distribuidores de drogas que van de puerta en puerta. Muchas enfermedades tropicales desatendidas son a menudo tratadas simultáneamente con administración masiva de medicamentos.
La dracunculiasis, también conocida como enfermedad de la lombriz de Guinea (GWD) es una dermatosis nodular producida por el crecimiento del parásito Dracunculus en la parte subcutánea de los tejidos de los mamíferos. Esta enfermedad se ha encontrado en humanos, perros, gatos, caballos, ganado, entre otros animales en África y Asia. Una especie similar del Dracunculus, llamada D. insignis, es un parásito que causa dracunculiasis en perros, mapaches, zorros, zorrillos, entre otros en Norteamérica.1 La Dracúnculus medinensis es una lombriz muy larga y delgada.2 El parásito entra a un huésped por medio de la ingestión de agua estancada contaminada con copépodoinfestado con la larva de la lombriz de Guinea. Aproximadamente un año después, la enfermedad se llega a presentar con una sensación dolorosa de ardor cuando la lombriz forma una ampolla, usualmente en alguna extremidad inferior.
Una vez prevalente en 20 países de Asia y África, la enfermedad sigue siendo endémica entre humanos presentándose en solo cuatro países de África.3
La lombriz de Guinea es uno de los parásitos humanos mejor documentados históricamente. La primera mención aparece en la medicina egipcia (en elPapiro Ebers) hacia el 1550 a. C.4 Existen informes sobre el comportamiento del parásito en escritos de cronistas de la Grecia antigua, hacia el siglo II a. C.5
El nombre «dracunculiasis» viene del latín “afección con dragones pequeños”6mientras que el nombre común “lombriz de Guinea” apareció después de que europeos vieron la enfermedad en las costas de Guinea (en el oeste de África) en el siglo XVII.7 El Centro Carter ha predicho que la enfermedad de la lombriz de Guinea “será la primera enfermedad parasitaria que será erradicada y la primera enfermedad que será erradicada sin usar una vacuna o un tratamiento médico”.8
El modo primario de prevención es con el cambio de comportamiento, a un lado de la provisión de fuentes de agua limpia y el tratamiento de agua bebible contaminada con larvicidas. No hay animal o ambiente natural de “D. Medinesis” así que el parásito debe pasar de huésped a huésped para poder sobrevivir.
Signos y síntomas
Conforme la lombriz se mueve hacia abajo, usualmente a la parte baja de la pierna, por el tejido subcutáneo va produciendo un dolor intenso localizado en el trayecto que va dejando. Esta sensación dolorosa de ardor que experimentan las personas infectadas lleva a diagnosticar la enfermedad llamada “la ardiente serpiente”. Otro síntoma incluye fiebre, náuseas y vómito.9
Causa y ciclo de vida
La enfermedad de la lombriz de Guinea es causada por el consumo de agua contaminada por pulgas de agua (microscópicamente conocidas como copépodos) que contienen la larva Dracunculus.9 Esta enfermedad se presentaba en unas de las áreas más pobres del mundo, particularmente en aquellas sin o con acceso limitado a agua limpia.10 En estas áreas, el agua estancada puede contener copépodos que tengan a la larva de la lombriz de Guinea.
La larva se desarrolla por aproximadamente dos semanas dentro del copépodo, en este tiempo la larva puede causar la enfermedad de la lombriz de Guinea si los copépodos infectados no son filtrados del agua bebible.7 La lombriz de Guinea macho es más pequeña que la hembra; en un adulto puede crecer hasta 2 metros de largo y ser tan grueso como un fideo de espagueti.710
Una vez que se encuentra dentro del cuerpo, el ácido estomacal digiere el copépodo pero no a la larva de la lombriz de Guinea que se encuentran dentro. Estas larvas se encuentran en camino a las cavidades del cuerpo donde la hembra se aparea con la lombriz de Guinea macho. Esto toma aproximadamente tres meses después de la infección. La lombriz macho muere después del apareamiento y es absorbido.7 La hembra que tiene la larva excava hacia lo profundo del tejido conectivo, adyacente a los huesos largos o a las articulaciones de las extremidades.7
Aproximadamente un año después de que la infección comienza, la lombriz crea una ampolla en la piel del huésped humano, usualmente en la pierna o pie.11 Pasadas 72 horas desde que la ampolla se rompe, se expone uno de los extremos de la lombriz emergente. Esta ampolla puede causar una sensación de ardor dolorosa conforme la lombriz emerge. Las personas infectadas frecuentemente sumergen la extremidad infectada en agua para aliviar la sensación de ardor. Una vez que se truena la ampolla y es sumergida en agua, la larva hembra libera cientos de miles de larvas de la lombriz de Guinea, contaminando el agua utilizada.
En los siguientes días, la lombriz hembra es capaz de liberar más larvas cuando entre en contacto con agua conforme se extiende su extremo por el hueco de la piel del huésped. Estas larvas contaminan el suministro de agua y son comidas por las pulgas de agua (copépodos), repitiendo de esta manera el ciclo de vida de la enfermedad. Los copépodos infectados pueden vivir en el agua por dos a tres semanas si no son ingeridas. La infección no crea inmunidad, así que una persona puede experimentar esta enfermedad repetitivas veces durante su vida.10
En áreas menos húmedas justo por debajo del desierto del Sahara, han habido casos de enfermedades en épocas lluviosas, que es la mejor fecha para que la comunidad agricultora plante o recolecte. En cualquier otra parte, la lombriz de Guinea se presenta más durante épocas lluviosas, donde los pantanos y los lagos son pequeños y hay más copépodos en ellos. El brote de la enfermedad de la lombriz de Guinea puede causar serios daños a la comida local.10
Prevención
Esta enfermedad puede ser transmitida con solo tomar agua contaminada y puede ser completamente prevenida con dos simples medidas :9
1) Prevenir que la gente tome agua contaminada con copépodos. El copépodo se puede ver en agua clara como partículas blancas nadando.
- Tomar agua que venga solamente de fuentes que estén limpias; como el agua de pozos.
- Tomar agua filtrada usando un filtrador como nilón, que quite a la lombriz de Guinea. Se puede usar tubos con filtro.
- Filtración por medio de filtros de arena o de cerámica.
- Hervir agua.
- Crear nuevas fuentes de agua potable que no tenga parásitos o arreglar a las que no sirvan.
2) Evitar que la gente que está contaminada con la lombriz de Guinea, esté en contacto con fuentes de agua potable, especialmente las usadas para beber.
- El grado de detección y contención en una comunidad es clave. Esto necesita de personal que vaya de puerta en puerta buscando casos y a poblaciones que estén dispuestas a ayudar y a no esconder sus casos.
- Inmersión controlada de lombrices emergentes en una cubeta de agua para reducir el número de larvas en la lombriz del individuo, seguido por descartar el agua en piso seco.
- Desalentar a los miembros de las comunidades de meter los pies en agua potable.
- Controlar guardias que cuiden las fuentes de agua potable y prevenir que personas con la lombriz lleguen a utilizar ese suministro de agua.
Tratamiento
No existe vacuna o medicina para tratar o prevenir la enfermedad de la lombriz de Guinea.9 Una vez que la lombriz comience a emerger el primer paso es llevar a cabo una controlada sumersión del área afectada en una cubeta de agua. Esto impulsa a la lombriz a deshacerse de tantas larvas como pueda, haciendo la herida menos infecciosa. El agua también tiene que ser tirada al piso lejos de una fuente de agua potable. La sumersión resulta en un alivio del ardor y hace la extracción de la lombriz más fácil. Para extraer a la lombriz, la persona tiene que envolver a esta con un pedazo de gasa o palo. El proceso puede ser lento, tomando desde horas hasta meses. Masajear ligeramente el área alrededor de la ampolla puede ayudar a aflojar a la lombriz un poco.8 Este tratamiento es casi igual al que se describe en los textos médicos del Antiguo Egipto.7 Algunas personas tratadas comentan que al remover la lombriz de Guinea, se siente el área afectada como si estuviera ardiendo.12 13 De todas maneras, si la infección es identificada antes de que se forme la úlcera, la lombriz puede ser removida vía quirúrgica por un doctor capacitado.10
A pesar de que la enfermedad de la lombriz de Guinea no es mortal, la herída donde la lombriz emerge puede desarrollar una infección como el tétanos, que puede ser una amenaza a la vida, especialmente en lugares donde hay poco o nulo acceso a un lugar donde puedan ser tratados.14 Analgésicos pueden ser utilizados para ayudar a reducir el hinchazón y el dolor, y los antibióticos untables pueden ayudar a prevenir la infección bacteriana en el área afectada.10 Al menos en la región norte de Ghana, el equipo encargado de estudiar a la lombriz de Guinea descubrieron que antibióticos untados en el área afectada puede causar que la herida sane rápidamente, volviéndose contraproducente ya que hace que la extracción de la lombriz sea más difícil. Se puede usar también aceite de tamale, que lubrica a la lombriz y ayuda a la extracción.
Es de gran importancia no romper la lombriz cuando la extraigan. La lombriz rota puede putrificarse o petrificarse. La putrefacción lleva al desprendimiento de la piel alrededor de la lombriz. La petrificación es un problema si la lombriz está unida o está rodeando una vena u otra área importante.
El uso de metronidazol puede hacer la extracción más fácil, pero también puede hacer que la lombriz migre a otras partes del cuerpo.15
Epidemiología
En 1986 se estimaron 3.5 millones de casos de esta enfermedad, endémica en 20 países de Asia y África.8 Ghana por si solo informó 180 000 casos en 1989. El número de casos se ha reducido desde el 99.98 % al 54.2 % en 2012.16 Este es el número más bajo de casos desde que comenzó la campaña de erradicación. Pero en el 2010, la Organización Mundial de la Salud predijo que faltarán algunos años por venir antes de que la erradicación se logre, basándose en que tomo de 6 a 12 años a los países que ya eliminaron la transmisión de esta enfermedad, después de informar un número similar de casos en Sudán en el 2009.17
La Organización Mundial de la Salud es el grupo internacional que certifica si una enfermedad se ha eliminado de un país o erradicado del mundo.18
Certificado libre
Los países endémicos deben informarse a la Comisión Internacional para la certificación de la erradicación de dracunculiasis y documentar la ausencia de casos por al menos tres años consecutivos. Esto es necesario para ser certificado como un país libre de dracunculiasis por la Organización Mundial de la Salud.19
Los resultados del esquema de certificación han sido remarcables: para el 2007, Benín, Burkina Faso, Chad, Costa de Marfil, Kenia, Mauritania, Togo y Uganda han parado la transmisión y Camerún, República Centroafricana, India, Pakistán, Senegal y Yemen fueron certificados por la Organización Mundial de la Salud.20
Endémico
Al final de 2010, Sudán, Malí y Etiopía seguían teniendo transmisión endémica. Ghana parecía tener éxito al eliminar la transmisión doméstica. En Chad se acababan de descubrir las transmisiones de bajo grado a pesar de no saber si era por una transmisión oculta o una nueva importación. El foco mayor es Sudán del Sur, que informa 94 % de todos los casos en el 2010.21 22 (96 % en 2012).
| Fecha | Sudan del Sur | Mali | Etiopía | Chad | Ghana | Total |
|---|---|---|---|---|---|---|
 |  |  |  |  | ||
| 2007 | 5,81523 | 31323 | 023 | 021 | 3,35823 | 9486 |
| 2008 | 3,61823 | 41723 | 4123 | 021 | 50123 | 4577 |
| 2009 | 2,73317 | 18617 | 2417 | 021 | 24217 | 3186 |
| 2010 | 1,69822 | 5722 | 2122 | 1022 | 822 | 1794 |
| 2011 | 1,02824 | 1224 | 824 | 1024 | 024 | 1058 |
| 2012 | 52124 | 724 | 424 | 1024 | 0 | 542 |
| 2013 | 11324 | 1124 | 724 | 1424 | 024 | 148 (incluyendo 3 exportados a Sudán) |
| 2014 | 7024 | 4024 | 324 | 1324 | 024 | 126 |
| 2015 (hasta el 31 de agosto) | 324 | 124 | 224 | 824 | 024 | 14 (provisional) |
2011
Ghana parece haber erradicado al gusano de Guinea. En agosto de 2011, los policías del sector público informaron que el país estaba libre de casos informados durante más de 14 meses.25 A pesar de esto debido al periodo de incubación de esta enfermedad, va a tomar más tiempo para que la OMS declare a Ghana como completamente libre de la enfermedad.
Para finales de junio de 2011 el número de casos fueron: 2 casos en Chad, 6 en Etiopía, 3 en Malí y 806 casos en Sudán. Después de la separación de Sudán en Sudán Norte y Sudán, el territorio de Sudán Norte se declaró por la OMS, libre de la enfermedad causada por el gusano de Guinea. Para finales de agosto de 2011 el número de casos informados fueron: en Chad 7 casos, Etiopía 8 casos, en Malí 9 casos, en Sudán 944 casos. Todos estos casos ocurrieron en 440 aldeas. De igual manera, un caso se informó en India, lo cual causó controversias debido a que India se había informado como libre de la enfermedad desde el año 2000, por lo que se sospechó que este caso pudo haber sido importado al país.
Durante septiembre de 2011 el número de casos fue: Sudán del Sur 241, Chad 6, Malí 6, Etiopía 1. El número total de casos en el 2011 fue de 1060, de estos 1030 fueron informados desde Sudán, Malí informó 12, Chad informó 10 y Etiopía 8. Los casos en Chad fueron parte de un brote que se identificó originalmente en el 2010 como parte de un proceso de certificación. Chad no informó ningún caso entre el 2001 y el 2009. Dos de los casos en Etiopía fueron importados desde Sudán.
2012
De acuerdo con la OMS el número de casos informados de dracunculiasis han ido disminuyendo a 143 casos entre el 1 de enero al 30 de abril de 2012, a comparación con los 382 casos informados en el mismo periodo durante el 2011. Tan solo Sudán informó 142 casos, que vienen siendo el 99 % del total global, mientras que Etiopía informó solamente un caso.26
El 16 de julio el centro colaborador de investigación de la OMS hizo el informe de “Entrenamiento y erradicación de la dracunculiasis” que señala que el número de casos informados entre el 1 de enero y el 30 de junio de 2012 ha disminiudo de 807 a 391 casos, con un 52 % de mejora. Y también aclaro que por países el número de casos informados era de: Sudán 387, Etiopía 2, Malí 1 y Chad 1.27
El 12 de septiembre el centro colaborador de investigación de la OMS hizo el informe de “Entrenamiento y erradicación de la dracunculiasis” que señala que el número de casos informados entre el 1 de enero y el 31 de agosto de 2012 ha disminuido de 944 casos a 484 en el mismo periodo de 2011, con un 49 % de mejora. También aclaro que el país número de casos informados era de: Sudán con 494, Etiopía 3, Malí 4 y Chad 7.
El 18 de octubre el centro colaborador de investigación de la OMS hizo el informe de “Entrenamiento y erradicación de la dracunculiasis” que señala que el número de casos informados entre el 1 de enero y el 30 de septiembre de 2012 ha disminuido de 1004 casos a 521 en el mismo periodo de 2011, con un 48 % de mejora. Y también aclaro que por países el número de casos informados era de: Sudán 502, Etiopía 3, Malí 7 y Chad 9. En este caso los trabajadores del programa para la erradicación del gusano de Guinea tenían acceso limitado al norte del Malí y no tenían la posibilidad de investigar los casos dentro de esta zona.28
Los resultados provisionales durante el 2012 fueron: un total de 542 casos: Sudán 521, Chad 10, Malí 7, Etiopía 4. Hay una mejoría del 49 % cuando se compara con los resultados del año 2011.29
2013
La OMS declaró provisionalmente la enfermedad como erradicada, ya que no se ha presentado ningún caso hasta la fecha del 11 de febrero de 2013. A pesar de estos prometedores resultados, la OMS menciona que este no es el fin del la dracunculiasis, van a existir casos durante el 2013, pero que cada vez nos vamos acercando a la erradicación total de esta enfermedad.30 El informe también compara los 521 casos en Sudán en el 2012 (de los 542 de forma global) con los 501 casos de Ghana en el 2008 y tomándoles más de 18 meses para eliminar la dracunculiasis de Ghana, con su último caso en mayo de 2010.
Historia del programa de erradicación
La campaña global para erradicar el gusano de Guinea empezó en CDC U.S. Centers for Disease Control and Prevention en 1980. En 1986, el presidente de Estados Unidos de la época, Jimmy Carter y su organización sin fines de lucro The Carter Center, empezaron lidereando la campaña global junto con CDC, UNICEF, andOMS.31 En esta época India, Pakistán, Yemen y otros 17 países en África estaban endémicos por esta enfermedad e informaban un total de 3.5 millones de casos al año.
Jimmy Carter hizo una visita personal a una aldea afectada por el gusano de Guinea en 1988:
En primer lugar, tener encuentros con estas víctimas, principalmente con los adolescentes y los niños pequeños, me impulsaron a mí y a Rosalynn para esforzarnos a impulsar el Centro Carter para erradicar a esta enfermedad.Jimmy Carter32
El presidente Carter también reclutó a dos africanos con poder político para que lo ayudaran a luchar contra la dracunculiasis. Desde entonces, uno de ellos, el generalAmadou Toumani Toure (presidente de Malí), ha luchado a favor de la erradicación del gusano de Guinea en Malí y otros países africanos desde 1992.33 34 Desde 1999, el general Dr. Yakubu Gowan ha cumplido el mismo papel que Amadou Toumani Toure pero en Nigeria, en donde la campaña de erradicación empezó cuando tenía muchos más casos de dracunculiasis que en cualquier otro país.35
Debido a que los humanos son el primer hospedero para el gusano de Guinea no hay evidencia de que esta enfermedad este presente dentro de otra especie. Por lo que podemos prevenir el contagio a diferentes especies si controlamos la enfermedad identificando todos los casos y también controlando el comportamiento de quienes lo padecen.8 36 Una vez que todos los casos humanos con dracunculiasis hayan sido eliminados, su resultado será la erradicación. 8
En 1991, WHA World Health Assembly acordó que la dracunculiasis debería ser erradicada.14 Durante este tiempo había 400 000 casos informados cada año. Simultáneamente, el centro Carter seguía con su programa de erradicación contra la dracunculiasis.37 Otros involucrados importantes para la erradicación de esta enfermedad son: OMS, U.S. Centers for Disease Control and Prevention, Fundación Bill y Melinda Gates, y UNICEF,37 38
En diciembre de 2008, se anunció que el Centro Carter sería el nuevo apoyo financiero, con un total de 55 millones de dólares provenientes de la Fundación Bill y Melinda Gates y del Departmento para el Desarrollo Internacional de Reino Unido.39 Estos fondos ayudaron a identificar e informar los últimos casos de la enfermedad. De acuerdo con el Centro Carter, para que la erradicación se haga realidad se necesita un cuidado intenso hasta en las comunidades más pequeñas para prevenir futuros brotes. En el caso de la dracunculiasis es más difícil realizar esto debido a que el gusano de Guinea tarda un año en incubarse.39
Barreras
La erradicación de la enfermedad causada por el gusano de Guinea tuvo que sobrepasar diferentes obstáculos:
- Seguridad inadecuada en muchos de los países afectados.
- Falta de voluntad y apoyo por parte de los líderes políticos de los países afectados.
- La falta de una vacuna o de un medicamento con eficacia inmediata.
- Falta de recursos durante ciertas épocas.6
Uno de los objetivos más significativos para la erradicación de la dracunculiasis fue la Segunda Guerra Civil en Sudán lo cual hizo este país muy inaccesible debido a la inseguridad.6 40 Para hacer frente a algunas de las necesidades humanitarias en Sudán en 1995 la paz fue lograda gracias a las negociaciones por Jimmy Carter.6 40 A este evento se le conoció como la paz del gusano de Guinea, ambos lados de la guerra civil acordaron mantener la paz durante 6 meses para permitir el paso de funcionarios de salud para comenzar la erradicación de la enfermedad.40 41
Funcionarios públicos de salud publicaron el fin de la guerra civil de Sudán oficialmente en el año 2005, lo cual ayudó muchísimo a la erradicación de la enfermedad.38Aunque quedó Malí, que sigue siendo un obstáculo para la erradicación porque también es muy insegura debido a los rebeldes tuareg.
Otro de los grandes obstáculos respecto a la erradicación de la dracunculiasis fue en Sudán, debido a que había mucha incertidumbre por las elecciones en Sudán durante el 2009, esto causo inseguridad esporádica y conflictos civiles que afectaban a las organizaciones que luchan contra el gusano de Guinea.42 Las comunidades que mantienen la endemia en Sudán son muy remotas y pobres, también los habitantes de estos lugares suelen ser nómadas, mudándose de hogar cada estación del año en búsqueda de agua y de recursos. Esto afecta demasiado porque cuando más se mudan coincide con las temporadas de lluvia por lo que el contagio de dracunculiasis se facilita, debido a esto se necesitan de más intervenciones en contra de la enfermedad en estos lugares.43
Sociedad y cultura
El dolor causado por el gusano de Guinea ocurre normalmente durante las temporadas en las que suelen plantar y cultivar, durante estas épocas las personas no van a trabajar a otros lugares ni suelen asisitir a la escuela por lo que el contagio es menor.8 38
Historia
La dracunculiasis ha sido una enfermedad reconocida desde hace miles de años.
- El gusano de Guinea se ha encontrado calcificado en momias egipcias del II milenio a. C.8
- Durante el siglo II a. C., en la Antigua Grecia, el escritor Agatharchides describió esta enfermedad como endémica en ciertos nómadas en lo que es hoy Sudán.7
- El método tradicional de extraer el gusano de Guinea, enrollando el gusano alrededor de un palo fue la inspiración para el símbolo de Asclepio, en la antigua medicina en Grecia.44
El primero en describir la patología de la dracunculiasis fue un físico búlgaro, Hristo Stambolski, durante su exilio en Yemen (1877-1878).45 Su teoría fue que la causa fue que las personas tomaban agua infectada.

No hay comentarios:
Publicar un comentario