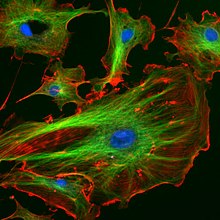
Citoesqueleto
Arp 2/3 (acrónimo inglés para Actin-Related Proteins, es decir, proteínas relacionadas con la actina) es una proteína celular implicada en el control de la disposición de la actina en el citoesqueleto de las células. Es de vital importancia en la fisiología celular y se encuentra ampliamente difundida por todo el dominio de los eucariotas.2 Compuesta por siete subunidades, algunas de ellas poseen una topología claramente relacionada con su función biológica: dos de sus subunidades, denominadas «ARP2» y «ARP3» , poseen una estructura muy semejante a la de los monómeros de actina. Dicha homología permite a ambas unidades comportarse como agentes nucleantes de la polimerización de los monómeros de actina G (actina libre o no polimerizada) a actina F (aquella que se halla en los microfilamentos), una de las funciones del complejo Arp 2/3. Además, este complejo es necesario para establecer estructuras dendríticas complejas de actina F.
Mecanismo molecular de la polimerización
Existe un buen número de proteínas capaces de asociarse al extremo de un microfilamento, afectando a su equilibrio de polimerización/despolimerización, e incluso actuando como agentes nucleantes. Sin embargo, el complejo Arp2/3 no sólo es capaz de modificar la mencionada dinámica, sino que puede generar nuevos lugares de nucleación y, por tanto, ramificar la estructura. Dicha actividad nucleante es estimulada mediante las proteínas reguladoras de las familias WASp, N-WASp yWAVE. En el caso de las WASp, dicha activación se desprende de la interacción mediante su dominio V con los monómeros de actina al tiempo que su región CA se asocia a Arp2/3, dando lugar a un centro de nucleación. Claro que la nucleación de novo no es suficiente para generar redes de actina F: es preciso que los nuevos microfilamentos, además, se entrelacen con otros preexistentes, dando lugar a un citoesqueleto de actina funcional.4 Según este modelo, las proteínas que recubren el extremo del microfilamento poseen dos funciones: limitar la polimerización de éste si no es mediante la región nucleante del complejo Arp2/3 y prevenir su despolimerización, a fin de mantener su estabilidad.5
Por tanto, el complejo Arp2/3 controla simultáneamente tanto la polimerización de la actina como la ramificación de los microfilamentos. Más aún, se ha descrito una actividad de autocatálisis durante la polimerización de actina mediada por el complejo: en ella, los nuevos microfilamentos activan a otros complejos Arp2/3, lo cual incrementa la complejidad de la estructura, facilitando el desarrollo de tramas más elaboradas.
El mecanismo molecular por el cual Arp2/3 interviene en la polimerización de la actina es objeto de disputa. Se han postulado dos modelos: en uno, la bifurcación es externa al microfilamento madre, mientras que, en el otro, es interna. No existen datos empíricos que permitan, hasta abril de 2008, aceptar o rechazar concluyentemente alguno de estos modelos, los cuales se describen a continuación.
Modelo de bifurcación externa al microfilamento
El modelo de bifurcación externa al microfilamento propone una nucleación dendrítica, en la cual el complejo Arp2/3 se une a un lateral de un microfilamento preexistente, dejando libres sus lugares de nucleación. De este modo, se postula que el complejo posee capacidad de unir a actina en al menos dos zonas: una para interactuar con la actina F original y otra con la de nueva síntesis. Existen evidencias de microscopía electrónica de alta resolución que respaldan estructuralmente este modelo.6 7
Modelo de bifurcación interna al microfilamento
En el modelo de bifurcación interna al microfilamento se postula que Arp2/3 se asocia al extremo de un microfilamento en crecimiento, permitiendo tanto la adición de nuevos monómeros a éste como a una rama hija, que nuclea en el complejo Arp2/3.4 Dicha dicotomía se explica sobre la base de la existencia de dos subunidades activas, tanto Arp2 como Arp3, capaces de interactuar con un microfilamento creciente de forma paralela. Esta hipótesis se basa en análisis cinéticos, pero no posee soporte en cuanto a estructura molecular de las proteínas se refiere.
Funciones
Arp2/3, como elemento ubicuo en los eucariotas y relacionado con una función tan vital como es el mantenimiento del citoesqueleto de actina, posee multitud de funciones celulares específicas. El complejo es especialmente abundante en aquellas zonas de la célula que posean una dinámica activa de la polimerización de actina: por ejemplo, en los lamelipodios de protozoosy en las zonas motiles de levaduras.8 De hecho, se ha detectado que tanto Arp2/3 como las proteínas reguladoras WAVE se acumulan selectivamente en los ápices de dichos lamelipodios, cuya formación es, además, esencial durante la migración celular en metazoos.9
En mamíferos y en la ameba Dictyostelium discoideum se ha demostrado que es imprescindible para la fagocitosis.10 11 Además, el complejo posee relevancia en el establecimiento de la polaridad celular y en la propia migración de algunos tipos celulares, como puede ser el caso de fibroblastos en zonas que han sufrido un trauma mecánico.12 Es más, existen casos de patógenosprocariotas que, aunque no presentan Arp2/3 por carecer de citoesqueleto, emplean el complejo Arp2/3 de la célula hospedadora cuando la infectan: es el caso de las cepas enteropatogénicas de Listeria monocytogenes y Shigella, que aprovechan la polimerización de la actina como medio motriz para desplazarse por el citosol y colonizar células vecinas.13 Otra función consiste en la regulación de los orgánulos asociados al citoesqueleto, como son los endosomas, lisosomas, vesículas de pinocitosis y mitocondrias.14 En levaduras el transporte mitocondrial depende de los microfilamentos de actina, a diferencia de los eucariotas superiores, en que depende de microtúbulos. Se ha demostrado que la forma principal de realizar el transporte anterógrado mitocondrial es a través del complejo arp 2/3, que es reclutado en la membrana externa mitocondrial a través de las proteínas Jsn1/Puf1. Como este complejo produce propulsión, pero no direccionalidad, esta se logra mediante la paralelización de los microfilamentos y la unión de los "cables" de actina a otro elemento de la membrana mitocondrial llamado "mitocoro", formado por las proteínas Mmm1, Mdm10 y Mdm12, quienes a su vez se unen al complejo arp 2/3 mediante la proteína Puf3. Los mutantes con defectos en arp 2/3 o elementos del mitocoro presentan a su vez problemas en el transporte mitocondrial y en su segregación en la división celular.15 En el caso de las plantas, es esencial para que se produzca una expansión polar de las células de los tricomas y delhipocótilo.16 17 18
Implicaciones en el desarrollo
Como se describió previamente, el complejo Arp2/3 también se encuentra en plantas. Por ejemplo, su subunidad de menor tamaño posee un homólogo, ARPC5, en elorganismo modelo Arabidopsis thaliana.19 De hecho, en esta especie se han descrito mutantes que carecen de dicha subunidad, y su fenotipo, que puede fenocopiarsepor adición de drogas que inhiben la polimerización de la actina, consiste en irregularidades en los tricomas. Por otra parte, el papel fundamental del citoesqueleto de actina en el tráfico de vesículas provoca que, en los mutantes carentes de una correcta función de Arp2/3, el comportamiento de las vesículas asociadas al complejo de Golgi sea anómalo; por añadidura, y puesto que dicho tráfico es el que puede sustentar una expansión celular, si las vesículas transportan componentes celulares de nueva síntesis, dichas anomalías repercuten en la fisiología celular de una forma estructural. De este modo, se ha comprobado que en las plantas Arp2/3 posee un papel esencial en la morfogénesis.19 De hecho, se ha postulado que en las plantas Arp2/3, junto con las fosfolipasas que interactúan con la membrana y los microtúbulo de actina, forman un sistema de cooperación intracelular que desempeñan un papel central en definir la forma definitiva de las células.20
Otros estudios en animales modelo, como Drosophila melanogaster, y en levaduras han demostrado que las mutaciones de pérdida de función en ARP3 son letales, lo cual pone de manifiesto el papel crucial de este complejo durante el desarrollo.

CapZ es una proteína de unión a actina que se une a los extremos (+) de los microfilamentos. Su estructura consiste en un heterodímero con una subunidad alfa y otra beta. Su función molecular es la regulación del ensamblaje de actina por estabilización de los oligómeros en elongación. Presente en el músculo esquelético, constituye la llamada banda Z del sarcómero.1 Se han descrito cuatro genes codificantes para CapZ en humanos, tres para subunidades alfa y uno para subunidades beta: CAPZA1,2 CAPZA2,3 CAPZA34 y CAPZB.
El centro organizador de microtúbulos (COMT) es una estructura que se encuentra en las células eucariotas de la que surgen los microtúbulos. Los COMTs tienen dos funciones principales: la organización de los flagelos eucarióticos y los cilios y la organización del aparato del huso mitótico y meiótico, que separan los cromosomas durante la división celular. El COMT es un importante sitio de nucleación de microtúbulos y se puede visualizar en las células mediante la detección inmunohistoquímica de γ-tubulina. Las características morfológicas de COMT varían entre los diferentes filos y reinos. En los animales, los dos tipos más importantes de COMT son los cuerpos basales asociados con cilios y el centrosoma asociado con la formación del huso.1En los animales, los dos tipos más importantes de COMT son los cuerpos basales asociados con cilios y el centrosoma asociado con la formación del huso.
Organización de los COMTs en células
La función organizadora de centros de microtúbulos ocurre tanto en el sitio donde se inicia la formación de microtúbulos, así como en un lugar donde los extremos libres de los microtúbulos son atraídos.2 Dentro de las células, los centros organizadores de microtúbulos pueden adoptar muchas formas diferentes. Una matriz de microtúbulos puede organizarse a sí misma en una estructura de molinete para formar los cuerpos basales, que pueden conducir a la formación de matrices de microtúbulos en el citoplasma o la estructura "9+2" del axonema. Otros arreglos van desde cuerpos polares del husillo fúngico hasta los cinetocoros eucariotas cromosómicos (planos, laminados placas). Los COMTs pueden dispersarse libremente por todo el citoplasma o localizados centralmente como focos. Los COMT más notables son el centrosoma en la interfase y los polos del huso mitótico.
Los centríolos pueden actuar como marcadores para los COMTs en la célula.2 Si se distribuyen libremente en el citoplasma, centríolos pueden reunirse durante la diferenciación para convertirse en COMTs. También pueden centrarse en torno a un centrosoma como un único COTM, aunque los centrosomas pueden trabajar como COTMs ausentes de los centríolos.
Inferfase COMT
La mayoría de las células animales cuentan un COTM durante la interfase, normalmente se encuentra cerca del núcleo, y generalmente asociado en estrecha colaboración con al aparato de Golgi. El COTM se compone de un par de centriolos en su centro, y está rodeado con material pericentriolar (MPC) que es importante para la nucleación de microtúbulos. Los microtúbulos están anclados en el COTM por medio de sus extremos menores, mientras que más cerca estén de su final continuarán creciendo en la periferia celular. La polaridad de los microtúbulos es importante para el transporte celular, ya que las proteínas quinesina y dineína suelen impulsarse preferencialmente en la dirección —bien sea “más” o “menos”, respectivamente— a lo largo de un microtúbulo, lo que permite a las vesículas ser dirigidas hacia o desde el retículo endoplásmico y el aparato de Golgi. En particular, para el aparato de Golgi, sus estructuras están asociadas con el aparato de desplazamiento que se dirige hacia extremo menor de un microtúbulo y la ayuda en la estructura general y el sitio del aparato de Golgi en la célula.3
Centrosomas
Los movimientos de los microtúbulos se basan en las acciones del centrosoma.1 Cada célula hija tras haber finalizado la mitosis contiene un COMT primario.2 Antes de que comience la división celular, la interfase COMT reproduce para formar dos COMT distintos (ahora se hace referencia habitualmente como centrosomas). Durante la división celular, estos centrosomas se mueven hacia los extremos opuestos de la célula y microtúbulos nucleados para ayudar a formar el huso mitótico/meiótico. Si el COMT no logra replicarse, entonces no se formará el huso, y la mitosis cesará antes de tiempo.1 (Información más detallada en el artículo centrosoma.)
La γ-tubulina es una proteína situada en el centrosoma que nuclea los microtúbulos mediante la interacción con el monómero de la subunidad de la tubulina en los microtúbulos en el extremo menor.1 La organización de los microtúbulos en el COMT, o centrosoma en este caso, está determinada por la polaridad de los microtúbulos definidos por γ-tubulina.1
Cuerpo basal
En las células epiteliales, los COMTs también sujetan y organizan los microtúbulos que forman cilios. Al igual que con el centrosoma, estos COMTs estabilizan y orientan a los microtúbulos, en este caso para permitir el movimiento unidireccional del propio cilio, en lugar de vesículas que circulen a través de ella.
Cuerpo polar del huso
En levaduras y algunas algas, la COMT se incrusta en la envoltura nuclear como un cuerpo polar del huso. Los centríolos no existen en los COMTs de levaduras y hongos.1 En estos organismos, la envoltura nuclear no se descompone durante la mitosis y el cuerpo polar del huso sirve para enlazar el citoplasma con los microtúbulos nucleares. El cuerpo polar del huso en forma de disco está organizado en tres capas: placa central, placa interior y placa exterior. La placa central está integrada en la membrana, mientras que la placa interior es un nivel intranuclear amorfo, y la placa exterior es la capa situada en el citoplasma.1
COMTs en las plantas
Las células vegetales carecen de centríolos o cuerpos polares del huso excepto en sus gametos masculinos flagelados, y son totalmente ausentes en las coníferas yplantas con flores.4 En su lugar, la propia envoltura nuclear parece funcionar como el COMT principal para la nucleación de microtúbulos y la organización del huso durante la mitosis de la célula vegetal.
Transducción de señales
El COMT se reorienta durante la transducción de señales, principalmente durante la reparación de heridas o respuestas inmunitarias.5 El COMT se relocaliza a una posición entre el borde de la célula y el núcleo en las células como los macrófagos, fibroblastos, y células endoteliales. Los orgánulos —como el aparato de Golgi— ayudan en la reorientación del COMT que puede ocurrir rápidamente. Las señales de transducción causan que los microtúbulos crezcan o se contraigan, así como hacer que el centrosoma obtenga motilidad. El COMT se encuentra en una posición perinuclear y contiene los extremos negativos de los microtúbulos, mientras que los extremos positivos crecen rápidamente hacia el borde de la célula. El aparato de Golgi se reorienta junto con el COMT, y en conjunto producen que la célula envíe aparentemente una señal polarizada.5
Para las respuestas inmunitarias —sobre la interacción con una célula objetivo en respuesta a antígenos específicos intencionados de células que presentan antígenos, células inmunes, tales como las células T, células asesinas naturales y linfocitos T citotóxicos—, localizan sus COMTs cerca de la zona de contacto entre la célula inmune y la célula objetivo. Para las células T, la respuesta de señalización del receptor de células T hace que la reorientación del COMT por los microtúbulos de acortamiento llevan el COMT hacia el sitio de interacción del receptor de células T.



No hay comentarios:
Publicar un comentario