Cianotoxinas
Las cianotoxinas son toxinas producidas por un grupo de bacterias denominado cianobacterias (incluidas dentro de las llamadas algas verdeazuladas, aún siendo una bacteria).
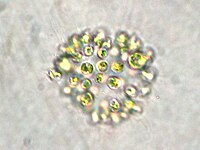
Las cianobacterias se encuentran en casi todos los lugares, pero especialmente se desarrollan en lagos y océanos en los que, bajo ciertas condiciones especiales, se reproducen exponencialmente formando grandes floraciones. Las floraciones de cianobacterias pueden producir cianotoxinas en tales concentraciones que pueden ser venenosas e incluso mortales para animales y humanos. Las cianotoxinas se pueden acumular también en pescados y mariscos, causando intoxicaciones por su ingesta.
Algunas de estas cianotoxinas son uno de los tóxicos naturales conocidos más fuertes, provocando en algunos casos una muerte rápida por fallos respiratorios (Stewart et al., 2008).
La exposición recreativa ante cianobacterias puede producir síntomas gastrointestinales, fiebre del Heno o erupciones cutáneas pruriginosas (Stewart et al., 2006). Se piensa que una exposición significativa de altos niveles de algunas cianobacterias puede causar esclerosis lateral amiotrófica, pero no existen evidencias firmes.
Existe además un interés militar en el potencial de ciertas toxinas como las cianotoxinas que "han adquirido cada vez más importancia como candidatos potenciales para usarlos como armas".(Dixit et al., 2005).
El primer informe publicado sobre los posibles efectos letales que las cianobacterias pudieran provocar apareció en la revista Nature, en 1878. George Francis describió las floraciones de algas en el estuario del río Murray en Australia como "una espesa espuma, como una pintura aceitosa verde, de alrededor de dos a seis pulgadas de grosor." Los animales que bebieron del agua murieron de forma rápida y terrible. (Francis, 1878)
La mayoría de los informes sobre envenamiento por toxinas de microalgas indican que ocurrieron en ambientes de agua dulce, pero son cada vez más comunes y se dan en áreas más extensas. Por ejemplo, miles de patos y gansos murieron a causa de beber agua contaminada en el mediooeste de Estados Unidos. En 2010 se documentaron por primera vez casos de muertes de mamíferos marinos por la ingesta de cianotoxinas.
Cianobacteria
Las cianotoxinas son producidas por las cianobacterias, un filo de bacterias que obtienen su energía a través de la fotosíntesis. El prefijo cian proviene del griego κύανoς que significa "sustancia de color azul oscuro", y normalmente se refiere a cualquier color en la gama azul/verde del espectro. Comúnmente las cianobacterias son llamadas cianofíceas o algas verdeazuladas. Tradicionalmente se pensaba que las cianobacterias eran un tipo de alga, y así se referían a ellas en los libros. Sin embargo las fuentes modernas consideran esta clasificación obsoleta (Nabors & Murray, 2004), por lo que ahora se considera que están más relacionadas con las bacterias (Guiry et al., 2007), y el término de alga se restringe únicamente a las algas eucariotas (Allaby, 1992). Al igual que estas últimas, las cianobacterias son fotosintéticas por lo que contienen pigmentos fotosintéticos, razón por la cual poseen un color verdoso o azulado.
Las cianobacterias habitan en casi todas partes; en océanos, lagos, ríos así como en tierra firme. Crecen en lagos árticos y antárticos (Skulberg, 1996), en fuentes termales (Castenholz, 1973) y en los tratamientos de las aguas residuales (Vasconcelos & Pereira, 2001). Habitan incluso en el pelaje de los osos polares a los cuales les da un tono verdoso (Karp, 2009). Las cianobacterias producen tóxicos potentes, pero también sintetizan compuestos bioactivos útiles, incluyendo sustancias antitumorales, antivirales, anticancerígenas, antibióticas, antifúngicas, protectoras de la radiación ultravioleta e inhibidores específicos de ciertas enzimas. (Herrero & Flores, 2008) (Sinonen & Jones, 1999)
Floraciones masivas de algas
Las cianotoxinas están a menudo implicadas en lo que comúnmente se conoce como Mareas Rojas o floraciones nocivas de algas ("blooms"). Los lagos y océanos contienen gran cantidad de organismos unicelulares o fitoplancton. En ciertas condiciones, especialmente cuando las concentraciones de nutrientes son altas, estos organismos se reproducen de forma exponencial. En consecuencia se forma una densa nube de fitoplancton sobre el agua llamada "bloom" que puede extenderse sobre cientos de kilómetros cuadrados de superficie y se pueden visualizar fácilmente en imágenes de satélites. Por sí mismo, el fitoplancton no suele perdurar más que unos días, pero estas floraciones pueden durar semanas.(Lindsey & Scott, 2010)
Generalmente estas blooms son inofensivas, pero en ocasiones pasan a ser nocivas al contener toxinas o patógenos que causan la muerte de peces e incluso de humanos. En ambientes marinos, las floraciones nocivas de algas están mayormente causadas pordinoflagelados, (Stewart & Falconer, 2008) a pesar de que otros grupos de algas pueden causarlas (diatomeas, flagelados,haptofitas y rodofíceas). Las especies marinas de dinoflagelados son frecuentemente tóxicas, en cambio las especies de agua dulce no son conocidas por serlo. Tampoco lo son las diatomeas, al menos para el ser humano (Vasconcelos, 2006).
En ecosistemas de agua dulce, las floraciones de algas son causadas normalmente por la eutrofización. Los brotes se parecen a espuma, verdín o pintura que flota sobre la superficie del agua, aunque no siempre son visibles. Tampoco han de ser siempre de color verde; pueden ser de color azul, incluso algunas especies de cianobacterias aportan un tono marrón o rojizo.
Una floración fuerte de cianobacterias puede reducir la visibilidad a uno o dos centímetros de profundidad. Las especies que no necesitan ver para migrar dentro de la columna de agua (como las propias cianobacterias) consiguen sobrevivir, pero la posibilidad de supervivencia para aquellas especies que sí necesitan visión para encontrar alimento o relacionarse con otros organismos, queda reducida. Durante del día la floración de cianobacterias satura el agua en oxígeno, en cambio por la noche la respiración de los organismos acuáticos puede agotar el oxígeno hasta el punto de que las especies más sensibles, como algunos peces, mueren. Es más probable que esto ocurra cerca del fondo marino o de la termoclina. La acidez del agua también sigue ciclos diarios a lo largo de una floración de algas. Durante el día se alcanzan pH del orden de 9 o incluso más altos, mientras que por la noche el pH cae a valores mucho más bajos. Además muchas especies de cianobacterias producen potentes cianotoxinas en gran concentración hasta el punto en el que son letales para algunos organismos acuáticos cercanos y para otros animales al contacto directo con la floración, como pájaros, animales de granjas o domésticos e incluso humanos en ciertas ocasiones.(Vasconcelos, 2006)
En 1991, una floración de cianobacterias afectó a 1000 kilómetros del río Darling-Barwon en Australia (Forc, N.S.W.B.G.A.T. 1992), y supuso un coste económico de 10 millones de dolares australianos (6,97 millones de euros). (Herath, 1995)
Estructura química
Las cianotoxinas se divide en tres grandes grupos en función de su estructura química: los péptidos cíclicos, los alcaloides y los policétidos
| Estructura | Cianotoxina | Principales órganos o funciones afectados en mamíferos | Género de cianobacterias que lo producen |
|---|---|---|---|
| Péptidos cíclicos | Microcistinas | Hígado | Microcystis, Anabaena, Planktothrix(Oscillatoria), Nostoc, Hapalosiphon,Anabaenopsis |
| Nodularinas | Hígado | Nodularia | |
| Alcaloides | Anatoxina-a | Sinapsis nerviosa | Anabaena,Planktothrix(Oscillatoria), Aphanizomenon |
| Anatoxina-a(S) | Sinapsis nerviosa | Anabaena | |
| Cilindrospermopsina | Hígado | Cylindrospermopsis, Aphanizomenon, Umezakia | |
| Lyngbyatoxin-a | Piel, tracto gastrointestinal | Lyngbya | |
| Saxitoxinas | Axones Nerviosos | Anabaena,Aphanizomenon,Lyngbya,Cylindrospermopsis | |
| Lipopolisacáridos | Irritante potencial, afecta a cualquier tejido expuesto | Todas | |
| Policétidos | Aplasiatoxina | Piel | Lyngbya, Schizothrix,Planktothrix(Oscillatoria) |
La mayoría de las cianotoxinas tienen un número de variantes (análogos). En total se conocen unas 84 cianotoxinas sin embargo sólo han sido bien estudiadas unas pocas.
Péptidos cíclicos
Un péptido es un polímero corto de aminoácidos unidos por enlaces peptídicos. Poseen la misma estructura química que las proteínas, con la excepción de que son cadenas más cortas. En un péptido cíclico, la cadena de aminoácidos se vuelve a unir al principio de ésta, formando una cadena circular estable. Para los mamíferos dicha estabilidad hace que sean resistentes a la digestión y se pueden acumular en el hígado. De todas las cianotoxinas, los péptidos cíclicos son los que más afectan a la salud humana. Las microcistinas y nodularinas son tóxicas para el hígado y en altas dosis pueden causar la muerte. (Chorus & Bartram, 1999)
Microcistinas
Como las demás cianotoxinas, las microcistinas fueron nombradas después de descubrir el primer organismo que las producía, en este caso Microcystis aeruginosa. Sin embargo, más tarde se encontró otro género de cianobacterias que también las produce (Chorus & Bartram, 1999). Existen unas 60 variantes conocidas de microcistinas, y muchas de ellas son producidas durante una floración. La microcistina más documentada es la microcistina-LR, posiblemente porque fue la primera de la cual estuvo disponible comercialmente su análisis estándar químico. (Chorus & Bartram, 1999)
Las proliferaciones que contienen microcistinas son un problema mundial. (Pelaez et al., 2010). Las microcistinas son péptidos cíclicos y pueden ser muy tóxicos para plantas y animales incluyendo humanos. Se acumulan en el hígado de los peces, en elhepatopáncreas de mejillones, y en el zooplancton. Son hepatotóxicas y causan serios daños para el hígado de los humanos.(Chorus & Bartram, 1999) En esto son similares a las nodularinas (abajo), y juntas, representan la mayor parte de las proliferaciones tóxicas de cianobacterias en aguas dulces y salobres.(Sinonen & Jones, 1999). En 2010, se documentó el envenanamiento de un número de nutrias marinas a causa de microcistinas. La fuente más probable de toxicidad por mariscos hepatotóxicos eran los bivalvos marinos. Este es el primer caso confirmado de mamíferos marinos que mueren intoxicados por ingestión de cianotoxinas.(Miller et al., 2010)
Nodularinas
La primera variante de nodularina identificada fue la Noduarina-R, producida por la cianobacteria Nodularia spumigena (Sivonen K, Kononen K, Carmichael WW, Dahlem AM, Rinehart KL, Kiviranta J, Niemela SI (1989)). Esta cianobacteria crece en todas las masas de agua del mundo. En el mar Báltico, la floración marina de Nodularia spumigena es uno de los eventos más grandes del mundo en cuanto a masas cianobacteriales. (David et al., 2009)
En general, los péptidos cíclicos producidos por la familia nodularia son las toxinas más comunes en una floración de cianobacterias, tanto en agua dulce como salobre. Al igual que las microcistinas (arriba), las nodularinas son hepatoxinas muy potentes y dañan gravemente el hígado. Suponen un riesgo para la salud de animales salvajes o domésticos así como para los humanos, y en muchas zonas plantean un reto importante en el abastecimiento de agua potable. (Sinonen & Jones, 1999)
Alcaloides
Los alcaloides son un grupo de compuestos químicos naturales que contienen principalmente átomos básicos de nitrógeno. Muchas variedades de organismos los producen, incluyendo las cianobacterias. También forman parte del grupo de los metabolitos secundarios. Los alcaloides actúan sobre diversos sistemas metabólicos de los humanos y otros animales, provocando a menudo efectos psicotrópicos o tóxicos. Suelen aportar un sabor amargo. (Rhoades & David, 1979)
Anatoxina-a
Las investigaciones sobre la anatoxina-a, también conocida como "el factor de muerte rápida", comenzaron en 1961 tras la muerte de vacas que bebieron agua de un lago en el que se dio una floración masiva de algas en Saskatchewan, Canada. (Carmichael & Gorham, 1978) (Carmichael et al., 1975). Al menos cuatro géneros diferentes de cianobacterias producen esta toxina, encontrada en NorteAmérica, Europa, África, Asia y Nueva Zelanda. (Yang, 2007)
Los efectos tóxicos de la anatoxina-a son muy rápidos porque actúa directamente en las células nerviosas (neuronas) como unaneurotoxina. Los síntomas progresivos ante una exposición de anatoxina-a son la pérdida de concentración, espasmos, convulsiones y finalmente la muerte rápida por parálisis respiratoria. Los tejidos nerviosos que se comunican con los músculos contienen un receptor llamado receptor nicotínico de acetilcolina. La estimulación de estos receptores causa una contracción muscular. La molécula de anatoxina-a tiene una estructura tal que se encaja en este receptor, como lo hace el neurotransmisor natural que es la acetilcolina. Una vez que se produce la contracción del músculo, la anatoxina-a no permite que las neuronas vuelvan a su estado de reposo, ya que la toxina no es degradada por la colinesterasa, que habitualmente si lo hace con la acetilcolina. Debido a esto la célula muscular queda contraída permanentemente, la comunicación entre el cerebro se interrumpe y la respiración cesa. (Wood et al., 2007)
Cuando la toxina fue descubierta, se la denominó Very Fast Death Factor (VFDF) debido a que al ser inyectada en ratones causaba temblores, parálisis y finalmente la muerte en pocos minutos. En 1977, se la denominó como amina alcaloide bicíclica y pasó a llamarse anatoxina-a (Devlin et al., 1977) (Moore, 1977). Estructuralmente es una sustancia similar a la cocaína. Existe un interés continuo sobre la anatoxina-a debido a los peligros que presenta para las aguas de recreo o potables, y porque es una molécula particularmente útil para investigar los receptores de la acetilcolina en el sistema nervioso.( Stewart et al., 2008) La letalidad de la toxina indica que tiene un alto potencial militar como arma biológica. (Dixit et al.,2005)
Cilindrospermopsinas
Las Cilindropermopsinas (abreviado como CYN o CYL) fueron descubiertas después de un brote de una misteriosa enfermedad en Palm Island (Australia) (Byth S (July 1980)). Dicho brote fue causado por una floración de Cylindrospermopsis raciborskii en el suministro de agua potable local, identificándose posteriormente la toxina. El análisis de la toxina reveló la estructura química propuesta en 1992, lográndose susíntesis en el 2000. Desde entonces se han aislado o sintetizado una gran cantidad de variedades de cilindrospermopsinas.(Griffiths & Saker, 2003)
La cilindrospermopsina es tóxica para el hígado y los tejidos del riñón y se piensa que puede inhibir la síntesis de proteínas así como modificar covalentemente el ARN y/o el ADN. Existe una preocupación debido a la bioacumulación de la cilindrospermopsina en organismos de agua dulce. (Kinnear, 2010) Las floraciones de géneros productores de cilindrospermopsinas se encuentran con mayor frecuencia en aguas de áreas tropicales, subtropicales o áridas, encontrándose recientemente floraciones de este tipo en Australia, Europa, Israel, Japón y EEUU. (Chorus & Bartram, 1999)
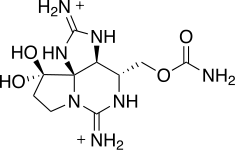
Saxitoxinas
La saxitoxina (STX) es una de las neurotoxinas naturales más potentes que se conocen. El término de saxitoxina proviene del nombre de la especie de la almeja de la mantequilla (Saxidomus giganteus) , gracias a la cual se reconoció la toxina por primera vez. La saxitoxina es producida por Anabaena spp., algunas Aphanizomenon spp., Cylindrospermopsis sp., Lyngbyasp. y Planktothrix sp. (Clark et al.,1999). El pez globo y algunos dinoflagelados marinos también son productores de la saxitoxina. (Nakamuraa et al., 1984) (Landsberg, 2002). Las saxitoxinas se acumulan en los mariscos y algunos peces. La ingestión de saxitoxina a través de marisco contaminado por algas tóxicas, puede producir una intoxicación que cause parálisis.(Sinonen & Jones, 1999)
Las saxitoxinas se han usado en la biología molecular para establecer la función del canal de sodio. Actúa sobre los canales de sodio dependientes del voltaje de las células nerviosas, impidiendo una función celular correcta y conduciendo a la parálisis. El bloqueo de los canales neuronales de sodio consecuencia de una intoxicación paralítica por marisco produce una parálisis "relajada" que deja a la víctima calmada y consciente de la progresión de los síntomas. La muerte se produce por una insuficiencia respiratoria.(Kao & Levinson, 1986). La saxitoxina fue aislada y descrita por primera vez por el ejército estadounidense, que le dio el nombre de arma química "TZ". La saxitoxina aparece en el anexo 1 de la Convención sobre Armas Químicas. De acuerdo con el libro Spycraft, a los pilotos de aviones estadounidenses de reconocimiento U-2 se les proporcionó agujas que contenían saxitoxinas para usarlas como método de suicidio en caso de que la huida fuera imposible. (Wallace et al., 2009)
Lipopolisacáridos
Los lipopolisacáridos se encuentran en todas las cianobacterias. Parece que no son tan potentes como otras cianotoxinas. Algunos investigadores afirman que todos los lipopolisacáridos procedentes de cianobacterias pueden irritar la piel, mientras que otros dudan de que los efectos tóxicos sean tan generalizados (Stewart et al., 2006).
Policétidos
Los policétidos son metabolitos secundarios de bacterias, hongos, plantas y animales. Son biosintetizados por la polimerización de subunidades de acetilo y propioniloen un proceso similar a la biosíntesis de ácidos grasos. Son los bloques de construcción para un amplio rango de productos naturales.
Los policétidos son estructuralmente una familia muy diversa de productos naturales con actividades biológicas y propiedades farmacológicas diversas. En uso comercial hay antibióticos, antifúngicos, citostáticos, anticolesterolémicos, antiparasíticos, promotores del crecimiento animal, e insecticidas naturales.
Aplisiatoxinas
Es la toxina más representativa de este grupo, se clasifica como dermatotoxina, provoca irritaciones y dermatitis severas si hay contacto cutáneo. En caso de ingestión accidental producen inflamación gastrointestinal. Son producidas por cianobacterias como Lyngbya sp., Oscillatoria sp. y Schizothrix sp..
Distribución de cianotoxinas en aguas españolas
Las cianobacterias son abundantes en alrededor del 50% de los embalses investigados. Los datos sobre toxicidad indican que alrededor del 65% de las muestras en las que las cianobacterias eran abundantes presentaban cianotoxinas (50). Combinando ambos datos se puede decir que alrededor del 25% de los embalses españoles pueden presentar en algún momento cianotoxinas en concentraciones variables. Las toxinas más habituales en aguas españolas son las microcistinas, y en particular la variante LR, que es muy tóxica. (Quesada et al., 2004)
Legislación española
España es uno de los pocos países que posee legislación concreta respecto a las cianotoxinas en aguas de consumo. El Real Decreto 140/2003 establece el valor de 1 µg/L de microcistinas totales a la salida de las estaciones de tratamiento de agua potable (ETAP), pero no establece que tipos de microcistinas se han de medir ni recomienda ninguna metodología para hacerlo. El resto de variantes de cianotoxinas, como la cilondrospermopsina, que ha sido encontrada en aguas españolas en concentraciones elevadas, no están incluidas en el Real Decrreto. (Quesada et al., 2004)
En cuanto a las aguas de recreo, no hay ninguna legislación, pero si hay recomendaciones de la OMS que sugieren no permitir el acceso a la zona recreativa en presencia de más de 2000 células de cianobacterias potencialmente tóxicas por mL de agua, lo que equivale a unos 10 µg de clorofila por litro de agua.
Efectos en los ecosistemas
A nivel ecológico lo más importante es la disminución de biodiversidad y la falta de oxígeno, aunque en realidad estas son consecuencias directas de la presencia del afloramiento masivo, independientemente si este este es tóxico o no lo es. Sin embargo, la presencia de toxinas puede suponer una variación en las especies dezooplancton, ya que muchas son sensibles a estas toxinas, permaneciendo aquellas que son más resistentes pero con diferente valor nutricional o que simplemente no son consumidas por los peces. Esto hace que la estructura trófica del ecosistema quede desequilibrada.
Además se ha comprobado que hay acumulación de toxinas en los tejidos de los animales que las ingieren. Recientemente se han atribuido mortandades importantes de animales, como en el caso de los flamencos del Parque Nacional de Doñana (Alonso et al., 2002) por el efecto directo de las cianotoxinas contenidas en las cianobacterias.
Cianuro
El cianuro es un anión monovalente de representación CN-. El mismo contiene el grupo cianuro (:C≡N:), que consiste de un átomo decarbono con un enlace triple con un átomo de nitrógeno.
Los compuestos orgánicos que poseen grupo funcional -C≡N adosado a un residuo alquilo son denominados nitrilos según la nomenclaturaIUPAC. Puede formar parte de moléculas de gas como el cianuro de hidrógeno (HCN) y en solución el Ácido cianhídrico, el cloruro de cianógeno (CNCl), o el bromuro de cianógeno (CNBr) o encontrarse en complejos cristalinos tetraédricos como el cianuro de sodio(NaCN) o el cianuro de potasio (KCN). Es utilizado en el ámbito industrial, minero, en la galvanoplastia de electrodeposición de zinc, oro,cobre y especialmente plata y de uso en la producción de plásticos de base acrílica. Es muy tóxico, potencialmente letal.
Características
Se describe con un olor fuerte a castañas o almendras amargas, pero no siempre emana olor y no todas las personas pueden detectarlo, está comprobado que la capacidad de detectarlo está en un gen recesivo asociado al cromosoma X femenino.6[cita requerida] Además el límite de detección del olor es muy cercano a la concentración donde comienza a ser tóxico.[cita requerida]
Toxicidad
Es potencialmente letal, actuando como tóxico a través de la inhibición del complejo citocromo c oxidasa, y por ende bloqueando la cadena transportadora de electrones, sistema central del proceso de respiración celular. Por consecuencia, causa una baja en la producción de ATP intracelular, impidiendo la homeostasis de las células. Afecta también, al estar cargado negativamente, el traspaso de electrones por medio de canales, creando un ambiente positivo dentro de la célula.[cita requerida]Esto genera una gran cantidad de cargas que generan suficiente energía como para que el AMP (Adenosín monofosfato) cíclico se pueda convertir en ADP (Adenosín difosfato), creando una sobreestimulación en varios procesos.[cita requerida]
El principal efecto nocivo y letal de las diversas variedades de cianuro es el impedir que el oxígeno portado por los glóbulos rojos pueda ser utilizado como aceptor de hidrógeno en el final de la cadena respiratoria intramitocondrial. En una autopsia, el cadáver presenta gran cantidad de oxígeno en las venas y una gran cantidad deácido láctico, producto de la respiración anaeróbica realizada por las células carentes de oxígeno.
Las sustancias químicas encontradas en productos hechos a base de acetonitrilo, utilizados para quitar uñas postizas principalmente, pueden liberar cianuro si se ingieren accidentalmente y como consecuencia producir la muerte por paro cardiorrespiratorio.[cita requerida]
El cianuro no es persistente ni asfixiante, ya que en la naturaleza se destruye por acción de la luz solar (por medio del ozono), descomponiéndose por oxidación en gases de tipo COx y NOx. Creando cloratos y nitritos muy utilizados en la purificación del agua contaminada con plomo.
La Agencia de Protección del Medio Ambiente de EE. UU. (EPA) regula los niveles permitidos de cianuro en el agua potable por medio de sales de potasio. El nivel máximo de cianuro permitido en el agua potable es 0.2 partes de cianuro por millón de partes de agua (0.2 ppm). La Administración de Seguridad y Salud Ocupacional de U.E. (EU-OSHA, por sus siglas en inglés) ha establecido un límite para el cianuro de hidrógeno y la mayoría de las sales de cianuro de 10 partes de cianuro por un millón de partes de aire (10 ppm) en el aire del trabajo.
Para la destrucción industrial del cianuro se utilizan cuatro métodos: degradación natural, oxidación química, precipitación y biodegradación. Existen tecnologías de reutilización o reciclado. El uso industrial y minero del cianuro debe ajustarse a normas estrictas, como las que aconseja el Consejo Internacional de Metales y Medio Ambiente, con sede en Ontario, Canadá (2012).
Cianuro en la naturaleza
El cianuro de hidrógeno se formó naturalmente en las primeras etapas del desarrollo de la vida sobre la tierra. Su efectividad a bajas concentraciones es fulminante y mortal. También es conocido por su denominación militar AN (para el cianuro de hidrógeno) y CK (para el cloruro de cianógeno).
Es un producto que se encuentra habitualmente en la naturaleza en diversos microorganismos, insectos y en el estado de crecimiento de muchas plantas como un mecanismo de protección, como un alcaloide común, que los convierte en una fuente alimenticia poco atractiva durante ese periodo, para cierto tipo de animales herbívoros.
El cianuro está presente en forma natural en algunos alimentos como las almendras, las nueces, las castañas1 , la parte interna de las semillas de frutas como losmelocotones, las ciruelas, los albaricoques, entre otros, el cazabe,2 la raíz de yuca y las pepitas de muchas otras frutas como la manzana, las peras o la uva. En ellos se encuentra con el nombre de amigdalina, un compuesto de glucosa, benzaldehído y cianuro, en concentraciones que oscilan entre los 377 y los 2,50 mg por kg, y que bajo la acción de un fermento (emulsina) se descompone, produciendo ácido cianhídrico. También se da la generación antropogénica, como es el caso de los escapes de los automóviles, el humo de los cigarrillos o tabaco y en la sal industrial que se usa para derretir el hielo de los caminos.
El cianuro aparece también en los productos de combustión de materiales sintéticos tales como telas y plásticos.3
Producción industrial
Es un subproducto de la fabricación de fibras acrílicas o bien generado por la combinación de gas natural (previo proceso de remoción del metil mercaptano) conamoníaco líquido. Su fabricación primaria es de 1,4 millones de toneladas y se produce en EE. UU., México, Singapur, China, Inglaterra, España y Alemania. La industria minera y del plástico en general consume el 82% del cianuro producido en el mundo, de dicho porcentaje tan solo un 18% es utilizado en minería y el otro 64% es utilizado en la industria para la fabricación de plásticos y derivados.
Aplicaciones
El cianuro se utiliza industrialmente desde 1889.
- En el sector industrial, el cianuro se utiliza para producir papel, pinturas, textiles y plásticos.
- Está presente en las sustancias químicas que se utilizan para revelar fotografías. Las sales de cianuro son utilizadas en la metalurgia para galvanización, limpieza de metales y la recuperación del oro del resto de material eliminado.
- El gas de cianuro se utiliza para exterminar plagas (ratas, ratones, lauchas, zarigüeyas etc.) e insectos en barcos, edificios y demás lugares que lo necesiten.2
- La minería utiliza para hidrometalurgia el 6% del cianuro utilizado en el mundo, generalmente en solución de baja concentración con agua para extraer yrecuperar metales como el oro y la plata mediante el proceso llamado lixiviación, que sustituyó al antiguo método de extracción por amalgamado de metales preciosos con mercurio. Ver también: Procesos con cianuro en la minería de oro.4 5 6
- La industria farmacéutica también lo utiliza, como en algunos medicamentos para combatir el cáncer como el nitroprusiato de sodio para la hipertensión arterial.
- Se utilizan mínimas dosis de cianuro para la confección de pegamentos sintéticos donde existen compuestos semejantes al acrílico.
- Los productos usados para quitar uñas postizas hechos con base en acetonitrilo pueden crear cianuro si se ingieren.2
- El cianuro es además usado en la química analítica cualitativa para reconocer iones de hierro, cobre y otros elementos.
- El cianuro es usado ampliamente en baños de galvanoplastia como agente acomplejante del cinc, de la plata, del oro, el cobre con el objeto de regular el ingreso de iones al ánodo debido a su valor pKa relativamente bajo.
- El ferrocianuro de potasio (K4[Fe(CN)6]) se utiliza en algunas industrias de la alimentación como la vitivinícola, para la eliminación de los metales pesados que se encuentran en el vino. Estos metales pueden provenir de la propia producción de uva (Pesticidas, derrames, desechos fabriles, etc) así como también de la maquinaria que se utiliza provocando enturbiamientos, ya que el mosto y el vino atacan, percuden, carcomen y disuelven los metales. Un alto contenido de metales se precipita al formar compuestos insolubles con ciertas sustancias como el ferrocianuro de potasio, haciéndolo precipitar abruptamente en forma de sales insolubles cuyo sedimento se retira por tamizado simple. El ferrocianuro desarrolla en el vino una acción química compleja dando como resultado la insolubilización y precipitación de los metales (Zn, Cu, Pb, Fe y Mn). El vino con el plomo forma una sal que no puede ser removida por el ferrocianuro, que endulza a la solución.
- Es indispensable en la cementación de aceros, en la producción de nailon, acrílicos, aplicaciones fotográficas, galvanoplastia y la producción de goma sintética. El Azul de Prusia (ferrocianuro férrico) de características Hematoxinófilas, una de sus formas industriales, fue descubierto por Dipel y Diesbach en 1704.
Aplicaciones militares
El cianuro de hidrógeno fue comercializado por la empresa alemana IG Farben, bajo el nombre de Zyklon B, y se usaba como pesticida en los años veinte. Después, fue utilizado en la Segunda Guerra Mundial como arma química por los nazis, en las cámaras de gas de los campos de exterminio. Con este producto se asesinó a gitanos, homosexuales, judíos, comunistas y otras personas consideradas enemigas.
Según lo indican varios informes, [cita requerida] es posible que el cianuro de hidrógeno gaseoso haya sido utilizado junto con otros agentes químicos contra los habitantes de la ciudad curda de Halabja, al noreste de Irak, durante la Guerra Irán-Irak en la década de 1980. También existen denuncias contra Estados Unidos, que alegan que pudo haber sido utilizado en Vietnam junto con el Agente Naranja.
Determinación de cianuro total por destilación y colorimetría
El método se basa en la destilación ácida a reflujo de la muestra a fin de provocar la volatilización de todas las formas de cianuro presentes en ella, como cianuro de hidrógeno (HCN), para luego condensarlas en una solución alcalina. La concentración de cianuro en esta solución se determina colorimétricamente por espectroscopia UV-VIS, mediante la conversión a CNCl por reacción con cloramina T a pH < 8. Después que la reacción se ha completado, el CNCl forma un compuesto de color rojo-azulado al adicionar ácido barbitúrico y piridina. El compuesto formado presenta una banda de absorción molecular entre 575 y 582 nm. El método colorimétrico es adecuado para concentraciones de cianuro hasta un límite inferior de 20µg/l (20ppb).7 8
Precauciones
Identificación de peligros
- Peligros para las personas: Muy tóxico por inhalación, en contacto con la piel y por ingestión. Causa quemaduras en la piel y ojos.
- Peligros para el medio ambiente: En contacto con ácidos libera cianuro de hidrógeno, gas muy tóxico.
Primeros auxilios
- Inhalación: Si se producen síntomas por inhalación, trasladar a la víctima a un lugar ventilado. Mantener en reposo y abrigado. Aplicar respiración artificial en caso de insuficiencia respiratoria. Requerir asistencia médica. No hacer respiración boca a boca. Si no se produce recuperación administrar cápsulas de nitrito de amilo.
- Contacto con la piel: Quitar las ropas contaminadas. Lavar con agua abundante el área afectada. Requerir asistencia médica en caso de irritación persistente.
- Contacto con los ojos: Lavar con abundante agua durante 15 minutos, manteniendo los párpados abiertos. Acudir inmediatamente al oftalmólogo.
- Ingestión: Tratar al paciente como en el caso de inhalación, provocar vomito y evitar ingerir alimentos.
Medidas de lucha contra incendios
- Medios de extinción adecuados: Polvo químico seco.
- Equipo de protección especial para lucha contra incendios: Utilizar equipo habitual de lucha contra incendios de tipo químico. Llevar equipo de respiración autónoma.





No hay comentarios:
Publicar un comentario