fármacos sistema cardiovascular
Sotalol es el nombre de un medicamento beta bloqueante no selectivo, es decir, bloquea la acción de la epinefrina tanto en receptores adrenérgicos β1 y receptores adrenérgicos β2. Se indica para el tratamiento de trastornos del ritmo cardíaco y de lahipertensión arterial en algunos individuos.
El sotalol es también un bloqueador de los canales de potasio, de modo que cae dentro de la categoría de
agente antiarrítmico clase III. En virtud de su acción dual, el sotalol prolonga tanto el
intervalo PR como el
intervalo QT.
El sotalol (en forma de clorhidrato) es un agente bloquante b-adrenérgico, hidrófilo y no selectivo que se utiliza para el tratamiento de arritmias ventriculares y supraventriculares. El sotalol es activo por vía oral e intravenosa. El sotalol es un beta-bloqueante único que tiene propiedades antiarrítmicas para arritmias de clase II y III de la  clasificación de Vaughn Williams. Como es un b-bloqueante no selectivo de Clase II, el sotalol no tiene actividad simpaticomimética intrínseca o actividad estabilizadora de membrana. Los efectos antiarrítmicos de clase III del sotalol, como la amiodarona, prolongan la duración potencial de acción y aumentan la refractariedad tejido cardíaco. Como resultado, el sotalol se utiliza en el tratamiento de arritmias auriculares o ventriculares potencialmente mortales, incluyendo taquicardia ventricular sostenida. No debe utilizarse para las arritmias leves porque se sabe que es proarrítmico, con un mayor riesgo de torsade de pointes. En estudios comparativos, sotalol ha demostrado ser más eficaz en la prevención de arritmias recurrentes que varios otros medicamentos. De este modo, podría beneficiar a los pacientes en los que otros tratamientos han fallado. No se ha determinado si la tasa de supervivencia se mejora con el uso de sotalol sobre el uso de un desfibrilador implantado solo. clasificación de Vaughn Williams. Como es un b-bloqueante no selectivo de Clase II, el sotalol no tiene actividad simpaticomimética intrínseca o actividad estabilizadora de membrana. Los efectos antiarrítmicos de clase III del sotalol, como la amiodarona, prolongan la duración potencial de acción y aumentan la refractariedad tejido cardíaco. Como resultado, el sotalol se utiliza en el tratamiento de arritmias auriculares o ventriculares potencialmente mortales, incluyendo taquicardia ventricular sostenida. No debe utilizarse para las arritmias leves porque se sabe que es proarrítmico, con un mayor riesgo de torsade de pointes. En estudios comparativos, sotalol ha demostrado ser más eficaz en la prevención de arritmias recurrentes que varios otros medicamentos. De este modo, podría beneficiar a los pacientes en los que otros tratamientos han fallado. No se ha determinado si la tasa de supervivencia se mejora con el uso de sotalol sobre el uso de un desfibrilador implantado solo.
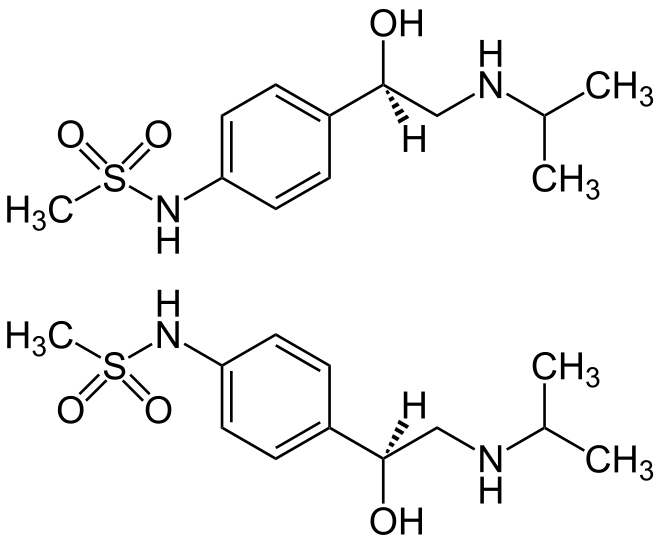
Mecanismo de acción: Sotalol es una mezcla racémica de isómeros. El isómero levógiro tiene toda la actividad beta-bloqueante, y el isómero dextrógiro posee la actividad antiarrítmica de Clase III. Aunque se obtiene un importante bloqueo beta con dosis orales de tan solo 25 mg, los efectos significativos de Clase III se ven sólo con dosis diarias > 160 mg. La actividad beta-bloqueante del fármaco aumenta la longitud del ciclo sinusal, disminuye la conducción AV, y aumenta la refractariedad AV nodal. La actividad antiarrítmica es ejercida por una combinación de actividades de Clase II y de Clase III, que alargan la repolarización o la fase de meseta del potencial de acción. Además, el sotalol prolonga el intervalo QT (un efecto de clase III), actividad que debe ser vigilada cuidadosamente para evitar que predisponga a los pacientes a eventos proarrítmicos En general, los beta-bloqueantes generales sin actividad simpaticomimética intrínseca ejercen efectos perjudiciales sobre la HVI y el perfil lipídico, y causan disfunción sexual.
Farmacocinética: El sotalol se administra por vía oral. La biodisponibilidad es casi del 100%. Los alimentos y leche reducen la velocidad y grado de absorción en aproximadamente un 20%, pero clínicamente, el medicamento puede tomarse con o sin alimentos. El inicio de acción tras la administración oral se presenta en aproximadamente 1 hora con máximos entre 2,5 a 4 horas. Sotalol tiene una baja solubilidad en lípidos y no cruza la barrera hematoencefálica. El sotalol no parece unirse a las proteínas plasmáticas.
No parece haber una correlación entre las concentraciones séricas pico y los efectos máximos sobre la frecuencia cardíaca. El sotalol no se metaboliza y se excreta principalmente por los riñones. Los pacientes con insuficiencia renal requieren reducciones de dosis. La semi-vida plasmática en pacientes con función renal normal es de entre 8-17 horas. Los pacientes con insuficiencia renal tienen una semi-vida de eliminación aumentada proporcional al grado de disfunción renal, semi-vida que puede prolongarse hasta 6 días en pacientes con insuficiencia renal grave. Los pacientes con insuficiencia hepática no muestran ninguna alteración en el aclaramiento de sotalol en comparación con los adultos sanos.
Toxicidad: No se observó ninguna evidencia carcinogénica en ratas durante un estudio de 24 meses con dosis de 137 a 275 mg/kg/día (aproximadamente 30 veces la dosis máxima recomendada oral humana) o en ratones, durante un estudio de 24 meses con dosis de 4141 a 7122 mg/kg/día (aproximadamente 450 a 750 veces la dosis máxima recomendada oral humana).
El sotalol no ha sido evaluada en ninguna de las pruebas específicas de mutagenicidad o clastogenicidad.
El sotalol no produjo ninguna reducción significativa de la fertilidad en ratas con dosis orales de 1,000 mg/kg/día (aproximadamente 100 veces la la dosis máxima recomendada oral humana) antes del apareamiento, a excepción de una pequeña reducción en el número de crías por camada.
Los estudios de reproducción en ratas y conejos durante la organogénesis con dosis 100 y 22 veces la la dosis máxima recomendada oral humana en mg/kg, respectivamente, no revelaron ningún potencial teratogénico asociado con el sotalol. En conejos, una alta dosis de sotalol HCl (160 mg / kg / día) equivalente a 16 veces la la dosis máxima recomendada oral humana, produjo un ligero aumento de las muertes fetales probablemente debido a la toxicidad materna. La dosis ocho veces la dosis máxima (80 mg / kg / día) no dio lugar a una mayor incidencia de muertes fetales.
| |
| | INDICACIONES Y POSOLOGIA
 Para la conversión a y el mantenimiento del ritmo sinusal normal en pacientes con fibrilación o aleteo (flutter) auricular: Para la conversión a y el mantenimiento del ritmo sinusal normal en pacientes con fibrilación o aleteo (flutter) auricular:
NOTA: Los pacientes con fibrilación auricular deben ser anticoagulada de acuerdo con la práctica médica habitual antes de la cardioversión eléctrica o farmacológica. El tratamiento anticoagulante puede continuar después de la cardioversión de acuerdo con las directrices médicas para el tratamiento de los pacientes con fibrilación auricular
Administración oral:
- Adultos: la dosis inicial de sotalol debe individualizarse de acuerdo con el aclaramiento de creatinina y el QTc. Antes de iniciar sotalol, el QTc debe ser determinado. Si la línea de base del QTc excede 450 mseg o CrCl < 40 ml / min, el sotalol está contraindicado para el tratamiento de arritmias auriculares. La dosis inicial en pacientes con función renal normal es de 80 mg por vía oral dos veces al día. Durante la iniciación y titulación, se debe controlar el intervalo QT 2-4 horas después de cada dosis. Si el intervalo QT se prolonga a > 500 ms, la dosis de sotalol debe disminuirse o suspenderse el fármaco. La dosis puede aumentarse hasta 120 mg PO dos veces al día en el caso de reincidencia. La dosis máxima recomendada es de 160 mg por vía oral dos veces al día en pacientes con función renal normal siempre y cuando el intervalo QT no sea excesivamente prolongada. Los pacientes deben ser monitoreados por electrocardiografía continua durante > 3 días después del ajuste de la dosis o durante al menos 5-6 dosis de sotalol si la dosis es una vez al día.
- Niños: Inicialmente, 2-4 mg/kg/día PO en 2-3 dosis divididas. Esta dosis puede ser aumentada por 1-2 mg/kg/día cada 3-4 días hasta un máximo de 8 mg / kg / día PO en 2-3 dosis divididas.
 Para sustituir otros anti-arritmicos por sotalol: Para sustituir otros anti-arritmicos por sotalol:
Administración oral:
- Adultos: las dosis deben ser individualizadas en función del ClCr y del QTc. Antes de iniciar el sotalol, el tratamiento antiarrítmico anterior debe retirarse bajo supervisión cuidadosa por un mínimo de (2-3) semividas plasmáticas del fármaco discontinuado. El tratamiento con sotalol se ha iniciado en los pacientes bajo lidocaína intravenosa sin efecto perjudicial. Debido a la farmacocinética impredecible con la amiodarona, el sotalol, no debe iniciarse tras la interrupción del tratamiento con amiodarona hasta que el intervalo QTc se haya normalizado.
 Terapia de mantenimiento con sotalol: Terapia de mantenimiento con sotalol:
- Adultos: las dosis deben ser individualizadas en función del ClCr y del QTc. Tras el alta hospitalaria, continuar con la dosis utilizada tras el ajuste de la dosis inicial. La función renal y QTc deben ser reevaluados regularmente o cuando estén médicamente justificadas. Si el QTc > 520 ms en cualquier momento, la dosis sotalol debe reducirse y el paciente deben ser monitorizada cuidadosamente hasta que el QTc vuelve a los niveles de referencia. Si el paciente está recibiendo 80 mg PO una vez o dos veces al día y el QTc es > 520 ms, el sotalol debe interrumpirse. Si la función renal se deteriora, ajustar la dosis tal y como se describe en las directrices de dosis para pacientes con insuficiencia renal. El sotalol fue comparable a la quinidina en el mantenimiento del ritmo sinusal después de 6 meses de tratamiento siguientes a la cardioversión en 183 pacientes.
 Para el tratamiento de las arritmias ventriculares, como la taquicardia ventricular sostenida que se consideran un peligro la vida: Para el tratamiento de las arritmias ventriculares, como la taquicardia ventricular sostenida que se consideran un peligro la vida:
NOTA: Las dosis iniciales de sotalol deben individualizarse de acuerdo con el aclaramiento de creatinina y el QTc. Antes de iniciar el tratamientop con sotalol, el QTc debe ser determinado. El Sotalol está contraindicado si está presente una prolongación del intervalo QT al inicio del estudio.
 Para el mantenimiento del ritmo sinusal en pacientes con taquicardia supraventricular paroxística refractaria, incluidos los pacientes con síndrome de Wolff-Parkinson-White (WPW) Para el mantenimiento del ritmo sinusal en pacientes con taquicardia supraventricular paroxística refractaria, incluidos los pacientes con síndrome de Wolff-Parkinson-White (WPW)
Administración oral:
- Niños: Inicialmente, 2-4 mg/kg/día PO en 2-3 dosis divididas. Esta dosis puede ser aumentada por 1-2 mg/kg/día cada 3-4 días hasta un máximo de 8 mg/kg/día PO en 2-3 dosis divididas.
Límites máximos de dosis:
• Adultos: 320 mg PO / día para la fibrilación auricular / flutter auricular. Hasta 480 a 640 mg / día PO en las arritmias ventriculares potencialmente mortales
• Ancianos: 320 mg PO / día para la fibrilación auricular / flutter auricular. Hasta 480 a 640 mg / día PO en las arritmias ventriculares potencialmente mortales.
• Adolescentes: El uso seguro y eficaz no se ha establecido.
• Niños: se ha sugerido como ldosis máxima, 8 mg/ kg / día PO pero el uso seguro y eficaz no se ha establecido definitivamente
Pacientes con insuficiencia hepática: No es necesario ajustar la dosis en insuficiencia hepática; sotalol no se metaboliza y se elimina inalterada por vía renal
Pacientes con insuficiencia renal: CrCl > 60 ml/min: ajustar la dosis necesaria, administrando la dosis adecuada cada 8-12 horas de acuerdo con la indicación (ventricular vs. arritmia auricular) y la respuesta clínica. La dosis inicial recomendada es de 80 mg por vía oral dos veces al día para ambas indicaciones.
ClCr 40-60 ml / min: extender el intervalo de dosificación para cada 24 horas. La dosis inicial recomendada es de 80 mg por vía oral una vez cada 24 horas.
ClCr < 40 ml / min: está contraindicado el uso del sotalol para el tratamiento de arritmias auriculares. En caso de arritmias ventriculares, si CrCL es < 30 ml / min se utiliza un intervalo de dosis de sotalol de 36-48 horas según la respuesta clínica.
Los pacientes con aclaramiento de creatinina <10 deben="" dosis="" font="" individualizadas.="" las="" min="" ml="" recibir="">
Hemodiálisis intermitente: Ver los ajustes de dosis para pacientes con aclaramiento de creatinina < 40 ml / min. Debe tenerse extrema precaución en pacientes en hemodiálisis, debido a que la semi-vida media del sotalol se prolonga hasta 69 horas en pacientes con anuria. Debido a que el sotalol se elimina parcialmente mediante hemodiálisis, la recuperación parcial posterior de las concentraciones de sotalol se deberá llevar a cabo una vez que se haya completado la sesión de diálisis. Tanto la frecuencia cardíaca y el intervalo QT, así como la eficacia (control de la arritmia) deben ser controlados cuidadosamente.
| |
| | CONTRAINDICACIONES Y PRECAUCIONES
La interrupción brusca de sotalol puede precipitar arritmias y, posiblemente, un infarto de miocardio. Si el fármaco debe interrumpirse abruptamente, debe ser considerado el uso temporal de un betabloqueante alternativo. Los pacientes deben ser advertidos de que no pueden interrumpir el tratamiento con sotalol abruptamente. Se recomienda reducir la dosis gradualmente durante 1 o 2 semanas.
Los beta-bloqueantes deben utilizarse con precaución en pacientes con hipertiroidismo o tirotoxicosis ya que pueden enmascarar la taquicardia, que es un parámetro de seguimiento útil en la enfermedad de la tiroides. La retirada brusca de los beta-bloqueantes en pacientes con hipertiroidismo puede precipitar una tormenta tiroidea. Sin embargo, los beta-bloqueantes son, en general, útiles en el tratamiento de estados relacionados con hipertiroidismo.
El sotalol está contraindicado en pacientes con bradicardia sinusal, síndrome del seno enfermo o bloqueo AV de segundo o tercer grado (a menos que un marcapasos que funcione estepresente) síndrome de prolongación del QT, hipopotasemia, shock cardiogénico o insuficiencia cardiaca no controlada. En general, los beta-bloqueantes no deben utilizarse en pacientes con shock cardiogénico o insuficiencia cardíaca congestiva sistólica, particularmente en aquellos con disfunción ventricular izquierda severamente comprometida, ya que el efecto inotrópico negativo de estos fármacos puede reducir aún más el gasto cardíaco.
El sotalol no debe utilizarse en pacientes con prolongación del intervalo QT o hipopotasemia, ya que podría precipitar torsade de pointes. A pesar de que el sotalol es un beta-bloqueante, también es proarrítmico y puede inducir arritmias ventriculares o empeorar las arritmias ventriculares preexistentes.
Al igual que la amiodarona, otra antiarrítmico de clase III, el sotalol se ha asociado con la prolongación del intervalo QT, que puede conducir a la fibrilación ventricular sostenida, taquicardia ventricular sostenida, y / o torsade de pointes. Aunque a veces es difícil distinguir entre arritmia maligna subyacente de un paciente y una arritmia inducida por fármacos, los pacientes con un intervalo QT inicialmente normal, que posteriormente sufren un evento proarrítmico generalmente lo hacen como resultado de tratamiento antiarrítmico.
El uso de fármacos antiarrítmicos se ha asociado con muerte súbita, y los pacientes están continuamente en riesgo, y no sólo durante el inicio de la terapia como alguna vez se creyó. Los factores de riesgo de arritmias inducidas por el sotalol incluyen enfermedad renal, desequilibrio electrolítico (por ejemplo, hipopotasemia, hipomagnesemia), y el uso concomitante de otros medicamentos que prolongan el intervalo QT. Las mujeres y los hombres con antecedentes de arritmias ventriculares o taquicardia ventricular pueden también tener una mayor incidencia de eventos proarrítmicos (por ejemplo, torsade de pointes). El sotalol está relativamente contraindicado en la insuficiencia renal debido a una disminución del aclaramiento del fármaco, ya que se elimina principalmente a través de los procesos renales.
El uso de sotalol está absolutamente contraindicado para el tratamiento de arritmias auriculares cuando el CrCl es < 40 ml / min. Al utilizar el sotalol para el tratamiento de las arritmias ventriculares, se recomienda ajustar la dosis cuando el aclaramiento de creatinina es < 60 ml / min. De deben tomar extremas precauciones en pacientes en hemodiálisis, debido a que la semi-vida del sotalol se prolonga hasta 69 horas en pacientes con anuria. Como el sotalol se elimina parcialmente durante la hemodiálisis, se debe proceder a la recuperación posterior de las concentraciones adecuadas delñ fármaco una vez que se haya completado la sesión de diálisis.
Tanto la frecuencia cardíaca y el intervalo QT, así como la eficacia (control de la arritmia) deben ser controlados cuidadosamente.
La monoterapia con beta-bloqueantes se debe utilizar con precaución en pacientes con feocromocitoma o angina vasoespástica (angina de Prinzmetal), debido al riesgo de hipertensión secundaria a la estimulación del alfa-receptor sin oposición.
En el tratamiento del infarto de miocardio, los beta-bloqueantes están contraindicados en pacientes con hipotensión (PAS < 100 mmHg).
El manejo de los pacientes sometidos a cirugía mayor que están siendo tratados con bloqueadores beta es controvertido. Se han descrito hipotensión grave prolongada y dificultad en la restauración y el mantenimiento del ritmo cardíaco normal después de la anestesia se han reportado en pacientes que reciben beta-bloqueantes.
El sotalol está contraindicado en pacientes con una enfermedad pulmonar como el asma bronquial, enfermedad alérgica broncoespástica (por ejemplo, la EPOC, enfisema, bronquitis), o durante el broncoespasmo agudo porque puede inhibir la broncodilatación
Sotalol se debe utilizar con precaución en pacientes con diabetes mellitus, ya que puede enmascarar signos de hipoglucemia, como la taquicardia, palpitaciones, temblor, y los sentimientos de ansiedad (pero no diaforesis). Sotalol también puede prolongar o mejorar la hipoglucemia al interferir con la glucogenolisis. |
Vernakalant (INN/DCI; con código
RSD1235, comercializado bajo los nombres de
Kynapid y
Brinavess) es un fármaco antiarrítimico para la conversión aguda de episodios de
fibrilación auricular. Fue inicialmente desarrollado por el laboratorio Cardiome Pharma, y su formulación
intravenosa fue llevada a cabo por
Merck en abril de 2009.
1
Esta aprobado como indicación para episodios de fibrilación auricular de reciente comienzo. No posee indicación en flutter auricular.
2
En septiembre de 2012, Merck rescindió sus acuerdos con Cardiome y consecuentemente ha regresado todos los derechos del fármaco atrás a Cardiome. El 11 de diciembre de 2007, el comite de fármacos cardiovasculares y renales de la
FDA (Administración de medicamentos y alimentos de los EEUU) votó a favor la aprobación de vernakalant, sin embargo en agosto de 2008 la FDA juzgó que mas información adicional era necesaria para su aprobación.
1 El fármaco (bajo nombre de marca Brinavess) estuvo aprobado en Europa el 1 de septiembre de 2010.
Su forma oral esta actualmente en ensayos clínicos fase III. La fase II se desarrolló entre 2005 y 2008.
Mecanismo de acción
Es un fármaco auriculo selectivo. Como otros
antiaarítmicos clase III, vernakalant bloquea canales de potasio auriculares, prolongando así la repolarizacion. Vernakalant difiere de los agentes clase III por hacer un bloqueo específico de un tipo de canal de potasio, cuyo paso de iones potasio se activa cuando existen frecuencias cardiacas altas. Esto significa que este fármaco es más eficaz en ritmos cardíacos altos, mientras que otros agentes clase III tienden a perder efectividad en estas circunstancias. Ligeramente bloquea además el canal de potasio subtipo hERG, con tendencia a prolongar el
intervalo QT. Esto teóricamente puede aumentar el riesgo de
taquicardia ventricular, aunque esto no parece para ser clínicamente significativo.
3
Es principalmente utilizado para conversión rápida de fibrilaciones auriculares de reciente comienzo (de duración de 3 a 72 horas).
Metabolismo
Vernakalant es metabolizado por las vías renal y hepática. Mayoritariamente a través del
citocromo CYP2D6 y excretado conjugandose con ácido glucuronido. Posee una vida media de 3-4 horas.
La interacción medicamentosa es un dato a tener en cuenta. La toma de fármacos que inhiban colateralmente este citocromo puede afectar a la farmacocinética de vernakalant acumulandose, como son
amiodarona,
fluoxetina,
duloxetina y
haloperidol. Por lo contrario, con inductores de dicho citocromo como la
rifampicina, se eliminaría con mayor rapidez.
Uso en fibrilación auricular
La fibrilación auricular es posible revertirla mediante dos tipos de estrategias: el control de ritmo (reversión a ritmo sinusal) y el control de frecuencia (descender la frecuencia cardiaca). Preferentemente en aquellos pacientes de edad inferior a 65 años o con baja carga de comorbilidades asociadas se opta por el control del ritmo; mientras que en caso contrario se prefiere el control de frecuencia
Dentro de la cardioversión farmacológica, la sociedad europea de cardiología en su última guía del 2012 sobre el manejo de la fibrilación auricular
4 indica tres grupos de posibilidades farmacológicas según la enfermedad cardíaca estructural:
-
Ausente: Las posibilidades terapeuticas son
flecainida, ibutilide, proprafenona o vernakalant o estrategia de "pastilla en bolsillo/ pill in the pocket" con flecainida o propafenona.
- Moderada (presencia de hipertensión arterial, cardiopatia hipertensiva o isquémica): El vernakalant es la opción terapéutica de referencia en este caso.
-
Severa (presencia de insuficiencia cardiaca, valvulopatía, miocardiopatía hipertrófica obstructiva o restricitiva, pericarditis constrictiva, o intervalo QRS >140 milisegundos): La
amiodarona es la opción terapéutica de referencia en este caso.
En caso de fallo de la cardioversión farmacológica, se pasa a la cardioversión eléctrica como método de elección o incluso sería posible el control de frecuencia mediante fármacos cronotrópicos negaticos como los betabloqueantes.
Vernakalant ha demostrado que revierte a ritmo sinusal en un tiempo medio de 8-10 minutos, en comparación con flecainida (tiempo medio entre 150-200 minutos) y amiodarona (700-800 minutos). Su eficacia aumenta cuanto menor sea el tiempo de duración de la firbilación auricular debido a la remodelación que va sufirendo el tejido auricular durante el episodio. Su uso puede reducir el tiempo medio de hospitalización de los pacientes en los servicios de urgencias, y con ello tomar decisiones con mayor rapidez incluso en caso de que el vernakalant sea ineficaz.
Este fármaco no suele estar disponible en la mayoría de los hospitales debido a su gran coste económico unitario, en contra posición a la amiodarona, la flecainida y la propafenona con un coste muy inferior. El uso de vernakalant a falta de estudios coste beneficio podría implicar un ahorro en el manejo de la fibrilación auricular a través de reducción de costes indirectos al disminuir enormemente la estancia del paciente en los servicios de urgencias.
Modo de empleo
Se administra en aquellos pacientes que presenten indicación, una dosis inicial en infusión de 3mg/kg en 10 minutos. Tras ello, 15 minutos de observación. En caso de no reversión a ritmo sinusal, se administraría una segunda dosis de 2mg/kg en infusión durante 10 minutos. Ante cualquier efecto adverso de gravedad, la infusión debe ser suspendida.
En toda la terapia, el paciente debe estar bajo monitoraje
holter continuo y electrocardiograma de 12 derivaciónes cada 5 minutos.
Efectos secundarios
Se han descrito reacciones adversas como la disgeusia, estornudos, parestesias, hipotensión, bradicardia y
flutter auricular. El aumento del intervalo QT así como otros efectos sobre la capacidad ventricular son menos probables debido a la aurículo selectividad de este fármaco.
El vernakalant es un fármaco antiarrítmico que actúa preferentemente en las aurículas para prolongar la refractariedad auricular y para retrasar la conducción de los impulsos de forma dependiente de la frecuencia. Se utiliza para tratar fibrilaciones auriculares de reciente aparición.
Mecanismo de acción: el vernakalant actúa preferentemente en las aurículas bloqueando las corrientes de potasio y de sodio y, en consecuencia, los potenciales de acción, alargando los períodos refractarios auriculares. La selectividad relativa del vernakalant sobre la refractariedad auricular frente a la ventricular se debe al bloqueo de las corrientes que están expresadas en las aurículas, pero no en los ventrículos, así como a las características electrofisiológicas únicas de la aurícula en fibrilación. En comparación con la amiodarona, el vernakalant revierte la fibrilación auricular a ritmo sinusal en muchos paciente en unos 12 minutos y siendo del 51.% los pacientes convertidos a los 90 minutos, frente al 5.1% para la amiodarona.
Farmacocinética: después de una perfusión única de 10 minutos de 3 mg/kg de vernakalant (en forma de clorhidrato) las concentraciones plasmáticas máximas fueron de 3,9 mg/ml y de 4,3 mg/ml después de una segunda perfusión de 2 mg/kg practicada a los 15 minutos de la primera.
El vernakalant se distribuye amplia- y rapidamente por el cuerpo, con un volumen de distribución de aproximadamente 2 L/kg. La farmacocinética del vernakalant es lineal en el rango usual de dosis (0,5 mg/kg a 5 mg/kg). El aclaramiento corporal total medio de vernakalant es de 0,41 Ll/h/kg. La fraccion libre de vernakalant en el suero humano es de 53-63 % en un intervalo de concentracion de 1-5 mg/ml.
El vernakalant se metaboliza por O-desmetilación a través de la isoenzima CYP2D6, seguida de glucuronidación. La excreción es renal. La semi-vida de eliminación es de unas 3 horas en los metabolizadores rápidos y de 5.5 horas en los metabolizadores lentos.
En los pacientes con insuficiencia hepática, la exposición a vernakalant aumenta entre el 9 y 25%. Sin embargo, no es necesario un reajuste de las dosis.
Toxicidad: no se han observado efectos sobre el embarazo, el desarrollo embriofetal, el parto o el desarrollo postnatal, después de la administración intravenosa de vernakalant, a niveles de exposición (AUC) similares o inferiores a los niveles de exposición humana.
En los estudios de desarrollo embriofetal, la administración oral de vernakalant dos veces al día originó niveles de exposición (AUC) por lo general superiores a los alcanzados en humanos con la dosis intravenosa única de vernakalant. Se produjeron malformaciones (huesos del cráneo deformes/ausentes/fundidos, incluyendo paladar hendido, radio torcido, escápula torcida/escápula deforme, tráquea estenosada, ausencia de tiroides, criptorquidia) en ratas y, en conejos con las dosis más altas estudiadas, se observó un aumento de la letalidad embriofetal, aumento del número de fetos con esternebra fusionada y/o adicional.
| |
| |
INDICACIONES Y POSOLOGÍA
 Conversión rápida a ritmo sinusal de la fibrilacion auricular de inicio reciente en adultos Conversión rápida a ritmo sinusal de la fibrilacion auricular de inicio reciente en adultos
Administración intravenosa
- Adultos: las dosis de vernakalant se deben individualizar según el peso del paciente. La dosis inicial recomendada es de 3 mg/kg administrados por perfusión intravenosa en 10 minutos. La dosis máxima, incluso en pacientes de más de 113 kg no debe ser superior a 339 mg. Si no se produce la conversión de la fibrilación auricular en un plazo de 15 minutos desde el final de perfusión, se debe administrar una segunda perfusión con dosis de 2 mg/kg en 10 minutos. En esta segunda perfusión no se deben superar los 226 mg incluso en los pacientes de peso > 113 kg.
No hay datos sobre dosis de más 5 mg/kg (perfusiones 1 y 2) en menos de 24 horas.
El vernakalant se debe administrar mediante perfusion intravenosa, preferentemente mediante una bomba de perfusión, en un departamento clínico adecuado para la cardioversión. Unicamente un profesional sanitario bien cualificado debe administrar el vernakalant, vigilando frecuentemente al paciente mientras dure la perfusión y al menos durante 15 minutos después de finalizar la misma por si aparecieran signos y síntomas de una disminución súbita de la presión arterial o de la frecuencia cardíaca.
- Pacientes despues de cirugía cardíaca: no es necesario ajuste de la dosis.
- Insuficiencia renal: no es necesario ajuste de la dosis
- Insuficiencia hepática: no es necesario ajuste de la dosis
- Pacientes de edad avanzada : no es necesario ajuste de la dosis.
- Población pediátrica: la eficacia y seguridad del vernakalant no han sido evaluadas.
| |
| |
CONTRAINDICACIONES y PRECAUCIONES
El vernakalant está contraindicado en pacientes con hipersensibilidad al principio activo o a cualquiera de los componentes de su formulación.
También está contraindicado el vernakalant en pacientes con estenosis aórtica grave, pacientes con presión arterial sistólica < 100 mm Hg, pacientes con insuficiencia cardiaca de clase NYHA III y IV o con intervalo QT prolongado en la situación inicial (> 440 ms no corregido), bradicardia grave, disfunción del nodo sinusal o bloqueo aurículo-ventricular de segundo y tercer grado en ausencia de marcapasos.
Igualmente, el vernakalant está contraindicado en pacientes que hayan mostrado un síndrome coronario agudo (incluido infarto de miocardio) dentro de los ultimos 30 dias.
Antes de iniciar el tratamiento con vernakalant, los pacientes deben estar adecuadamente hidratados y hemodinámicamente optimizados y en los pacientes con hipopotasemia los niveles de potasio deben ser normalizados.
No se debe administrar el vernakalant si en las cuatro horas anteriores se han uilizado antiarritmicos intravenosos para el control del ritmo (clase I y clase III) ni estos últimos debe usarse en las cuatro horas siguientes a la administración de vernakalant.
Se han comunicado casos de hipotensión grave durante e inmediatamente después de la perfusión de vernakalant. Se debe observar atentamente a los pacientes durante la duración completa de la perfusion y al menos durante 15 minutos despues de finalizar esta, con evaluación de las constantes vitales y monitorizacion continua del electrocardiograma, discontinuando el fármaco y/o instaurando el tratamiento médico adecuado en los siguientes casos:
- Una caída súbita de la presión arterial o de la frecuencia cardíaca, con o sin hipotensión o bradicardia sintomáticas.
-Cambios en el ECG (como pausa sinusal clinicamente significativa, bloqueo auriculoventricular completo, nuevo bloqueo de rama, prolongación significativa del QRS o del intervalo QT, cambios compatibles con isquemia o infarto y arrítmia ventricular)
El paciente debe ser vigilado durante 2 horas después de empezar la perfusión hasta que los parámetros clínicos y el ECG se hayan estabilizado. En los pacientes que no responden al tratamiento puede intentarse la cardioversión con corriente continua.
Los pacientes con insuficiencia cardíiaca congestiva mostraron una mayor incidencia global de acontecimientos de hipotensión durante las 2 primeras horas despues de la administración en comparacion con los pacientes que recibieron placebo (16,1% frente a 4,7%, respectivamente). En el 2,9% de los pacientes tratados con vernakalant se tuvo que discontinuar el tratamiento debido a una grave hipotensión.
Igualmente, los pacientes con antecedentes de insuficiencia cardíaca congestiva mostraron una mayor incidencia de arritmia ventricular en las dos primeras horas despues de la dosis (7,3% con vernakalant en comparacion con el 1,6% con placebo). Estas arritmias se presentaron tipicamente como taquicardias ventriculares asintomaticas, monomórficas, no mantenidas (promedio de 3-4 latidos).
El vernakalant debe usarse con precaución en pacientes hemodinámicamente estables con insuficiencia cardíaca congestiva de clases funcionales I a II de la NYHA. Esta contraindicado su uso en pacientes con insuficiencia cardíaca congestiva correspondiente a NYHA III o IV.
El vernakalant no es eficaz para convertir el flutter auricular primario típico a ritmo sinusal. Además, los
pacientes tratados con vernakalant tienen una mayor incidencia de conversión de la fibrilación a flutter auricular durante las 2 primeras horas despues de la dosis. Si se observa flutter auricular secundario al tratamiento, debe valorarse la continuacióon del tratamiento.
El vernakalant se debe utilizar con precaucion en pacientes en tratados con antiarritmicos orales (clase I y III). El flutter auricular puede aumentar en estos pacientes.
|

No hay comentarios:
Publicar un comentario