FLUIDEZ y HETEROGENEIDAD
Semipermeabilidad.
Las moléculas cargadas tienen dificultades para cruzar las membranas. Permite crear ambientes moleculares diferentes separados por ella. Permite la creación y utilización de gradientes. Fluidez. Las moléculas de la membrana pueden moverse lateralmente. La fluidez afecta a la funcionalidad de la membrana y de sus moléculas. La movilidad lateral de las moléculas puede restringirse por interacciones con moléculas externas o con otras moléculas de la propia membrana.
La composición química de las membranas hace que posean unas propiedades esenciales para las funciones que desempeñan en la célula. Podemos agrupar dichas propiedades en cinco: semipermeabilidad, asimetría, fluidez, reparación y renovación.
Semipermeabilidad
Esta propiedad es consecuencia del ambiente hidrófobo interno de la membrana creado por las cadenas de ácidos grasos de los lípidos, difícil de cruzar por las moléculas con carga eléctrica neta. Esto permite a las membranas crear compartimentos intracelulares o mantener separados el medio intracelular del extracelular y, por tanto, impedir la libre difusión de diversos tipos de moléculas a su través. Sin embargo, la permeabilidad es selectiva. Las variables que más influyen en la difusión pasiva son la polaridad y el tamaño de la molécula. Así, moléculas pequeñas sin carga, por ejemplo el CO2, N2, O2, o moléculas con alta solubilidad en grasas como el etanol cruzan las membranas prácticamente sin oposición, por un proceso de difusión pasiva. La permeabilidad de la membrana es menor para aquellas moléculas con cargas pero globalmente neutras (el número de cargas negativas iguala al de cargas positivas) como el agua o el glicerol. Se podría pensar que el agua difunde libremente por las membranas pero no es así y por ello en determinadas membranas existen unas moléculas denominadas acuaporinas que facilitan el cruce de la membrana por parte del agua. Es menor aún la capacidad de atravesar la membrana para moléculas grandes neutras pero con cargas, como la glucosa. Sin embargo, es altamente impermeable a los iones y a las moléculas que también carga neta. Algunos valores del coeficiente de permeabilidad a través de membranas por difusión pasiva son: O2: 2.3 cm/s, CO2: 0,35 cm/s, H2O: 0,0034 cm/s, glicerol: 10 -6 cm/s, sodio y potasio: 10 -14 cm/s

El cruce de la membrana por parte de las moléculas depende de su tamaño y de sus características eléctricas (Modificado de Alberts et al., 2002).
La desigual distribución de iones y moléculas entre ambos lados de la membrana es la base para la creación de los gradientes químicos y eléctricos. La medida de esa diferencia de concentración de cargas es lo que se llama potencial de membrana, que se usa para muchas funciones celulares, como por ejemplo la síntesis de ATP o la transmisión del impulso nervioso. La semipermeabilidad de la membrana también permite el fenómeno de la ósmosis, es decir, el flujo de agua hacia donde más concentración de solutos haya. Las células vegetales deben su crecimiento a este proceso. Como veremos más adelante, las moléculas que no cruzan las membranas libremente son interesantes para las células puesto que la variación de sus concentraciones a un lado u otro de la membrana puede actuar como señales o como herramientas. Por ello se han inventado proteínas integrales de membrana que permiten selectivamente el paso de estas sustancias de un lado al otro. Por ejemplo, la contracción muscular se debe a una rotura de ese gradiente eléctrico.
Fluidez y heterogeneidad

Movimientos que pueden sufrir los lípidos en las membranas gracias a su fluidez. Los movimientos flip-flop son muy raros para los lípidos y no se han documentado para las proteínas.
Es la capacidad de una molécula que forma parte de una membrana para desplazarse por ella. Las membranas son fluidas, prácticamente son láminas de grasa, donde las moléculas se encuentran en un estado de líquido viscoso. Esto implica que, en teoría, las moléculas podrían difundir y desplazarse por ella sin restricciones. Consideremos un glicerofosfolípido que está situado en la membrana plasmática en su monocapa externa. Tendría dos posibilidades de movimiento: uno lateral donde se desplazaría entre las moléculas contiguas, y otro en el que saltaría a la monocapa interna, movimiento denominado "flip-flop". Los dos tipos de movimientos se han demostrado experimentalmente en membranas artificiales pero el primero es mucho más frecuente que el segundo. Una molécula lipídica puede recorrer 30 micras en unos 20 segundos por difusión pasiva lateral, es decir, podría dar la vuelta a una célula de tamaño medio en aproximadamente un minuto. Sin embargo, los saltos entre monocapas son muy infrecuentes y se estima que la posibilidad de que le ocurra a un lípido es de una vez al mes debido a que las cabezas polares de los lípidos se encuentran con la barrera de las cadenas de ácidos grasos. El colesterol posee, sin embargo, la capacidad de hacer movimientos "flip-flop" con relativa facilidad.
La fluidez de la membrana puede variar con la composición química de sus componentes. Así, generalmente, la menor longitud o la mayor cantidad de enlaces insaturados de las cadenas de ácidos grasos hacen que las membranas sean más fluidas. El colesterol también influye en la fluidez de la membrana, pero su efecto depende de las condiciones de temperatura y composición lipídica de la membrana. En general se puede decir que mayor concentración de colesterol disminuye la fluidez de la membrana plasmática (aunque a bajas temperaturas favorece la fluidez). Por tanto, las células pueden alterar la fluidez de sus membranas modificando la composición química de éstas. Por ejemplo, algunas bacterias son capaces de aumentar la concentración de ácidos grasos insaturados (dobles enlaces) a temperaturas bajas, mientras que cuando suben los cambian por ácidos grasos saturados. La bajada de la temperatura disminuye la fluidez de la membrana.
Debido a la fluidez de la membrana podría pensarse que las moléculas están distribuidas al azar y que por tanto la membrana sería homogénea en cuando a composición molecular en cualquier lugar de su superficie. Esto no es así y hay diversas restricciones a las movilidad lateral de las moléculas que hacen que la membrana tenga dominios con composiciones moleculares diferentes. Las resticciones pueden se causadas por diferentes mecanismos como interacción con moléculas del citoesqueleto o la matrix extracelular, interacciones moleculares entre las propias moléculas de la membrana, densidad (menor fluidez local), concentraciónn de cargas eléctricas, grado de curvatura de la membrana o espesor de la misma.
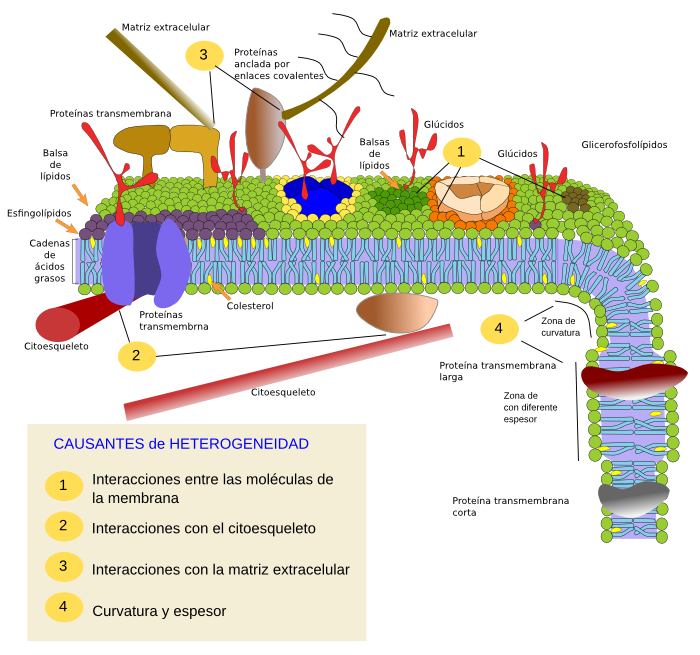
Modelo de membrana actualizado con las posibles causas que generan dominios de membrana.
Una restricción al movimiento de las moléculas en las membranas de las células se debe alas interacciones y asociaciones moleculares entre las propias moléculas de las membranas. Esto afecta tanto a proteínas como a los lípidos y crea dominios, distribución heterogénea de moléculas en las membranas.

Las interacciones entre lípidos, sobre todo esfingolípidos y colesterol, pueden crear zonas de mayor densidad lípidica. También la interacción entre proteínas y ciertos lípidos pueden crear zonas o conchas de lípidos característicos alrededor de las proteínas.
Los esfingolípidos y el colesterol se pueden asociar entre sí espontáneamente haciendo que su movilidad disminuya y por tanto se conviertan en una región membranosa más densa que el resto, como si de una balsa en un mar se tratara. Se cree que estas asociaciones, denominadas balsas de lípidos ("lipid rafts"), son muy abundantes y dinámicas y hacen que las membranas celulares sean en realidad un mosaico de dominios más densos que viajan entre los glicerofosfolípidos, más fluidos. Hay experimentos que apoyan la idea de que ciertas proteínas tendrían mayor apetencia por estas balsas y por tanto viajarían en el interior de ellas. Este confinamiento de proteínas en dominios celulares es importante puesto que permitiría agrupar o segregar conjuntos de proteínas que favorecerían o no el inicio de cascadas de señalización intracelulares. Además, se postula que la alta concentración de ciertos tipos de lípidos en dichas balsascrea un ambiente químico propicio para determinadas reacciones químicas o interacciones moleculares. Por ejemplo, se cree que la infección de los linfocitos por parte del virus del SIDA necesita la existencia de dichas balsas de lípidos. En cualquier caso tales dominios de esfingolípidos y colesterol sólo se han postulado para la monocapa externa de la membrana plasmática, aunque también se propone su existencia en las membranas de los orgánulos celulares donde algunas funciones del propio orgánulo estarían segregadas en distintos dominios de sus membranas.
Las proteínas integrales o asociadas a la membrana también pueden interaccionar entre sí y pueden ensamblarse en estructuras macromoleculares que pueden favorecer la transmisión de señales, reconocimiento celular, activación enzimática, movimiento celular, etc. También hay proteínas multiméricas que sólo son activas cuando tienen todas sus subunidades asociadas entre sí. Por ejemplo, el receptor de la insulina está compuesto por cuatro subunidades. Por supuesto, también hay interacciones entre lípidos y proteínas que crean dominios de membrana.

Los movimientos de las moléculas pueden estar restringidos por las interacciones directas con la matriz extracelular, con el citoesqueleto, aunque también se pueden limitar los movimientos por la inclusión en las balsas de lípidos o por la disposición del citoesqueleto (imagen de la derecha).
Las proteínas integrales de membrana también tienen la posibilidad de una libre difusión lateral. Pero se ha comprobado quelas proteínas tienen numerosas restricciones a la movilidad, principalmente por culpa de las interacciones de sus dominios intra y extracelulares con moléculas del citoesqueleto y de la matriz extracelular, respectivamente. Estas interacciones anclan por tiempos más o menos prolongados las proteínas de membrana a lugares concretos de la superficie celular. Las células tienen otros mecanismos para confinar proteínas a determinados dominios celulares. Por ejemplo, en las células epiteliales del digestivo ciertos transportadores y enzimas están localizados sólo en la zona apical y otros en la basal gracias al cierre a modo de cinturón que realizan las uniones estrechas, como vimos en el capítulo dedicado a la matriz extracelular. Tal asimetría es esencial para el funcionamiento de la célula epitelial.
Curvar una membrana es otra manera de crear dominios, y esta curvatura puede ser el proceso inicial de la formación de una vesícula, la extensión de una expansión celular, el cambio o crecimiento de un orgánulo, o simplemente un pliegue que actúa como barrera a las difusión lateral de moléculas.
La maquinaria necesaria para curvar una membrana requiere a su vez un dominio de membrana para llevarlo a cabo. Determinadas composiciones lipídicas o zonas con diferente carga eléctrica son sitios de atracción para la maquinaria. Los fosfoinosítidos son lípidos que participan en este reclutamiento, particularmente PIP2 y PIP3. Son apropiados para esto puesto que su cabeza puede cambiar en carga y estructura mediante modificaciones químicas locales. Estos lípidos son a su vez mantenidos en el sitio por afinidad con las proteías reclutadas. La creación inicial de un dominio para curvar una membrana ocurre también con la fostatidil serina, la cual, cuando cambia de hemicapa por acción de las flipasas, es capaz de ayudar a generar curvatura, y es retenida por proteínas como la caveolina. Los filamentos de actina pueden también controlar la difusión de lípidos, además de proteínas, creando barreras a modo de vallas en superficie citosólica de la membrana, creando así dominios de lípidos sin la intervención del colesterol o los esfingolípidos.
Los microdominios de lípidos atraen a las proteínas que realmente curvan a las membranas de manera efectiva. Hay proteínas especializadas en crear curvatura de membranas. El domimio proteico BAR (Bin/amphyphysin/Rsv161) es uno de ellos. Lo hace de dos maneras: mediante la creación de un andamiaje curvado sobre el que descansa la membrana o mediante inserciones de secuencias de aminoácidos en la membrana a modo de cuñas. Otros ejemplos son las caveolinas que también generan curvatura para formar caveolas, las tetraspaninas que generan túbulos en las membrana, los ESCRT que son responsables en los endosomas de crear las vesículas de los cuerpos multivesiculares, etcétera. Por último, los filamentos de actina son unas auténticos curvadores de membranas mediante polimerización, mediante la cual empuja a la membrana plasmática hacia afuera creando expansiones celulares. Muchas de las proteínas capaces de curvar la membrana son también unas activadoras de la polimerización de filamentos de actina.

Algunos mecanismos moleculares que curvan las membranas de las células.
Otros dominios físicos de las membranas, aunque creados por moléculas presentes en la propia membrana como las proteínas transmembrana, son regiones de diferente espesor o altura. Son formados por proteínas transmembrana que tienen del dominio hidrofóbico más largo de lo habitual y por tanto se acomodan mejor en la membrana cuando se rodean de lípidos con cadenas de ácidos grasos largos. Estas agrupaciones de lípidos y proteínas crean áreas de mayor grosor que excluyen a otras proteínas con secuencias de aminoácidos hidrofóbicos más cortas o a lípidos con cadenas de ácidos grasos con menos átomos de carbono.

Dominio de membrana creado por diferencias de espesor.
|
No hay comentarios:
Publicar un comentario