La terapia con inhibidores de punto de control es una forma de inmunoterapia contra el cáncer actualmente en investigación. La terapia se dirige a los puntos de control inmunitarios , reguladores clave del sistema inmunitario que estimulan o inhiben sus acciones, que los tumores pueden usar para protegerse de los ataques del sistema inmunitario. La terapia de punto de control puede bloquear los puntos de control inhibitorios, restaurando la función del sistema inmunológico. [1] El primer medicamento contra el cáncer dirigido a un punto de control inmunológico fue ipilimumab , un bloqueador de CTLA4 aprobado en los Estados Unidos en 2011. [2]
Los inhibidores de punto de control aprobados actualmente apuntan a las moléculas CTLA4 , PD-1 y PD-L1 . PD-1 es la proteína transmembrana programada de la muerte celular 1 (también llamada PDCD1 y CD279), que interactúa con la PD-L1 ( ligando PD-1 1 o CD274). PD-L1 en la superficie celular se une a PD1 en una superficie de células inmunitarias, lo que inhibe la actividad de las células inmunitarias. Entre las funciones de PD-L1 se encuentra una función reguladora clave en las actividades de las células T. [3] [4] Parece que la regulación positiva (mediada por el cáncer) de PD-L1 en la superficie celular puede inhibir las células T que, de lo contrario, podrían atacar. Los anticuerpos que se unen a PD-1 o PD-L1 y, por lo tanto, bloquean la interacción pueden permitir que las células T ataquen el tumor. [5]
Los descubrimientos en la ciencia básica que permiten terapias con inhibidores de puntos de control llevaron a James P. Allison y Tasuku Honjo a ganar el Premio Tang en Biofarmacéutica y el Premio Nobel de Fisiología o Medicina en 2018.
Tipos [ editar ]
| Nombre | Objetivo | Aprobado |
|---|---|---|
| Ipilimumab | CTLA-4 | 2011 |
| Nivolumab | PD-1 | 2014 |
| Pembrolizumab | PD-1 | 2014 |
| Atezolizumab | PD-L1 | 2016 |
| Avelumab | PD-L1 | 2017 |
| Durvalumab | PD-L1 | 2017 |
| Cemiplimab | PD-1 | 2018 |
CTLA-4 bloqueo [ editar ]
El primer anticuerpo de punto de control aprobado por la FDA fue ipilimumab, aprobado en 2011 para el tratamiento del melanoma . [2]Bloquea la molécula de control inmunitario CTLA-4 . Los ensayos clínicos también han demostrado algunos beneficios de la terapia anti-CTLA-4 sobre el cáncer de pulmón o el cáncer de páncreas, específicamente en combinación con otros medicamentos. [8] [9]
Sin embargo, los pacientes tratados con bloqueo del punto de control (específicamente los anticuerpos bloqueadores de CTLA-4), o una combinación de anticuerpos bloqueadores del punto de control, tienen un alto riesgo de sufrir eventos adversos relacionados con el sistema inmunitario, como dermatológicos, gastrointestinales, endocrinos o hepáticos. Reacciones autoinmunes . [10] Esto es más probable debido a la amplitud de la activación de las células T inducida cuando los anticuerpos anti-CTLA-4 se administran por inyección en el torrente sanguíneo.
Utilizando un modelo de ratón de cáncer de vejiga, los investigadores han encontrado que una inyección local de una dosis baja de anti-CTLA-4 en el área del tumor tenía la misma capacidad de inhibición del tumor que cuando se administró el anticuerpo en la sangre. [11] Al mismo tiempo, los niveles de anticuerpos circulantes fueron más bajos, lo que sugiere que la administración local de la terapia anti-CTLA-4 podría resultar en menos eventos adversos. [11]
Inhibidores de PD-1 [ editar ]
Los resultados iniciales de los ensayos clínicos con el anticuerpo IgG4 PD1 Nivolumab (con el nombre de marca Opdivo y desarrollado por Bristol-Myers Squibb ) se publicaron en 2010. [1] Se aprobó en 2014. Nivolumab está aprobado para tratar el melanoma, el cáncer de pulmón, el cáncer de riñón, cáncer de vejiga, cáncer de cabeza y cuello y linfoma de Hodgkin . [12]
Pembrolizumab (nombre de marca Keytruda) es otro inhibidor de PD1 que fue aprobado por la FDA en 2014 y fue el segundo inhibidor de punto de control aprobado en los Estados Unidos. [13] Keytruda está aprobado para tratar el melanoma y el cáncer de pulmón y es producido por Merck . [12]
Spartalizumab (PDR001) es un inhibidor de la PD-1 que actualmente Novartis está desarrollando para tratar tumores sólidos y linfomas [14] [15] [16]
Inhibidores de PD-L1 [ editar ]
En mayo de 2016, el inhibidor de PD-L1 atezolizumab fue aprobado para tratar el cáncer de vejiga. [ cita requerida ]
Otro [ editar ]
Otros modos de mejorar la inmunoterapia [adoptiva] incluyen la orientación de los llamados bloqueos de punto de control intrínsecos, por ejemplo, CISH .
Efectos adversos [ editar ]
Los efectos adversos inmunológicos pueden ser causados por inhibidores del punto de control. La alteración de la inhibición del punto de control puede tener diversos efectos en la mayoría de los sistemas de órganos del cuerpo. El mecanismo preciso es desconocido, pero difiere en algunos aspectos en función de la molécula seleccionada.
Las células T receptoras de antígeno quimérico (también conocidas como células CAR T ) son células T que han sido diseñadas genéticamente para producir un receptor de células T artificial .
Los receptores de antígenos quiméricos ( CARs , también conocidos como inmunorreceptores quiméricos , receptores de células T quiméricos o receptores de células T artificiales ) son proteínas receptoras que se han diseñado para dar a las células T la nueva capacidad de dirigirse a una proteína específica . Los receptores son quiméricos porque combinan las funciones de unión a antígeno y de activación de células T en un solo receptor.
La terapia con células CAR-T utiliza células T diseñadas con CAR para la terapia del cáncer. La premisa de la inmunoterapia con CAR-T es modificar las células T para reconocer las células cancerosas con el fin de atacarlas y destruirlas con mayor eficacia. Los científicos recolectan células T de personas, las alteran genéticamente y luego inyectan las células CAR-T resultantes en pacientes para atacar sus tumores. [1] Las células CAR-T pueden derivar de células T en la propia sangre de un paciente ( autólogas ) o derivarse de las células T de otro donante sano ( alogénico). Una vez aisladas de una persona, estas células T están diseñadas genéticamente para expresar un CAR específico, que las programa para atacar un antígeno que está presente en la superficie de los tumores. Por seguridad, las células CAR-T están diseñadas para ser específicas a un antígeno expresado en un tumor que no se expresa en células sanas. [2]
Después de infundir células CAR-T en un paciente, actúan como un "fármaco vivo" contra las células cancerosas. [3] Cuando entran en contacto con su antígeno objetivo en una célula, las células CAR-T se unen a él y se activan, luego proliferan y se vuelven citotóxicas . [4] Las células CAR-T destruyen las células a través de varios mecanismos, incluida la proliferación celular extensiva estimulada, lo que aumenta el grado en que son tóxicas para otras células vivas (citotoxicidad), y provoca la mayor secreción de factores que pueden afectar a otras células, como Citoquinas , interleucinas y factores de crecimiento.
Producción [ editar ]
El primer paso en la producción de células CAR-T es el aislamiento de las células T de la sangre humana. Las células CAR-T pueden fabricarse a partir de la propia sangre del paciente, conocida como tratamiento autólogo , o de la sangre de un donante sano, conocida como tratamiento alogénico . El proceso de fabricación es el mismo en ambos casos; Sólo la elección del donante de sangre inicial es diferente.
Primero, los leucocitos se aíslan utilizando un separador de células sanguíneas en un proceso conocido como aféresis de leucocitos . Las células mononucleares de sangre periférica (PBMC) se separan y se recogen. [6] Los productos de la aféresis de leucocitos se transfieren a un centro de procesamiento celular. En el centro de procesamiento celular, se estimulan células T específicas para que proliferen activamente y se expandan a grandes números. Para conducir su expansión, las células T se tratan típicamente con la citocina interleucina 2 (IL-2) y anti- CD3 anticuerpos . [7]
Las células T expandidas se purifican y luego se transducen con un gen que codifica la CAR diseñada mediante un vector retroviral, típicamente un gammaretrovirus integrante (RV) o un vector lentiviral (LV). Estos vectores son muy seguros en los tiempos modernos debido a una eliminación parcial de la región U3. [8]
El paciente se somete a quimioterapia con linfodepleción antes de la introducción de las células CAR-T diseñadas. [9] El agotamiento de la cantidad de leucocitos circulantes en el paciente aumenta la cantidad de citoquinas que se producen y reduce la competencia por los recursos, lo que ayuda a promover la expansión de las células CAR-T diseñadas. [10]
El tratamiento del cáncer [ editar ]
Las células T están diseñadas genéticamente para expresar receptores de antígenos quiméricos específicamente dirigidos hacia los antígenos en las células tumorales de un paciente, y luego se inyectan en el paciente donde atacan y matan a las células cancerosas. [11] Latransferencia adoptiva de células T que expresan CAR es una terapéutica anticancerígena prometedora, ya que las células T modificadas con CAR pueden diseñarse para atacar virtualmente cualquier antígeno asociado a un tumor . Existe un gran potencial para que este enfoque mejore la terapia del cáncer específica para el paciente de manera profunda.
La investigación inicial sobre las células CAR-T se ha centrado en los cánceres de sangre . Los primeros tratamientos aprobados utilizan CAR que apuntan al antígeno CD19 , presente en los cánceres derivados de células B , como la leucemia linfoblástica aguda (LLA) y el linfoma difuso de células B grandes (DLBCL). También se están realizando esfuerzos para diseñar CAR dirigidos a muchos otros antígenos del cáncer de la sangre, incluido el CD30 en el linfoma de Hodgkin refractario ; CD33 , CD123 y FLT3 en leucemia mieloide aguda (LMA); y BCMA en el mieloma múltiple . [12]
Los tumores sólidos han presentado un objetivo más difícil. [13] Laidentificación de buenos antígenos ha sido desafiante: dichos antígenos deben expresarse en gran medida en la mayoría de las células cancerosas, pero en gran parte ausentes en los tejidos normales. Las células CAR-T tampoco son traficadas eficientemente hacia el centro de las masas tumorales sólidas, y el microambiente tumoral hostil suprime la actividad de las células T. [12]
Los estudios clínicos y aprobaciones de la FDA [ editar ]
Las dos primeras terapias CAR-T aprobadas por la FDA apuntan al antígeno CD19 , que se encuentra en muchos tipos de cánceres de células B. [14] Tisagenlecleucel (Kymriah) está aprobado para tratar leucemia linfoblástica aguda precursora de células B en recaída / refractaria , mientras que axicabtagene ciloleucel(Yescarta) está aprobado para tratar linfoma de células B grande difusa recidivante / refractario (DLBCL). [14]
A partir de marzo de 2019, había alrededor de 364 ensayos clínicos en curso que tenían lugar en todo el mundo e incluían células CAR-T. [15] La mayoría de esos ensayos se dirigen a los cánceres de sangre: las terapias CAR-T representan más de la mitad de todos los ensayos para enfermedades malignas hematológicas. [15] CD19 sigue siendo el objetivo de antígeno más popular, seguido de BCMA (comúnmente expresado en mieloma múltiple ). [15] En 2016, los estudios comenzaron a explorar la viabilidad de otros antígenos, como el CD20. [16] Los ensayos para tumores sólidos están menos dominados por CAR-T, con aproximadamente la mitad de los ensayos basados en terapia celular que involucran otras plataformas como las células NK . [15]
Aunque las tasas iniciales de remisión clínica después de la terapia con células CAR-T en pacientes con ALL son tan altas como 90%, [17] las tasas de supervivencia a largo plazo son mucho más bajas. La causa suele ser la aparición de células de leucemia que no expresan CD19 y, por lo tanto, evitan el reconocimiento por parte de las células T CD19-CAR, un fenómeno conocido como escape de antígeno . [12] Los estudios preclínicos que desarrollan células CAR-T con diana dual de CD19 más CD22 o CD19 más CD20 han demostrado ser prometedores, y los ensayos que estudian la focalización biespecífica para evitar la regulación negativa de CD19 continúan. [12]
Preocupaciones de seguridad [ editar ]
Las células CAR-T son, sin duda, un gran avance en el tratamiento del cáncer. Sin embargo, hay efectos secundarios graves que resultan de la introducción de células CAR-T en el cuerpo, incluido el síndrome de liberación de citoquinas y la toxicidad neurológica. [9] Debido a que es un tratamiento relativamente nuevo, hay poca información sobre los efectos a largo plazo de la terapia con células CAR-T. Todavía hay preocupaciones sobre la supervivencia del paciente a largo plazo, así como las complicaciones del embarazo en mujeres tratadas con células CAR-T. [18]
El problema más común después del tratamiento con células CAR-T es el síndrome de liberación de citoquinas (SRC), una afección en la que el sistema inmunitario se activa y libera un mayor número de citoquinasinflamatorias . La manifestación clínica de este síndrome se parece a la sepsis con fiebre alta, fatiga, mialgia , náuseas, fugas capilares, taquicardia y otras disfunciones cardíacas, insuficiencia hepática y insuficiencia renal. [19] La CRS ocurre en casi todos los pacientes tratados con terapia con células CAR-T; de hecho, la presencia de CRS es un marcador de diagnóstico que indica que las células CAR-T están funcionando como las que intentan destruir las células cancerosas. [18]Tenga en cuenta, sin embargo, que un mayor grado de severidad del SRC no se correlaciona con una mayor respuesta al tratamiento, sino con una mayor carga de la enfermedad. [18]
La toxicidad neurológica también suele asociarse con el tratamiento con células CAR-T. [20] El mecanismo subyacente es poco conocido, y puede o no estar relacionado con el SRC. Las manifestaciones clínicas incluyen delirio, la pérdida parcial de la capacidad de hablar de manera coherente y la capacidad de interpretar el lenguaje ( afasia expresiva ), la disminución del estado de alerta ( obtundación ) y las convulsiones. [18] Durante algunos ensayos clínicos se produjeron muertes causadas por neurotoxicidad. La principal causa de muerte por neurotoxicidad es el edema cerebral . En un estudio realizado por Juno Therapeutics , Inc., cinco pacientes inscritos en el ensayo murieron como resultado de un edema cerebral. Dos de los pacientes fueron tratados conLa ciclofosfamida sola y los tres restantes se trataron con una combinación de ciclofosfamida y fludarabina . [21] En otro ensayo clínico patrocinado por el Centro de Investigación del Cáncer Fred Hutchinson , hubo un caso reportado de toxicidad neurológica irreversible y fatal 122 días después de la administración de células CAR-T. [22]
La anafilaxis es un efecto secundario esperado, ya que el CAR se fabrica con un anticuerpo monoclonal extraño y, como resultado, provoca una respuesta inmune.
El reconocimiento en el blanco / fuera del tumor se produce cuando la célula CAR-T reconoce el antígenocorrecto , pero el antígeno se expresa en un tejido sano y no patógeno. Esto provoca que las células CAR-T ataquen tejidos no tumorales, como las células B sanas que expresan CD19. La gravedad de este efecto adverso puede variar desde la aplasia de células B , que puede tratarse con infusiones de apoyo, hasta toxicidad extrema que conduce a la muerte. [7]
También existe la posibilidad poco probable de que las células CAR-T modificadas por ingeniería propia se transformen en células cancerosas a través de la mutagénesis de inserción , debido a que el vector viral inserta el gen CAR en un supresor de tumores o en un oncogén en el genoma de la célula T huésped. Los vectores lentivíricos (LV) tienen un riesgo menor que los vectores retrovirales (RV). Sin embargo, ambos tienen el potencial de ser oncogénicos.
La estructura del receptor [ editar ]
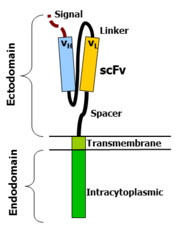
Los receptores de antígenos quiméricos combinan muchas facetas de la activación normal de las células T en una sola proteína. Unen un dominio de reconocimiento de antígeno extracelular a dominios de señalización intracelular, que activa la célula T cuando se une un antígeno. Las CAR se componen de tres regiones: el ectodominio , el dominio transmembrana y el endodominio . [23]
Ectodominio [ editar ]
El ectodominio es la región del receptor que está expuesta al exterior de la célula y, por lo tanto, interactúa con las posibles moléculas diana. Consta de 3 componentes principales: una región de reconocimiento de antígeno que se une a la molécula diana, un péptido señal que dirige la proteína naciente hacia el retículo endoplásmico y un espaciador que hace que el receptor esté más disponible para la unión.
La región de reconocimiento de antígenos es responsable de dirigir las células CAR-T a las células que expresan una molécula particular, y típicamente consiste en un fragmento variable de cadena única (scFv). [23] Un scFv es una proteína quimérica compuesta de la luz (V L ) y pesada (V H cadenas de) las inmunoglobulinas , conectado con un péptido enlazador corto. [24] Estos V L y V H regiones se seleccionan de antemano por su capacidad de unión al antígeno diana (por ejemplo, CD19). El enlazador entre las dos cadenas consiste en residuos hidrofílicos con tramos de glicina y serina.en él para la flexibilidad, así como estiramientos de glutamato y lisina para mayor solubilidad. [25]
El espaciador es un pequeño dominio estructural que se encuentra entre la región de reconocimiento del antígeno y la membrana externa de la célula. Un espaciador ideal aumenta la flexibilidad de la cabeza del receptor scFv, reduciendo las restricciones espaciales entre el CAR y su antígeno objetivo. Esto promueve la unión del antígeno y la formación de sinapsis entre las células CAR-T y las células diana. [26] Los espaciadores a menudo se basan en dominios de bisagra de IgG o CD8 . [27]
Dominio transmembrana [ editar ]
El dominio transmembrana es un componente estructural, que consiste en una hélice alfa hidrófoba que se extiende por la membrana celular. Este dominio es esencial para la estabilidad del receptor en su conjunto. En general, se usa el dominio transmembrana de la mayoría del componente proximal a la membrana del endodominio, pero los diferentes dominios transmembrana dan como resultado una estabilidad diferente del receptor. Se sabe que el dominio transmembrana de CD28 da como resultado un receptor estable altamente expresado.
No se recomienda el uso del dominio transmembrana CD3-zeta , ya que puede dar lugar a la incorporación del TCR artificial en el TCR nativo. [28]
Endodominio [ editar ]
Después de que un antígeno se une a la región externa de reconocimiento de antígenos, los receptores CAR se agrupan y transmiten una señal de activación. El endodominio es el extremo citoplásmico interno del receptor que perpetúa la señalización dentro de la célula T. [24]
La activación normal de las células T se basa en la fosforilación de los motivos de activación basados en tirosina inmunoreceptor (ITAM) presentes en el dominio citoplásmico de CD3-zeta . Para imitar este proceso, el dominio citoplasmático de CD3-zeta se usa comúnmente como el componente primario del endodominio CAR. También se han probado otros dominios que contienen ITAM, pero no son tan efectivos. [23]
Las células T también requieren moléculas coestimuladoras además de la señalización de CD3 para activarse. Por esta razón, los endodominios de los receptores CAR también suelen incluir uno o más dominios quiméricos de proteínas coestimuladoras, como CD28 , 4-1BB (CD137) u OX40 . [29]
Historia [ editar ]
Las primeras células CAR-T fueron desarrolladas en 1989 por Gideon Gross y Zelig Eshhar [31] [32] en el Instituto Weizmann , Israel. [33] La sofisticación de los receptores de CAR de ingeniería ha crecido con el tiempo y se conoce como CAR de primera, segunda, tercera o cuarta generación, según su composición.
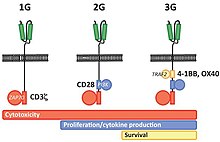
Los CAR de primera generación están compuestos por un dominio de unión extracelular, una región bisagra, un dominio transmembrana y uno o más dominios de señalización intracelular. [4] El dominio de unión extracelular contiene un fragmento variable de cadena única (scFv) derivado de anticuerpos reactivos al antígeno tumoral que generalmente tiene una alta especificidad a un antígeno tumoral específico. [4] Todos los CAR contienen el dominio de la cadena CD3ζ como el dominio de señalización intracelular, que es el transmisor principal de las señales de activación de las células T.
Los CAR de segunda generación agregan un dominio coestimulador, como CD28 o 4‐1BB. La participación de estos dominios de señalización intracelular mejora la proliferación de células T, la secreción de citoquinas, la resistencia a la apoptosis y la persistencia in vivo. [4]
Los CAR de tercera generación combinan múltiples dominios coestimulantes, como CD28-41BB o CD28-OX40, para aumentar la actividad de las células T. Los datos preclínicos muestran que los CAR de tercera generación exhiben funciones de efectoras mejoradas y una mejor persistencia in vivo en comparación con los CAR de segunda generación. [4]
Los CAR de cuarta generación (también conocidos como TRUCK o CAR blindados) agregan factores que mejoran la expansión de las células T, la persistencia y la actividad antitumoral. Esto puede incluir citocinas, como IL-2 , IL-5 , IL-12 y ligandos coestimulantes. [34] [35]
Smart T cell [ editar ]
Las células T inteligentes están diseñadas para incluir un mecanismo de control sintético. Estos permiten a los médicos controlar con precisión la persistencia o actividad de las células T en el cuerpo del paciente, con el objetivo de aliviar la citotoxicidad. [36] Las principales técnicas de control desencadenan la muerte de las células T, limitan la activación de las células T para que solo ocurra cuando las células tumorales estén cerca, o regulan las células T a través de un medicamento separado que se puede introducir o retener según sea necesario.
Genes suicidas: las células T modificadas genéticamente están diseñadas para incluir uno o más genes que pueden inducir la apoptosis cuando son activadas por una molécula extracelular. La timidina quinasa del virus del herpes simple (HSV-TK) y la caspasa inducible 9 (iCasp9) son dos tipos de genes suicidas que se han integrado en las células CAR-T. [36] [37] [38]En el sistema iCasp9, el complejo del gen suicida tiene dos elementos: una proteína de unión a FK506 mutada con alta especificidad a la pequeña molécula rimiducid / AP1903, y un gen que codifica una caspasa humana pro-domain borrada. 9. Dosificación al paciente de activados rimiducidos El sistema suicida, que conduce a una rápida apoptosis de las células T modificadas genéticamente. Aunque los sistemas HSV-TK e iCasp9 demuestran una función notable como interruptor de seguridad en los ensayos clínicos, algunos defectos limitan su aplicación. HSV-TK es derivado de virus y puede ser inmunogénico para los humanos. [36] [39] En la actualidad, tampoco está claro si las estrategias de los genes suicidas actuarán con la suficiente rapidez en todas las situaciones para detener la peligrosa citotoxicidad no tumoral.
Receptor de antígeno dual: las células CAR-T están diseñadas para expresar dos receptores de antígeno asociados a tumores al mismo tiempo, lo que reduce la probabilidad de que las células T ataquen células no tumorales. Se ha informado que las células CAR-T del receptor de antígeno dual tienen efectos secundarios menos intensos. [40] Un estudio in vivo en ratones muestra que las células CAR-T de doble receptor erradicaron el cáncer de próstata y lograron una supervivencia completa a largo plazo. [41]
ON-switch: En este sistema, las células CAR-T solo pueden funcionar en presencia de un antígeno tumoral y una molécula exógena benigna. Para lograr esto, el receptor de antígeno quimérico de ingeniería de las células CAR-T se divide en dos proteínas separadas que deben unirse para que funcione. La primera proteína receptora contiene típicamente el dominio de unión a antígeno extracelular, mientras que la segunda proteína contiene los elementos de señalización corriente abajo y las moléculas coestimuladoras (como CD3ζ y 4-1BB). En presencia de una molécula exógena (como un análogo de rapamicina), las proteínas de unión y señalización se dimerizan juntas, lo que permite que las células CAR-T ataquen el tumor. [42]
Moléculas biespecíficas como interruptores: las moléculas biespecíficas se dirigen tanto a un antígeno asociado a un tumor como a la molécula CD3 en la superficie de las células T. Esto asegura que las células T no puedan activarse a menos que estén cerca de una célula tumoral. [43] La molécula biespecífica anti-CD20 / CD3 muestra una alta especificidad tanto para las células B malignas como para las células cancerosas en ratones. [44] FITC es otra molécula bifuncional utilizada en esta estrategia. FITC puede redirigir y regular la actividad de las células CAR-T específicas de FITC hacia células tumorales con receptores de folato. [45]
Tecnología de adaptador SMDC [ editar ]
La plataforma de SMDC (conjugados farmacológicos de molécula pequeña) en inmuno-oncología es un enfoque novedoso (actualmente experimental) que hace posible la ingeniería de una única célula CAR T universal, que se une con una afinidad extraordinariamente alta a una molécula benigna designada como FITC . Estas células se utilizan para tratar varios tipos de cáncer cuando se administran conjuntamente con moléculas adaptadoras SMDC biespecíficas. Estos adaptadores biespecíficos únicos están construidos con una molécula FITCy una molécula que se dirige al tumor para unir con precisión la célula universal CAR T con las células cancerosas, lo que causa la activación localizada de las células T. La actividad antitumoral en ratones se induce solo cuando están presentes tanto las células universales CAR T como las moléculas adaptadoras específicas de antígeno correctas. La actividad antitumoral y la toxicidad pueden controlarse ajustando la dosificación de la molécula adaptadora administrada. El tratamiento de tumores antigénicamente heterogéneos se puede lograr mediante la administración de una mezcla de los adaptadores específicos de antígeno deseados. Por lo tanto, varios desafíos de las terapias actuales con células T CAR, tales como:
- La incapacidad para controlar la tasa de liberación de citoquinas y la lisis tumoral
- la ausencia de un "interruptor de apagado" que puede terminar la actividad citotóxica cuando se completa la erradicación del tumor
- un requisito para generar una célula CAR T diferente para cada antígeno tumoral único
Puede resolverse o mitigarse utilizando este enfoque.


No hay comentarios:
Publicar un comentario