(Redirigido desde la transformación química )
Una reacción química es un proceso que conduce a la transformación química de un conjunto de sustancias químicas a otro. [1] Clásicamente, las reacciones químicas abarcan cambios que solo involucran las posiciones de los electrones en la formación y ruptura de los enlaces químicos entre los átomos , sin cambios en los núcleos (sin cambios en los elementos presentes), y a menudo pueden ser descritos por un químico ecuación . La química nuclear es una subdisciplina de la químicaque involucra las reacciones químicas de inestabilidad y Elementos radiactivos donde pueden ocurrir cambios electrónicos y nucleares.
La sustancia (o sustancias) inicialmente involucradas en una reacción química se llaman reactivos o reactivos . Las reacciones químicas generalmente se caracterizan por un cambio químico , y producen uno o más productos , que generalmente tienen propiedades diferentes a las de los reactivos. Las reacciones a menudo consisten en una secuencia de subpasos individuales, las llamadas reacciones elementales , y la información sobre el curso preciso de acción es parte del mecanismo de reacción . Las reacciones químicas se describen con ecuaciones químicas , que presentan simbólicamente los materiales de partida, los productos finales y, a veces, los productos intermedios y las condiciones de reacción.
Las reacciones químicas se producen a una velocidad de reacción característica a una temperatura y concentración química determinadas. Típicamente, las velocidades de reacción aumentan con el aumento de la temperatura porque hay más energía térmica disponible para alcanzar la energía de activación necesaria para romper los enlaces entre los átomos.
Las reacciones pueden proceder en la dirección hacia adelante o hacia atrás hasta que se completen o alcancen el equilibrio. Las reacciones que proceden en la dirección hacia adelante para acercarse al equilibrio a menudo se describen como espontáneas y no requieren la entrada de energía libre para avanzar. Las reacciones no espontáneas requieren la entrada de energía libre para avanzar (los ejemplos incluyen cargar una batería mediante la aplicación de una fuente de energía eléctrica externa o la fotosíntesis impulsada por la absorción de radiación electromagnética en forma de luz solar).
Se utilizan diferentes reacciones químicas en combinaciones durante la síntesis química para obtener un producto deseado. En bioquímica , una serie consecutiva de reacciones químicas (donde el producto de una reacción es el reactivo de la siguiente reacción) forma rutas metabólicas . Estas reacciones a menudo son catalizadas por enzimas proteicas . Las enzimas aumentan las tasas de reacciones bioquímicas, de modo que pueden producirse síntesis metabólicas y descomposiciones imposibles en condiciones normales a las temperaturas y concentraciones presentes dentro de una célula .
El concepto general de una reacción química se ha extendido a las reacciones entre entidades más pequeñas que los átomos, incluidas las reacciones nucleares , las desintegraciones radiactivas y las reacciones entre partículas elementales , según lo descrito por la teoría cuántica de campos .
Historia
Las reacciones químicas como la combustión en el fuego, la fermentación y la reducción de minerales a metales se conocieron desde la antigüedad. Los filósofos griegos desarrollaron teorías iniciales sobre la transformación de materiales, como la Teoría de los cuatro elementosde Empédocles que establece que cualquier sustancia está compuesta por los cuatro elementos básicos: fuego, agua, aire y tierra. En la Edad Media, las transformaciones químicas fueron estudiadas por los alquimistas . Intentaron, en particular, convertir el plomo en oro , para lo cual utilizaron reacciones de plomo y aleaciones de plomo-cobre con azufre . [2]
La producción de sustancias químicas que normalmente no ocurren en la naturaleza ha sido probada durante mucho tiempo, como la síntesis de ácidos sulfúricos y nítricos atribuidos al controvertido alquimista Jābir ibn Hayyān . El proceso implicó el calentamiento de minerales de sulfato y nitrato como sulfato de cobre , alumbre y salitre . En el siglo XVII, Johann Rudolph Glauber produjo ácido clorhídrico y sulfato de sodio al reaccionar el ácido sulfúrico y el cloruro de sodio . Con el desarrollo del proceso de cámara de plomo en 1746 y el proceso de Leblanc, permitiendo la producción a gran escala de ácido sulfúrico y carbonato de sodio , respectivamente, las reacciones químicas se implementaron en la industria. Una mayor optimización de la tecnología del ácido sulfúrico resultó en el proceso de contacto en la década de 1880, [3] y el proceso de Haber se desarrolló en 1909-1910 para la síntesis de amoníaco . [4]
A partir del siglo XVI, investigadores como Jan Baptist van Helmont , Robert Boyle e Isaac Newton intentaron establecer teorías de las transformaciones químicas observadas experimentalmente. La teoría del flogisto fue propuesta en 1667 por Johann Joachim Becher . Postulaba la existencia de un elemento similar al fuego llamado "flogisto", que estaba contenido dentro de cuerpos combustibles y liberado durante la combustión . Esto resultó ser falso en 1785 por Antoine Lavoisier, quien encontró la explicación correcta de la combustión como reacción con el oxígeno del aire. [5]
Joseph Louis Gay-Lussac reconoció en 1808 que los gases siempre reaccionan en cierta relación entre ellos. Basado en esta idea y en la teoría atómica de John Dalton , Joseph Proust había desarrollado la ley de proporciones definidas , que más tarde resultó en los conceptos de estequiometría y ecuaciones químicas . [6]
Con respecto a la química orgánica , durante mucho tiempo se creyó que los compuestos obtenidos de organismos vivos eran demasiado complejos para ser obtenidos sintéticamente . Según el concepto de vitalismo, la materia orgánica estaba dotada de una "fuerza vital" y se distinguía de los materiales inorgánicos. Sin embargo, esta separación terminó con la síntesis de urea a partir de precursores inorgánicos por Friedrich Wöhler en 1828. Otros químicos que aportaron importantes contribuciones a la química orgánica incluyen a Alexander William Williamson con su síntesis de éteres y Christopher Kelk Ingold , quien, entre muchos descubrimientos, estableció el mecanismos dereacciones de sustitución .
Ecuaciones
Las ecuaciones químicas se utilizan para ilustrar gráficamente las reacciones químicas. Consisten en fórmulas químicas o estructuralesde los reactivos a la izquierda y de los productos a la derecha. Están separados por una flecha (→) que indica la dirección y el tipo de reacción; la flecha se lee como la palabra "cede". [7] La punta de la flecha apunta en la dirección en que procede la reacción. Se usa una flecha doble (pointing) que apunta en direcciones opuestas para las reacciones de equilibrio . Las ecuaciones deben estar equilibradas de acuerdo con la estequiometría , el número de átomos de cada especie debe ser el mismo en ambos lados de la ecuación. Esto se logra al escalar el número de moléculas involucradas ( y en un ejemplo esquemático a continuación) por los enteros apropiados a, b, c y d . [8]
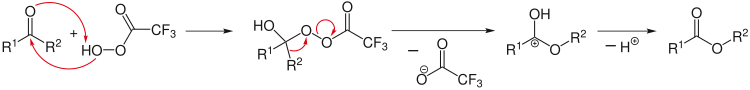
Las reacciones más elaboradas están representadas por esquemas de reacción, que además de los materiales de partida y los productos muestran intermedios importantes o estados de transición . Además, algunas adiciones relativamente menores a la reacción se pueden indicar sobre la flecha de reacción; ejemplos de tales adiciones son agua, calor, iluminación, un catalizador, etc. De manera similar, algunos productos menores se pueden colocar debajo de la flecha, a menudo con un signo menos.
El análisis retrosintético se puede aplicar para diseñar una reacción de síntesis compleja. Aquí el análisis comienza con los productos, por ejemplo, dividiendo los enlaces químicos seleccionados, para llegar a reactivos iniciales plausibles. Una flecha especial (⇒) se usa en reacciones retro. [9]
Reacciones elementales
La reacción elemental es la división más pequeña en la que se puede descomponer una reacción química, no tiene productos intermedios. [10] La mayoría de las reacciones observadas experimentalmente se desarrollan a partir de muchas reacciones elementales que ocurren en paralelo o secuencialmente. La secuencia real de las reacciones elementales individuales se conoce como mecanismo de reacción . Una reacción elemental involucra unas pocas moléculas, generalmente una o dos, debido a la baja probabilidad de que varias moléculas se encuentren en un momento determinado. [11]
Las reacciones elementales más importantes son las reacciones unimoleculares y bimoleculares. Solo una molécula está involucrada en una reacción unimolecular; se transforma mediante una isomerización o una disociación en una o más moléculas diferentes. Dichas reacciones requieren la adición de energía en forma de calor o luz. Un ejemplo típico de una reacción unimolecular es la isomerización cis-trans , en la cual la forma cis de un compuesto se convierte en la forma trans o viceversa. [12]
En una reacción de disociación típica , un enlace en una molécula se divide (se rompe ) dando como resultado dos fragmentos moleculares. La división puede ser homolítica o heterolítica . En el primer caso, el enlace se divide para que cada producto retenga un electrón y se convierta en un radical neutro . En el segundo caso, ambos electrones del enlace químico permanecen con uno de los productos, lo que resulta en iones cargados . La disociación juega un papel importante en la activación de reacciones en cadena , como las reacciones de hidrógeno-oxígeno o polimerización .
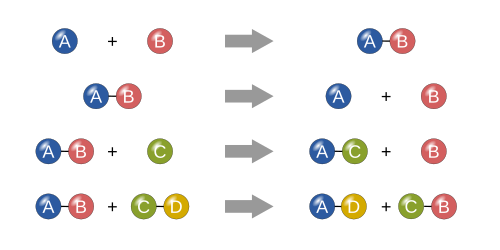
- Disociación de una molécula AB en fragmentos A y B
Para reacciones bimoleculares, dos moléculas chocan y reaccionan entre sí. Su fusión se llama síntesis químicao reacción de adición .
Otra posibilidad es que solo una parte de una molécula se transfiera a la otra molécula. Este tipo de reacción ocurre, por ejemplo, en reacciones redox y ácido-base. En las reacciones redox, la partícula transferida es un electrón, mientras que en las reacciones ácido-base es un protón. Este tipo de reacción también se llama metátesis .
por ejemplo
Equilibrio químico
La mayoría de las reacciones químicas son reversibles, es decir, pueden y corren en ambas direcciones. Las reacciones directas e inversas compiten entre sí y difieren en las velocidades de reacción . Estas velocidades dependen de la concentración y, por lo tanto, cambian con el tiempo de la reacción: la velocidad inversa aumenta gradualmente y se vuelve igual a la velocidad de la reacción directa, estableciendo el llamado equilibrio químico. El tiempo para alcanzar el equilibrio depende de parámetros tales como la temperatura, la presión y los materiales involucrados, y está determinado por la energía libre mínima . En equilibrio, la energía libre de Gibbsdebe ser cero. La dependencia de la presión puede explicarse con el principio de Le Chatelier.. Por ejemplo, un aumento en la presión debido a la disminución del volumen hace que la reacción se desplace hacia un lado con menos moles de gas. [13]
El rendimiento de la reacción se estabiliza en el equilibrio, pero puede aumentarse eliminando el producto de la mezcla de reacción o modificarse aumentando la temperatura o la presión. Un cambio en las concentraciones de los reactivos no afecta la constante de equilibrio, pero sí afecta la posición de equilibrio.
Termodinámica
Las reacciones químicas están determinadas por las leyes de la termodinámica . Las reacciones pueden proceder por sí mismas si son exergónicas , es decir, si liberan energía. La energía libre asociada de la reacción se compone de dos cantidades termodinámicas diferentes, entalpía y entropía : [14]
-
- .
- G : energía libre, H : entalpía, T : temperatura, S : entropía, Δ : diferencia (cambio entre original y producto)
Las reacciones pueden ser exotérmicas , donde ΔH es negativo y se libera energía. Ejemplos típicos de reacciones exotérmicas son la precipitación y la cristalización , en las que los sólidos ordenados se forman a partir de fases gaseosas o líquidas desordenadas. Por el contrario, en endotérmicareacciones, el calor se consume del medio ambiente. Esto puede ocurrir al aumentar la entropía del sistema, a menudo a través de la formación de productos de reacción gaseosa, que tienen alta entropía. Como la entropía aumenta con la temperatura, muchas reacciones endotérmicas tienen lugar preferiblemente a altas temperaturas. Por el contrario, muchas reacciones exotérmicas como la cristalización ocurren a bajas temperaturas. Los cambios de temperatura a veces pueden revertir el signo de la entalpía de una reacción, como para la reducción de monóxido de carbono del dióxido de molibdeno :
- ;
Esta reacción para formar dióxido de carbono y molibdeno es endotérmica a bajas temperaturas, volviéndose menos con el aumento de la temperatura. [15] ΔH ° es cero en1855 K , y la reacción se vuelve exotérmica por encima de esa temperatura.
Los cambios en la temperatura también pueden revertir la tendencia en la dirección de una reacción. Por ejemplo, la reacción de cambio de gas de agua
se ve favorecida por las bajas temperaturas, pero su inversa es favorecida por las altas temperaturas. El cambio en la tendencia de dirección de reacción ocurre en1100 K . [15]
Las reacciones también pueden caracterizarse por la energía interna que tiene en cuenta los cambios en la entropía, el volumen y el potencial químico . Esto último depende, entre otras cosas, de las actividades de las sustancias involucradas. [dieciséis]
-
- U : energía interna, S : entropía, p : presión, μ : potencial químico, n : número de moléculas, d : signo de cambio pequeño
Cinética
La velocidad a la que tienen lugar las reacciones se estudia mediante la cinética de reacción . La tasa depende de varios parámetros, como:
- Concentraciones de reactivos , que generalmente hacen que la reacción suceda a una velocidad más rápida si aumentan a través de un aumento de colisiones por unidad de tiempo. Sin embargo, algunas reacciones tienen tasas que son independientes de las concentraciones de reactivo. Estas se llaman reacciones de orden cero .
- Área de superficie disponible para el contacto entre los reactivos, en particular los sólidos en sistemas heterogéneos. Las áreas de superficie más grandes conducen a velocidades de reacción más altas.
- Presión : al aumentar la presión, disminuye el volumen entre las moléculas y, por lo tanto, aumenta la frecuencia de colisiones entre las moléculas.
- Energía de activación , que se define como la cantidad de energía requerida para que la reacción comience y continúe espontáneamente. Una energía de activación más alta implica que los reactivos necesitan más energía para comenzar que una reacción con una energía de activación más baja.
- Temperatura , que acelera las reacciones si se eleva, ya que una temperatura más alta aumenta la energía de las moléculas, creando más colisiones por unidad de tiempo,
- La presencia o ausencia de un catalizador . Los catalizadores son sustancias que cambian la vía (mecanismo) de una reacción que a su vez aumenta la velocidad de una reacción al disminuir la energía de activación necesaria para que la reacción tenga lugar. Un catalizador no se destruye ni cambia durante una reacción, por lo que puede usarse nuevamente.
- Para algunas reacciones, la presencia de radiación electromagnética , especialmente la luz ultravioleta , es necesaria para promover la ruptura de los enlaces para iniciar la reacción. Esto es particularmente cierto para las reacciones que involucran radicales .
Varias teorías permiten calcular las velocidades de reacción a nivel molecular. Este campo se conoce como dinámica de reacción. La velocidad v de una reacción de primer orden , que podría ser la desintegración de una sustancia A, viene dada por:
Su integración produce:
Aquí k es una tasa constante de primer orden que tiene una dimensión 1 / tiempo, [A] (t) es concentración en un tiempo ty [A] 0 es la concentración inicial. La velocidad de una reacción de primer orden depende solo de la concentración y las propiedades de la sustancia involucrada, y la reacción en sí misma puede describirse con la vida media característica . Se necesita más de una constante de tiempo cuando se describen reacciones de orden superior. La dependencia de la temperatura de la constante de velocidad generalmente sigue la ecuación de Arrhenius :
donde E a es la energía de activación y k B es la constante de Boltzmann . Uno de los modelos más simples de velocidad de reacción es la teoría de colisión . Los modelos más realistas se adaptan a un problema específico e incluyen la teoría del estado de transición , el cálculo de la superficie de energía potencial , la teoría de Marcus y la teoría de Rice-Ramsperger-Kassel-Marcus (RRKM) . [17]
Tipos de reacción
Cuatro tipos básicos
Síntesis
En una reacción de síntesis, dos o más sustancias simples se combinan para formar una sustancia más compleja. Estas reacciones son en forma general:
Dos o más reactivos que producen un producto es otra forma de identificar una reacción de síntesis. Un ejemplo de una reacción de síntesis es la combinación de hierro y azufre para formar sulfuro de hierro (II) :
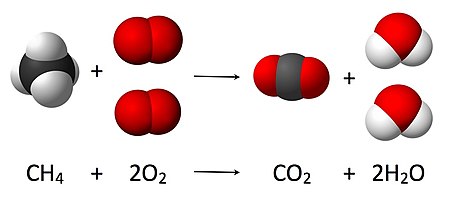
Otro ejemplo es el gas de hidrógeno simple combinado con gas de oxígeno simple para producir una sustancia más compleja, como el agua. [18]
Descomposición
Una reacción de descomposición es cuando una sustancia más compleja se descompone en sus partes más simples. Por lo tanto, es lo opuesto a una reacción de síntesis, y puede escribirse como [18] [19]
Un ejemplo de una reacción de descomposición es la electrólisis del agua para producir oxígeno y gas hidrógeno:
Reemplazo individual
En una única reacción de reemplazo , un solo elemento no combinado reemplaza a otro en un compuesto; en otras palabras, un elemento intercambia lugares con otro elemento en un compuesto [18] Estas reacciones vienen en la forma general de:
Un ejemplo de una reacción de desplazamiento único es cuando el magnesio reemplaza el hidrógeno en agua para producir hidróxido de magnesio y gas hidrógeno:
Doble reemplazo
En una reacción de doble reemplazo , los aniones y cationes de dos compuestos cambian de lugar y forman dos compuestos completamente diferentes. [18] Estas reacciones son en forma general: [19]
Por ejemplo, cuando el cloruro de bario (BaCl 2 ) y sulfato de magnesio (MgSO 4 ) reaccionan, el SO 4 2- anión cambia lugares con el 2Cl - anión, dando los compuestos BASO 4 y MgCl 2 .
Otro ejemplo de una reacción de doble desplazamiento es la reacción del nitrato de plomo (II) con yoduro de potasio para formar yoduro de plomo (II) y nitrato de potasio :
Oxidación y reducción
Las reacciones redox se pueden entender en términos de transferencia de electrones de una especie involucrada ( agente reductor ) a otra ( agente oxidante ). En este proceso, la primera especie se oxida y la segunda se reduce . Aunque suficientes para muchos propósitos, estas descripciones no son precisamente correctas. La oxidación se define mejor como un aumento en el estado de oxidación , y la reducción como una disminución en el estado de oxidación. En la práctica, la transferencia de electrones siempre cambiará el estado de oxidación, pero hay muchas reacciones que se clasifican como "redox" a pesar de que no se produce transferencia de electrones (como las que implican enlaces covalentes ). [20] [21]
En la siguiente reacción redox, el metal de sodio peligroso reacciona con cloro gaseoso tóxico para formar el compuesto iónico cloruro de sodio o sal de mesa común:
En la reacción, el sodio metálico pasa de un estado de oxidación de 0 (ya que es un elemento puro) a +1: en otras palabras, el sodio perdió un electrón y se dice que se ha oxidado. Por otro lado, el gas de cloro pasa de una oxidación de 0 (también es un elemento puro) a -1: el cloro gana un electrón y se dice que se ha reducido. Debido a que el cloro es el reducido, se considera el aceptor de electrones, o en otras palabras, induce oxidación en el sodio, por lo que el gas de cloro se considera el agente oxidante. Por el contrario, el sodio se oxida o es el donante de electrones, y por lo tanto induce la reducción en las otras especies y se considera el agente reductor .
¿Cuál de los reactivos involucrados sería agente reductor u oxidante puede predecirse a partir de la electronegatividad de sus elementos? Los elementos con baja electronegatividad, como la mayoría de los metales, donan fácilmente electrones y se oxidan, son agentes reductores. Por el contrario, muchos iones con altos números de oxidación, como H
2 O
2 ,MnO-
4 ,CrO
3 ,Cr
2 O2−
7 ,OsO
4 pueden ganar uno o dos electrones adicionales y son agentes oxidantes fuertes.
2 O
2 ,MnO-
4 ,CrO
3 ,Cr
2 O2−
7 ,OsO
4 pueden ganar uno o dos electrones adicionales y son agentes oxidantes fuertes.
El número de electrones donados o aceptados en una reacción redox puede predecirse a partir de la configuración electrónica del elemento reactivo. Los elementos intentan alcanzar la configuración de gas noble de baja energía y, por lo tanto, los metales alcalinos y los halógenos donarán y aceptarán un electrón respectivamente. Los gases nobles en sí mismos son químicamente inactivos. [22]
Una clase importante de reacciones redox son las reacciones electroquímicas , donde los electrones de la fuente de alimentación se utilizan como agente reductor. Estas reacciones son particularmente importantes para la producción de elementos químicos, como el cloro [23] o el aluminio . El proceso inverso en el que los electrones se liberan en reacciones redox y se pueden usar como energía eléctrica es posible y se usa en baterías.















![{\ displaystyle v = - {\ frac {d [{\ ce {A}}]} {dt}} = k \ cdot [{\ ce {A}}].}](https://wikimedia.org/api/rest_v1/media/math/render/svg/12291760fcaff20a02ff74abd0dfcb922664cddb)
![{\ displaystyle {\ ce {[A]}} (t) = {\ ce {[A]}} _ {0} \ cdot e ^ {- k \ cdot t}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/498c37558508e2f7297604f93bb5408dcd8c3fd4)










No hay comentarios:
Publicar un comentario