Una reacción de los medios seco o reacción de estado sólido o de reacción sin disolvente es una reacción química del sistema en ausencia de un disolvente . El impulso para el desarrollo de reacciones de medios secos en química es
- economía (ahorre dinero en solventes)
- facilidad de purificación (sin eliminación de disolventes después de la síntesis )
- alta velocidad de reacción (debido a la alta concentración de reactivos)
- respetuoso con el medio ambiente (no se requiere solvente), ver química verde
Inconvenientes a superar:
- los reactivos deben mezclarse con un sistema homogéneo
- alta viscosidad en el sistema reactivo
- inadecuado para reacciones químicas asistidas por solventes
- problemas con la disipación de calor de manera segura; riesgo de fuga térmica
- reacciones secundarias aceleradas
- si los reactivos son sólidos, muy alto consumo de energía de la molienda
En un tipo de reacción sin solvente, se usa un reactivo líquido puro , por ejemplo, la reacción de 1-bromonaftaleno con el reactivo de Lawesson se realiza sin solvente líquido agregado, pero el 1-bromonaftaleno actúa como solvente.
Una reacción que está más cerca de una verdadera reacción sin solvente es una condensación de cetonas de Knoevenagel con ( malononitrilo ) donde se irradia una mezcla 1: 1 de los dos reactivos (y acetato de amonio ) en un horno de microondas .
El grupo de investigación de Colin Raston ha sido responsable de una serie de nuevas reacciones sin solventes. En algunas de estas reacciones, todos los materiales de partida son sólidos, se muelen junto con algo de hidróxido de sodio para formar un líquido, que se convierte en una pasta que luego se endurece hasta convertirse en un sólido.
En otro desarrollo, los dos componentes de una reacción aldólica se combinan junto con el catalizador asimétricoS- prolina en un molino de bolas en una mecanosíntesis . El producto de reacción tiene un 97% de exceso enantiomérico .
Se observa una aceleración de la velocidad de reacción en varios sistemas cuando un sistema solvente homogéneo se evapora rápidamente en un rotavapor al vacío , uno de ellos es una reacción de Wittig . La reacción se completa en 5 minutos con evaporación inmediata, mientras que la misma reacción en solución después de los mismos 5 minutos ( diclorometano ) tiene solo un 70% de conversión e incluso después de 24 horas queda algo del aldehído.
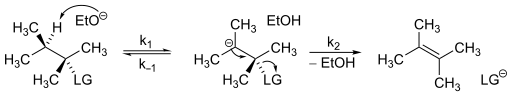
La reacción de eliminación de E1cBes un tipo de reacciónde eliminación que ocurre en condiciones básicas, donde el hidrógeno a eliminar es relativamente ácido, mientras que el grupo saliente (como -OH o -OR) es relativamente pobre. Por lo general, una base moderada a fuerte está presente. E1cB es un proceso de dos pasos, cuyo primer paso puede ser reversible o no. Primero, una base extrae el protón relativamente ácido para generar un anión estabilizado . El par solitario de electrones en el anión luego se mueve al átomo vecino, expulsando así el grupo saliente y formando un enlace doble o triple . [1] El nombre del mecanismo - E1cB- significa E limination U nimolecular conjugate B ase. La eliminación se refiere al hecho de que el mecanismo es una reacción de eliminación y perderá dos sustituyentes. Unimolecular se refiere al hecho de que el paso determinante de la velocidad de esta reacción solo involucra una entidad molecular . Finalmente, la base conjugada se refiere a la formación del carbanión intermedio , que es la base conjugada del material de partida.
Debe considerarse que E1cb está en un extremo de un continuo, que incluye el mecanismo E1 en el extremo opuesto y el mecanismo E2 en el medio. El mecanismo E1 generalmente tiene las características opuestas: el grupo saliente es bueno (como -OTs o -Br), mientras que el hidrógeno no es particularmente ácido y no hay una base fuerte. Por lo tanto, en el mecanismo E1, el grupo saliente se va primero para generar un carbocatión. Debido a la presencia de un orbital p vacío después de la partida del grupo saliente, el hidrógeno en el carbono vecino se vuelve mucho más ácido, lo que le permite ser eliminado por la base débil en el segundo paso. En una reacción E2, la presencia de una base fuerte y un buen grupo saliente permite que la abstracción de protones por parte de la base y la salida del grupo saliente ocurran simultáneamente.
Mecanismo [ editar ]
Hay dos requisitos principales para que una reacción avance por un camino mecanicista E1cB. El compuesto debe tener un hidrógeno ácido en su carbono β y un grupo salienterelativamente pobre en el carbono α . El primer paso de un mecanismo E1cB es la desprotonación del carbono β, lo que resulta en la formación de un estado de transición aniónico , como un carbanión. Cuanto mayor sea la estabilidad de este estado de transición, más favorecerá el mecanismo un mecanismo E1cB. Este estado de transición se puede estabilizar mediante inducción o deslocalización del par de electrones solos mediante resonancia.. En general, se puede afirmar que un grupo de extracción de electrones en el sustrato, una base fuerte, un grupo saliente pobre y un disolvente polar activa el mecanismo E1cB. Un ejemplo de un mecanismo E1cB que tiene un estado de transición estable se puede ver en la degradación de ethiofencarb , un insecticida carbamato que tiene una vida media relativamente corta en la atmósfera terrestre. Tras la desprotonación de la amina , la amida resultante es relativamente estable porque se conjuga con el carbonilo vecino . Además de contener un hidrógeno ácido en el carbono β, también es necesario un grupo saliente relativamente pobre. Un mal grupo de partidaes necesario porque un buen grupo saliente se irá antes de la ionización de la molécula. Como resultado, el compuesto probablemente procederá a través de una vía E2 . Algunos ejemplos de compuestos que contienen grupos salientes pobres y pueden sufrir el mecanismo E1cB son los alcoholes y los fluoroalcanos . También se ha sugerido que el mecanismo E1cB es más común entre los alquenos que eliminan a los alquinos que de un alcano a alqueno. [2] Una posible explicación para esto es que la hibridación sp 2 crea protones ligeramente más ácidos. Aunque este mecanismo no se limita al carbonoeliminaciones Se ha observado con otros heteroátomos , como el nitrógeno, en la eliminación de un derivado de fenol del etiofencarb . [3]
Distinguir las reacciones de eliminación de E1cB de las reacciones de eliminación de E1 y E2 [ editar ]
Todas las reacciones de eliminación implican la eliminación de dos sustituyentes de un par de átomos adyacentes en un compuesto. Alqueno, alquinos o variaciones de heteroátomos similares (como carbonilo y ciano) formará. El mecanismo E1cB es solo uno de los tres tipos de reacción de eliminación. Las otras dos reacciones de eliminación son las reacciones E1 y E2. Aunque los mecanismos son similares, varían en el momento de la desprotonación del carbono α y la pérdida del grupo saliente. E1 significa eliminación unimolecular, y E2 significa eliminación bimolecular. En un mecanismo E1, la molécula contiene un buen grupo saliente que parte antes de la desprotonación del carbono α. Esto da como resultado la formación de un carbocatión intermedio. El carbocatión se desprotona y se forma un nuevo enlace pi. La molécula involucrada también debe tener un grupo saliente muy bueno, como bromo o cloro, y debe tener un carbono α relativamente menos ácido.
En una reacción de eliminación de E2, tanto la desprotonación del carbono α como la pérdida del grupo saliente ocurren simultáneamente en un paso concertado . Las moléculas que se someten a mecanismos de eliminación de E2 tienen más α-carbonos ácidos que las que se someten a mecanismos E1, pero sus α-carbonos no son tan ácidos como los de las moléculas que se someten a mecanismos E1cB. La diferencia clave entre las vías E2 frente a E1cb es un carbanión intermedio distinto en lugar de un mecanismo concertado. Los estudios han demostrado que las vías difieren mediante el uso de diferentes grupos salientes halógenos . Un ejemplo usa cloro como un halógeno estabilizador mejor para el aniónque el flúor , [4] que hace que el flúor sea el grupo saliente aunque el cloro es un grupo saliente mucho mejor. [5] Esto proporciona evidencia de que el carbanión se forma porque los productos no son posibles a través del mecanismo E2 concertado más estable . La siguiente tabla resume las diferencias clave entre las tres reacciones de eliminación; Sin embargo, la mejor manera de identificar qué mecanismo está desempeñando un papel clave en una reacción particular implica la aplicación de la cinética química .
| E1 | E2 | E1cB |
|---|---|---|
| Reacción paso a paso | Reacción concertada | Reacción paso a paso |
| Carbocación intermedia | Eliminación simultánea de protones, formación de doble enlace y pérdida del grupo saliente. | Carbanion intermedio |
| ningún tipo de conclusión | Sin preferencias | ningún tipo de conclusión |
| Buenos grupos de partida | Dejando el grupo | Pobres grupos salientes |
| BH menos ácido | BH ácido | BH más ácido |
Cinética química de los mecanismos de eliminación de E1cB [ editar ]
Cuando se trata de determinar si una reacción sigue o no al mecanismo E1cB, la cinética química es esencial. La mejor manera de identificar el mecanismo E1cB implica el uso de leyes de velocidad y el efecto cinético del isótopo . Estas técnicas también pueden ayudar a diferenciar aún más entre las reacciones de eliminación de E1cB, E1 y E2.
Ley de tarifas [ editar ]
Cuando se trata de determinar experimentalmente si una reacción sigue o no el mecanismo E1cB, la cinética química es esencial. Las mejores formas de identificar el mecanismo E1cB implica el uso de leyes de velocidad y el efecto cinético del isótopo.
La ley de tasas que gobierna los mecanismos E1cB es relativamente simple de determinar. Considere el siguiente esquema de reacción.
Suponiendo que hay una concentración de carbaniones en estado estable en el mecanismo, la ley de velocidad para un mecanismo E1cB.
A partir de esta ecuación, está claro que se exhibirá la cinética de segundo orden . [6] La cinética de los mecanismos E1cB puede variar ligeramente según la velocidad de cada paso. Como resultado, el mecanismo E1cB se puede dividir en tres categorías: [7]
- El anión E1cB es cuando el carbanión es estable y / o se usa una base fuerte en exceso del sustrato, lo que hace que la desprotonación sea irreversible, seguida de la pérdida determinante de la velocidad del grupo saliente (k 1 [base] ≫ k 2 ).
- E1cB rev es cuando el primer paso es reversible pero la formación del producto es más lenta que la reforma del material de partida, esto nuevamente resulta de un segundo paso lento (k −1 [ácido conjugado] ≫ k 2 ).
- E1cB irr es cuando el primer paso es lento, pero una vez que se forma el anión, el producto sigue rápidamente (k 2 ≫ k −1 [ácido conjugado]). Esto conduce a un primer paso irreversible, pero a diferencia del anión E1cB , la desprotonación determina la velocidad.
Efecto de isótopo cinético [ editar ]
Deuterio [ editar ]
El intercambio de deuterio y un efecto de isótopo cinético de deuterio pueden ayudar a distinguir entre E1cB rev , E1cB anion y E1cB irr . Si el disolvente es prótico y contiene deuterio en lugar de hidrógeno (por ejemplo, CH 3OD), a continuación, el intercambio de los protones en el material de partida se puede controlar. Si el material de partida recuperado contiene deuterio, lo más probable es que la reacción esté experimentando un revE1cBMecanismo de tipo. Recuerde, en este mecanismo, la protonación del carbanión (ya sea por el ácido conjugado o por el solvente) es más rápido que la pérdida del grupo saliente. Esto significa que después de que se forma el carbanión, eliminará rápidamente un protón del disolvente para formar el material de partida.
Si el reactivo contiene deuterio en la posición β, un efecto de isótopo cinético primario indica que la desprotonación determina la velocidad. De los tres mecanismos E1cB, este resultado solo es consistente con el mecanismo E1cB irr , ya que el isótopo ya está eliminado en el anión E1cB y la salida del grupo de partida es determinante de la velocidad en E1cB rev .
Si el reactivo contiene deuterio en la posición β, un efecto de isótopo cinético primario indica que la desprotonación determina la velocidad. De los tres mecanismos E1cB, este resultado solo es consistente con el mecanismo E1cB irr , ya que el isótopo ya está eliminado en el anión E1cB y la salida del grupo de partida es determinante de la velocidad en E1cB rev .
Flúor-19 y carbono-11 [ editar ]
Otra forma en que el efecto cinético del isótopo puede ayudar a distinguir los mecanismos E1cB implica el uso de 19 F. El flúor es un grupo saliente relativamente pobre, y a menudo se emplea en mecanismos E1cB. Los efectos del isótopo cinético del flúor también se aplican en el etiquetado de radiofármacos y otros compuestos en la investigación médica. Este experimento es muy útil para determinar si la pérdida del grupo saliente es el paso determinante de la velocidad en el mecanismo y puede ayudar a distinguir entre los mecanismos E1cB irr y E2. 11 C también se puede utilizar para sondear la naturaleza de la estructura del estado de transición. El uso de 11C puede usarse para estudiar la formación del carbanión, así como estudiar su vida útil, lo que no solo puede mostrar que la reacción es un mecanismo E1cB de dos pasos (en oposición al mecanismo E2 concertado), sino que también puede abordar la vida útil y estabilidad de la estructura del estado de transición que puede distinguir aún más entre los tres tipos diferentes de mecanismos E1cB. [8]
Reacciones de Aldol [ editar ]
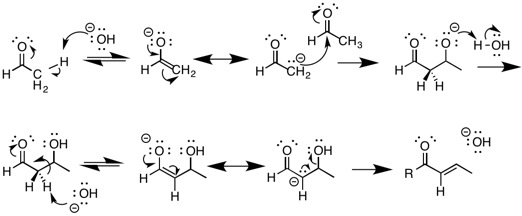
La reacción más conocida que sufre la eliminación de E1cB es la reacción de condensación de aldol en condiciones básicas. Esto implica la desprotonación de un compuesto que contiene un grupo carbonilo que da como resultado la formación de un enolato . El enolato es la base conjugada muy estable del material de partida y es uno de los intermedios en la reacción. Este enolato actúa entonces como nucleófilo y puede atacar a un aldehído electrófilo. El producto Aldol se desprotona formando otro enolato seguido de la eliminación de agua en una reacción de deshidratación E1cB.. Las reacciones aldólicas son una reacción clave en la química orgánica porque proporcionan un medio para formar enlaces carbono-carbono, lo que permite la síntesis de moléculas más complejas. [9]
E1cB fotoinducido [ editar ]
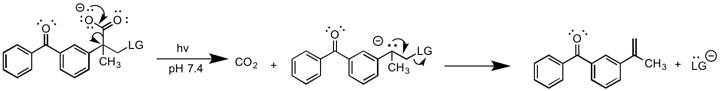
Lukeman et al. Han informado de una versión fotoquímica de E1cB . [10] En este informe, una reacción de descarboxilación inducida fotoquímicamente genera un carbanión intermedio, que posteriormente elimina el grupo saliente. La reacción es única de otras formas de E1cB ya que no requiere una base para generar el carbanión. El paso de formación de carbaniones es irreversible y, por lo tanto, debe clasificarse como E1cB irr .
En biología [ editar ]
La reacción de eliminación de E1cB es una reacción importante en biología. Por ejemplo, el penúltimo paso de la glucólisis implica un mecanismo E1cB. Este paso implica la conversión de 2-fosfoglicerato en fosfoenolpiruvato , facilitado por la enzima enolasa .




![La ley de velocidad y la velocidad observada para el mecanismo de eliminación de E1cB en el ejemplo anterior donde la base es etóxido. {\ displaystyle {\ begin {alineado} {\ frac {\ ce {d [P]}} {{\ ce {d}} t}} & = {\ frac {k_ {1} k_ {2} {\ ce {[sustrato] [base]}}} {k _ {- 1} [{\ ce {conjugate \ acid}}] + k_ {2}}} \\ {\ ce {rate}} & = k _ {\ ce { obs}} {\ ce {[sustrato] [base]}} \ end {alineado}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9fcaecea886d403f885d43b58cfb946af0778938)
No hay comentarios:
Publicar un comentario