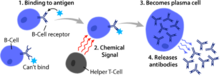
Las células B , también conocidas como linfocitos B , son un tipo de glóbulo blanco del subtipo de linfocitos . [1] Funcionan en la inmunidad humoral componente del sistema inmune adaptativo por secretoras de anticuerpos . [1] Además, las células B presentan antígeno (también se clasifican como células presentadoras de antígeno profesionales (APC) ) y secretan citoquinas . [1] En los mamíferos , las células B maduran en la médula ósea , que es el núcleo de la mayoríalos huesos . [2] En las aves, las células B maduran en la bolsa de Fabricio , un órgano linfoide. (La "B" de las células B proviene del nombre de este órgano , donde fue descubierto por primera vez por Chang y Glick, [2] y no por la médula ósea como se cree comúnmente).
Las células B, a diferencia de las otras dos clases de linfocitos, células Ty células asesinas naturales , expresan receptores de células B (BCR)en su membrana celular . [1] Los BCR permiten que las células B se unana un antígeno específico , contra el cual iniciará una respuesta de anticuerpos.
Desarrollo [ editar ]
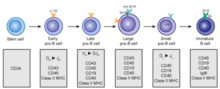
Las células B se desarrollan a partir de células madre hematopoyéticas (HSC) que se originan a partir de la médula ósea. [3] Las HSC primero se diferencian en células progenitoras multipotentes (MPP), luego en células progenitoras linfoides comunes (CLP). [3] A partir de aquí, su desarrollo en las células B se produce en varias etapas (que se muestran en la imagen de la derecha), cada una marcada por varios patrones de expresión génica y la cadena de inmunoglobulina H y los arreglos de loci génicos de la cadena L , esta última debido a las células B que experimentan V (D) J recombinación a medida que se desarrollan. [4]
Las células B se someten a dos tipos de selección mientras se desarrollan en la médula ósea para asegurar un desarrollo adecuado. La selección positiva se produce a través de la señalización independiente del antígeno que involucra tanto el pre-BCR como el BCR. [5] [6] Si estos receptores no se unen a su ligando, las células B no reciben las señales adecuadas y dejan de desarrollarse. [5] [6] La selección negativa se produce a través de la unión del autoantígeno con el BCR; Si el BCR puede unirse fuertemente al auto-antígeno, entonces la célula B experimenta uno de los cuatro destinos: eliminación clonal , edición del receptor , anergia o ignorancia (la célula B ignora la señal y continúa su desarrollo). [6]Este proceso de selección negativa conduce a un estado de tolerancia central , en el que las células B maduras no se unen con los antígenos propios presentes en la médula ósea. [4]
Para completar el desarrollo, las células B inmaduras migran de la médula ósea al bazo como células B de transición , pasando a través de dos etapas de transición: T1 y T2. [7] A lo largo de su migración al bazo y después de la entrada del bazo, se consideran células B T1. [8] Dentro del bazo, las células T1 B hacen la transición a las células T2 B. [8] Las células T2 B se diferencian en células B foliculares (FO) o en células de la zona marginal (MZ) dependiendo de las señales recibidas a través del BCR y otros receptores. [9] Una vez diferenciados, ahora se consideran células B maduras o células B ingenuas. [8]
Activación [ editar ]
La activación de las células B se produce en los órganos linfoides secundarios (SLO), como el bazo y los ganglios linfáticos . [1] Después de que las células B maduran en la médula ósea, migran a través de la sangre a los SLO, que reciben un suministro constante de antígeno a través de la linfa circulante . [10] En la SLO, la activación de las células B comienza cuando las células B se unen a un antígeno a través de su BCR. [11] Aunque los eventos que tienen lugar inmediatamente después de la activación aún no se han determinado completamente, se cree que las células B se activan de acuerdo con el modelo de segregación cinética [ cita requerida ], inicialmente determinado en linfocitos T. Este modelo indica que antes de la estimulación con antígeno, los receptores se difunden a través de la membrana al entrar en contacto con Lck y CD45 en igual frecuencia, lo que genera un equilibrio neto de fosforilación y no fosforilación. Es solo cuando la célula entra en contacto con una célula presentadora de antígeno que el CD45 más grande se desplaza debido a la distancia cercana entre las dos membranas. Esto permite la fosforilación neta del BCR y el inicio de la vía de transducción de señales [ cita requerida ] . De los tres subconjuntos de células B, las células FO B experimentan preferentemente la activación dependiente de células T, mientras que las células MZ B y las células B1 B experimentan preferentemente la activación independiente de células T. [12]
La activación de las células B se potencia a través de la actividad de CD21 , un receptor de superficie en complejo con las proteínas de superficie CD19 y CD81 (los tres se conocen colectivamente como el complejo correceptor de células B). [13] Cuando un BCR se une a un antígeno marcado con un fragmento de la proteína del complemento C3, CD21 se une al fragmento de C3, se co-une con el BCR unido, y las señales se transducen a través de CD19 y CD81 para disminuir el umbral de activación de la célula. [14] También se ha demostrado que CD20 se requiere directamente para la señalización de BCR en las células B, y los anticuerpos anti-CD20 utilizados terapéuticamente, tales como rituximab, eliminan principalmente las células B que tienen un alto potencial de activación de la vía de señalización de BCR. [15]
Recientemente se ha descrito que la señalización de BCR y la activación de células B se inhibe por la estabilización de p53 durante la respuesta de daño al ADN. [dieciséis]
Activación dependiente de células T [ editar ]
Los antígenos que activan las células B con la ayuda de las células T se conocen como antígenos dependientes de las células T (TD) e incluyen proteínas extrañas. [1] Se nombran como tales porque no pueden inducir una respuesta humoral en organismos que carecen de células T. [1] La respuesta de las células B a estos antígenos toma varios días, aunque los anticuerpos generados tienen una mayor afinidad y son más versátiles funcionalmente que los generados a partir de la activación independiente de las células T. [1]
Una vez que un BCR se une a un antígeno TD, el antígeno se recoge en la célula B a través de la endocitosis mediada por el receptor , se degrada y se presenta a las células T como piezas peptídicas en complejo con moléculas MHC-II en la membrana celular. [17] Las células T helper (T H ) , típicamente células foliculares T helper (T FH ) , que se activaron con el mismo antígeno reconocen y se unen a estos complejos de péptidos MHC-II a través de su receptor de células T (TCR) . [18] Tras la unión del péptido TCR-MHC-II, las células T expresan la proteína de superficie CD40L , así como las citoquinas como la IL-4 yIL-21 . [18] El CD40L sirve como un factor coestimulador necesario para la activación de los linfocitos B al unirse al receptor CD40 de la superficie de los linfocitos B , que promueve la proliferación de los linfocitos B , el cambio de clase de inmunoglobulina y la hipermutación somática , además de sostener el crecimiento y diferenciación de los linfocitos T. [1] Las citocinas derivadas de células T unidas por receptores de citocinas de células B también promueven la proliferación de células B, el cambio de clase de inmunoglobulina y la hipermutación somática, así como la diferenciación de las guías. [18] Después de que las células B reciben estas señales, se consideran activadas. [18]
Ahora activadas, las células B participan en un proceso de diferenciación de dos pasos que produce ambos plasmablastos de vida corta para una protección inmediata y células de plasma de larga vida y células B de memoria para una protección persistente. [12] El primer paso, conocido como la respuesta extrafolicular, ocurre fuera de los folículos linfoides pero aún en el SLO. [12] Durante este paso, las células B activadas proliferan, pueden sufrir un cambio de clase de inmunoglobulina y diferenciarse en plasmablastos que producen anticuerpos tempranos y débiles, principalmente de clase IgM. [19] El segundo paso consiste en células B activadas que ingresan a un folículo linfoide y forman un centro germinal (CG), que es un microentorno especializado donde las células B experimentan una proliferación extensa, cambio de clase de inmunoglobulina y maduración de afinidaddirigida por hipermutación somática. [20] Estos procesos son facilitados por las células T FH dentro del GC y generan tanto células B de memoria de alta afinidad como células plasmáticas de larga vida. [12] Las células plasmáticas resultantes secretan grandes cantidades de anticuerpos y permanecen dentro del SLO o, más preferiblemente, migran a la médula ósea. [20]
Activación independiente de células T [ editar ]
Los antígenos que activan las células B sin la ayuda de las células T se conocen como antígenos independientes de las células T (TI) [1] e incluyen polisacáridos extraños y ADN CpG no metilado. [12] Se nombran como tales porque son capaces de inducir una respuesta humoral en organismos que carecen de células T. [1] La respuesta de las células B a estos antígenos es rápida, aunque los anticuerpos generados tienden a tener una menor afinidad y son menos versátiles funcionalmente que los generados a partir de la activación dependiente de las células T. [1]
Al igual que con los antígenos TD, las células B activadas por los antígenos TI necesitan señales adicionales para completar la activación, pero en lugar de recibirlas de las células T, se proporcionan mediante el reconocimiento y la unión de un componente microbiano común a los receptores tipo toll (TLR) o mediante La reticulación extensa de BCR a epítopes repetidos en una célula bacteriana. [1] Las células B activadas por los antígenos de TI continúan proliferando fuera de los folículos linfoides, pero aún en SLO (GCs no se forman), posiblemente experimentan un cambio de clase de inmunoglobulina, y se diferencian en plasmablastos de corta duración que producen anticuerpos tempranos y débiles principalmente de IgM de clase , pero también algunas poblaciones de células plasmáticas de larga vida. [21]
Activación de células de memoria B [ editar ]
La activación de las células B de memoria comienza con la detección y unión de su antígeno objetivo, que es compartido por su célula B principal. [22] Algunas células B de memoria pueden activarse sin ayuda de células T, como ciertas células B de memoria específicas de virus, pero otras necesitan ayuda de células T. [23] Tras la unión al antígeno, la célula B de memoria absorbe el antígeno a través de la endocitosis mediada por el receptor, la degrada y la presenta a las células T como piezas peptídicas en complejo con moléculas MHC-II en la membrana celular. [22] Las células T auxiliares de memoria (T H ), típicamente las células T auxiliares foliculares de memoria (T FH ), que se derivaron de las células T activadas con el mismo antígeno, reconocen y se unen a estos complejos de péptidos MHC-II a través de su TCR. [22]Después de la unión del péptido TCR-MHC-II y el relevo de otras señales de la célula T FH de la memoria, la célula B de la memoria se activa y se diferencia en plasmablastos y células plasmáticas a través de una respuesta extrafolicular o ingresa en una reacción del centro germinal donde generan plasma Células y más células B de memoria. [22] [23] No está claro si las células B de memoria experimentan una maduración de afinidad adicional dentro de estos GC secundarios. [22]
Tipos de células B [ editar ]
- Plasmablast: célula de proliferación de anticuerpos de corta duración y proliferación que surge de la diferenciación de las células B. [1] Los plasmablastos se generan temprano en una infección y sus anticuerpos tienden a tener una afinidad más débil hacia su antígeno objetivo en comparación con las células plasmáticas. [12] Los plasmablastos pueden ser el resultado de la activación de células B independiente de células T o la respuesta extrafolicular de la activación de células B dependiente de células T. [1]
- Célula plasmática: una célula de proliferación de anticuerpos no proliferativa de larga vida que surge de la diferenciación de las células B. [1] Hay evidencia de que las células B primero se diferencian en una célula similar a un plasmablasto, luego se diferencian en una célula plasmática. [12] Las células plasmáticas se generan más tarde en una infección y, en comparación con los plasmablastos, tienen anticuerpos con una mayor afinidad hacia su antígeno objetivo debido a la maduración de la afinidad en el centro germinal (GC) y producen más anticuerpos. [12] Las células plasmáticas generalmente resultan de la reacción del centro germinal de la activación de las células B dependiente de las células T, sin embargo, también pueden resultar de la activación de las células B independiente de las células T. [21]
- Célula linfoplasmocitoide: una célula con una mezcla de linfocitos B y características morfológicas de las células plasmáticas que se cree que está estrechamente relacionada o es un subtipo de células plasmáticas. Este tipo de células se encuentra en discrasias de células plasmáticas pre-malignas y malignas que están asociadas con la secreción de proteínas monoclonales IgM ; estas discrasias incluyen gammapatía monoclonal IgM de importancia indeterminada y macroglobulinemia de Waldenström . [24]
- Células B de memoria: células B inactivas que surgen de la diferenciación de células B. [1] Su función es circular a través del cuerpo e iniciar una respuesta de anticuerpos más fuerte y más rápida (conocida como respuesta de anticuerpos secundarios anamnésicos) si detectan el antígeno que había activado sus células B primarias (células B de memoria y sus células B primarias) comparten el mismo BCR, por lo que detectan el mismo antígeno). [23] Las células B de memoria pueden generarse a partir de la activación dependiente de las células T a través de la respuesta extrafolicular y la reacción del centro germinal, así como a partir de la activación de las células B independientes de las células T. [23]
- Células B-2 - células B FO y células B MZ. [25]
- Célula B folicular (FO) (también conocida como célula B-2): el tipo más común de célula B y, cuando no circula a través de la sangre, se encuentra principalmente en los folículos linfoides de los órganos linfoides secundarios (SLO). [12] Son responsables de generar la mayoría de los anticuerpos de alta afinidad durante una infección. [1]
- Célula marginal de la zona (MZ) B : se encuentra principalmente en la zona marginal del bazo y sirve como primera línea de defensa contra los patógenos transmitidos por la sangre, ya que la zona marginal recibe grandes cantidades de sangre de la circulación general. [26] Pueden someterse a activación independiente tanto de células T como dependientes de células T, pero preferentemente a una activación independiente de células T. [12]
- Célula B-1 : surge de una vía de desarrollo diferente de las células FO B y las células B MZ. [25] En ratones, predominantemente pueblan la cavidad peritoneal y la cavidad pleural , generan anticuerpos naturales(anticuerpos producidos sin infección), se defienden contra patógenos de la mucosa y exhiben principalmente activación de células T independientes. [25] No se ha descubierto un verdadero homólogo de células B-1 de ratón en humanos, aunque se han descrito varias poblaciones de células similares a las células B-1. [25]
- Células B reguladoras (Breg) : un tipo de célula B inmunosupresora que detiene la expansión de los linfocitos proinflamatorios patógenos a través de la secreción de IL-10, IL-35 y TGF-β. [27] Además, promueve la generación de células T (Treg) reguladoras al interactuar directamente con las células T para sesgar su diferenciación hacia las Treg. [27] No se ha descrito una identidad de célula Breg común y se han encontrado muchos subconjuntos de células Breg que comparten funciones reguladoras tanto en ratones como en humanos. [27] Actualmente se desconoce si los subconjuntos de células Breg están vinculados al desarrollo y cómo se produce la diferenciación exacta en una célula Breg. [27]Existe evidencia que muestra que casi todos los tipos de células B pueden diferenciarse en una célula Breg a través de mecanismos que involucran señales inflamatorias y reconocimiento de BCR. [27]
[ editar ]
La enfermedad autoinmune puede resultar del reconocimiento anormal de células B de autoantígenos seguido de la producción de autoanticuerpos. [28] Las enfermedades autoinmunes en las que la actividad de la enfermedad se correlaciona con la actividad de las células B incluyen la esclerodermia , la esclerosis múltiple , el lupus eritematoso sistémico , la diabetes tipo 1 y la artritis reumatoide . [28]
La transformación maligna de las células B y sus precursores puede causar una serie de tipos de cáncer , incluyendo leucemia linfocítica crónica (CLL) , leucemia linfoblástica aguda (ALL) , leucemia de células pilosas , linfoma folicular , linfoma no Hodgkin , linfoma de Hodgkin , y neoplasias malignas de células plasmáticas tales como mieloma múltiple , macroglobulinemia de Waldenström y ciertas formas de amiloidosis . [29] [30]
Epigenética [ editar ]
Un estudio que investigó el metiloma de las células B a lo largo de su ciclo de diferenciación, utilizando la secuenciación de bisulfito de genoma completo (WGBS), mostró que existe una hipometilación desde las etapas más tempranas hasta las etapas más diferenciadas. La mayor diferencia de metilación es entre las etapas de las células B del centro germinal y las células B de la memoria. Además, este estudio demostró que existe una similitud entre los tumores de células B y las células B de larga duración en sus firmas de metilación de ADN .



No hay comentarios:
Publicar un comentario