Reacción química
1. Reacción química
Recordemos los tipos de cambios que experimenta la materia, pueden ser de dos tipos:
- Cambios físicos: son aquellos en los que no se altera la naturaleza (composición) de la sustancia que cambia. Por ejemplo: los cambios de estado.
- Cambios químicos: son aquellos en los que si se altera la naturaleza (composición) de la sustancia que cambia. Por ejemplo: una oxidación.
Todo cambio químico tiene lugar a través de una reacción química. Una reacción química es un proceso por el que una sustancia inicial, llamada "reactivo", se transforma en otra distinta llamada "producto".
Las reacciones químicas se representan mediante ecuaciones químicas, en el primer miembro escribiremos los reactivos y en el segundo miembro los productos.
Reactivos → Productos
HCl + Zn → ZnCl2 + H2
Así vemos que la reacción anterior presenta como reactivos el cloruro de hidrógeno y el cinc, y como productos, hidrógeno y cloruro de zinc. Se puede leer de la siguiente forma: el cloruro de hidrógeno reacciona con el zinc para dar lugar a hidrógeno y cloruro de zinc.
En ocasiones resulta recomendable expresar el estado de agregación en el que se encuentran las sustancias participantes en la reacción, para ello utilizaremos los siguientes subíndices:
(s) → estado sólido
(l) → estado líquido
(g) → estado gaseoso
(dis) → en disolución
Por ejemplo:
Carbonato cálcico (S) → óxido cálcico (S) + dióxido de carbono (g)
CaCO3 (S) →CaO (S) + CO2 (g)
Vemos como el carbonato de calcio en estado sólido se descompone para dar lugar a óxido de calcio sólido y dióxido de carbono gaseoso.
1.1 Ajuste de reacción química
De acuerdo con la Teoría atómica de Dalton, en las reacciones químicas los átomos ni se crean ni se destruyen, por lo tanto debe existir el mismo número de átomos de cada elemento en los reactivos y en los productos.
Sin embargo, en ocasiones vemos que el número de partículas no coincide con el resultado final de la fórmula.
Esto se debe a que las moléculas no tienen por qué reaccionar 1:1, sino que pueden reaccionar en otra proporción. Para ello ajustaremos la reacción asignando números, llamados coeficientes estequiométricos, delante de cada sustancia participante hasta comprobar que el número de átomos coincide.
Por ejemplo: el metano reacciona con el oxígeno gaseoso para dar lugar dióxido de carbono y agua.
Si escribimos la ecuación, tal cual, vemos que no coinciden el número de partículas del producto con el de los reactivos.
Obtenemos:

Reactivos:
1 átomo de carbono
2 átomos de oxígeno
4 átomos de hidrógeno
Productos:
1 átomo de carbono
3 átomos de oxígeno
2 átomos de hidrógeno
Aplicando el ajuste tenemos (observa el número "2" que agregamos delante de O2 y H2O, es el coeficiente estequiométrico):
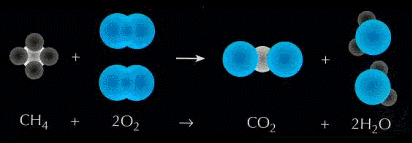
Reactivos:
1 átomo de carbono
4 átomos de oxígeno
4 átomos de hidrógeno
Productos:
1 átomo de carbono
4 átomos de oxígeno
4 átomos de hidrógeno
El número de partículas de productos coincide con el de reactivos.
http://www.aulafacil.com
LAS REACCIONES QUÍMICAS
|
1.- LOS CAMBIOS EN LA MATERIA
La materia puede sufrir cambios mediante diversos procesos. No obstante, todos esos cambios se pueden agrupar en dos tipos: cambios físicos y cambios químicos.
1.1- CAMBIOS FÍSICOS
En estos cambios no se producen modificaciones en la naturaleza de las sustancia o sustancias que intervienen. Ejemplos de este tipo de cambios son:
- Cambios de estado.
- Mezclas.
- Disoluciones.
- Separación de sustancias en mezclas o disoluciones.
1.2- CAMBIOS QUÍMICOS
En este caso, los cambios si alteran la naturaleza de las sustancias: desaparecen unas y aparecen otras con propiedades muy distintas. No es posible volver atrás por un procedimiento físico (como calentamiento o enfriamiento, filtrado, evaporación, etc.)
Una reacción química es un proceso por el cual una o más sustancias, llamadas reactivos, se transforman en otra u otras sustancias con propiedades diferentes, llamadas productos.
En una reacción química, los enlaces entre los átomos que forman los reactivos se rompen. Entonces, los átomos se reorganizan de otro modo, formando nuevos enlaces y dando lugar a una o más sustancias diferentes a las iniciales.
2.- CARACTERÍSTICAS DE LAS REACCIONES QUÍMICAS
- La o las sustancias nuevas que se forman suelen presentar un aspecto totalmente diferente del que tenían las sustancias de partida.
- Durante la reacción se desprende o se absorbe energía:
- Reacción exotérmica: se desprende energía en el curso de la reacción.
- Reacción endotérmica: se absorbe energía durante el curso de la reacción.
- Se cumple la ley de conservación de la masa: la suma de las masas de los reactivos es igual a la suma de las masas de los productos. Esto es así porque durante la reacción los átomos ni aparecen ni desaparecen, sólo se reordenan en una disposición distinta.
3.- ECUACIONES QUÍMICAS
Una reacción química se representa mediante una ecuación química. Para leer o escribir una ecuación química, se deben seguir las siguientes reglas:
- Las fórmulas de los reactivos se escriben a la izquierda, y las de los productos a la derecha, separadas ambas por una flecha que indica el sentido de la reacción.
- A cada lado de la reacción, es decir, a derecha y a izquierda de la flecha, debe existir el mismo número de átomos de cada elemento.
Nota: estos coeficientes situados delante de las fórmulas, son los únicos números en la ecuación que se pueden cambiar, mientras que los números que aparecen dentro de las fórmulas son intocables, pues un cambio en ellos significa un cambio de sustancia que reacciona y, por tanto, se trataría de una reacción distinta.
Si se quiere o necesita indicar el estado en que se encuentran las sustancias que intervienen o si se encuentran en disolución, se puede hacer añadiendo los siguientes símbolos detrás de la fórmula química correspondiente:
- (s) = sólido.
- (metal) = elemento metálico.
- (l) = líquido.
- (g) = gas.
- (aq) = disolución acuosa (en agua).
- Ajustar reacciones químicas 1 (con ejercicios)
- Ajustar reacciones químicas 2
4.- CÁLCULO DE LA MASA Y EL VOLUMEN A PARTIR DE ECUACIONES QUÍMICAS
Las ecuaciones químicas permiten calcular, a partir de una cantidad determinada de alguno de los reactivos y productos que intervienen en una reacción, la cantidad necesaria del resto de los componentes de la misma.
4.1- Cálculos masa - masa
En este caso nos aprovechamos de la relación que hay entre cantidad de sustancia (en mol), masa de sustancia y masa molar, tal como indica la relación:
| cantidad de sustancia = | masa en gramos | ; n (mol) = | m(g) |
| masa molar | M (g/mol) |
Se quiere calcular la cantidad de cloruro de calcio que se obtiene cuando 50 g de carbonato de calcio se hacen reaccionar con la cantidad suficiente de ácido clorhídrico, en una reacción en la que se obtienen, además, agua y dióxido de carbono
|
La ley de Avogadro dice lo siguiente:
Volumenes iguales de diferentes gases en las mismas condiciones de presión y temperatura, contienen el mismo número de partículas
|
Al igual que en el caso anterior, pulsa sobre el gráfico para ver cómo se plantea y soluciona un problema de este tipo:
Aquí tienes un par de actividades para practicar ambos tipos de cálculos:
5.- VELOCIDAD DE UNA REACCIÓN QUÍMICA
Para saber si una reacción es rápida o lenta, hay que conocer la velocidad a la que transcurre. Podemos definir velocidad de reacción como la variación de cantidad de sustancia formada o transformada por unidad de tiempo.
En general, para determinar la velocidad de una reacción, hay que medir la cantidad de reactivo que desaparece o la cantidad de producto que se forma por unidad de tiempo.
5.1- Factores que afectan a la velocidad de reacción
la velocidad de una reacción se ve influida por una serie de factores; entre ellos se pueden destacar:
Naturaleza de los reactivos
Se ha observado que según los reactivos que intervengan, las reacciones tienen distinta velocidad, pero no se ha podido establecer aún unas reglas generales.
Concentración de los reactivos
La velocidad de reacción aumenta con la concentración de los reactivos. Para aumentar la concentración de un reactivo:
- Si es un gas, se consigue elevando su presión.
- Si se encuentra en disolución, se consigue cambiando la relación entre el soluto y el disolvente.
Superficie de contacto de los reactivos
Cuanto más divididos están los reactivos, más rápida es la reacción. Esto es así porque se aumenta la superficie expuesta a la misma.
Temperatura
En general, la velocidad de una reacción química aumenta conforme se eleva la temperatura.
Presencia de catalizadores
Un catalizador es una sustancia, distinta a los reactivos o los productos, que modifican la velocidad de una reacción. Al final de la misma, el catalizador se recupera por completo e inalterado. En general, hace falta muy poca cantidad de catalizador.
Los catalizadores aumentan la velocidad de la reacción, pero no la cantidad de producto que se forma.
6.- IMPORTANCIA DE LAS REACCIONES QUÍMICAS
Estamos rodeados por reacciones químicas; tienen lugar en laboratorios, pero también en fábricas, automóviles, centrales térmicas, cocinas, atmósfera, interior de la Tierra... Incluso en nuestro cuerpo ocurren miles de reacciones químicas en cada instante, que determinan lo que hacemos y pensamos.
De toda la variedad de reacciones posibles, vamos a ver dos: las de neutralización y las de combustión. Pero antes de verlas, es necesario conocer y dominar el concepto de ácido y base.
6.1- Ácidos y bases
Las características de los ácidos y las bases se resumen en el siguiente cuadro:
| Ácidos | Bases | |
| ▪Tienen sabor agrio (ácido). | ▪Tienen sabor amargo. | |
| ▪Reaccionan con ciertos metales, como Zn, Mg o Fe, para dar hidrógeno | ▪Reaccionan con las grasas para dar jabones. | |
| ▪Reaccionan con las bases para dar sales | ▪Reaccionan con los ácidos para dar sales. | |
| Son sustancias ácidas: el ácido clorhídrico (HCl); el ácido bromhídrico (HBr); el ácido nítrico (HNO3); el ácido carbónico (H2CO3) y el ácido sulfúrico (H2SO4), entre otros | Son sustancias básicas el hidróxido de amonio o amoniaco disuelto en agua (NH4OH); y los hidróxidos de los metales alcalinos (LiOH, NaOH, KOH,...) y alcalinotérreos, como el Ca(OH)2, y Mg(OH)2, entre otros |
- Si una sustancia tiene un pH igual a 7, se dice que es neutra, ni ácida ni básica (por ejemplo, el agua pura).
- Si una sustancia tiene un pH menor que 7, tiene carácter ácido.
- Si una sustanica tien un pH mayor que 7, tiene carácter básico.
| Indicadores | Color en medio ácido | Color en medio básico | |
| Naranja de metilo | Naranja | Amarillo | |
| Fenolftaleina | Incoloro | Rosa | |
| Azul de bromotimol | Amarillo | Azul | |
| Tornasol | Rojo | Azul |
Para ahorrar tiempo y trabajo, se utiliza mucho el papel indicador universal, que es un papel impregnado con una mezcla de indicadores y que adquiere un color distinto según los distintos pH.
http://www.quimicaweb.net/grupo_trabajo_fyq3/tema6/index6.htm
No hay comentarios:
Publicar un comentario