Los carotenoides ( / k ə r ɒ t ɪ n ɔɪ d / ), también llamados tetraterpenoids , son de color amarillo, naranja y rojo orgánicos pigmentos que son producidos por las plantas y algas, así como varias bacterias y hongos. [1] Los carotenoides dan el color característico a calabazas , zanahorias , maíz , tomates , canarios , flamencos y narcisos. [1]Todos estos organismos pueden producir carotenoides a partir de grasas y otros componentes básicos metabólicos orgánicos orgánicos. Los únicos animales que se sabe que producen carotenoides son áfidosy ácaros , que adquirieron la capacidad y los genes de los hongos [2] [3] [4] o son producidos por bacterias endosimbióticas en las moscas blancas. [5] Los carotenoides de la dieta se almacenan en los tejidos grasos de los animales, [1] y los animales exclusivamente carnívoros obtienen los compuestos de la grasa animal. En la dieta humana, la absorción de carotenoides mejora cuando se consume con grasa en una comida. [6] Cocinar vegetales que contienen carotenoides en aceite aumenta el carotenoidebiodisponibilidad . [1] [6]
Hay más de 1.100 carotenoides conocidos [7] que pueden clasificarse en dos clases, las xantofilas (que contienen oxígeno) y los carotenos (que son puramente hidrocarburos y no contienen oxígeno). [1] Todos son derivados de tetraterpenos , lo que significa que se producen a partir de 8 moléculas de isopreno y contienen 40 átomos de carbono. En general, los carotenoides absorben longitudes de onda que van desde 400–550 nanómetros (luz violeta a verde). Esto hace que los compuestos sean de color amarillo, naranja o rojo. Los carotenoides son el pigmento dominante en la coloración de las hojas de otoño de aproximadamente el 15-30% de las especies de árboles, [1]pero muchos colores de plantas, especialmente los rojos y púrpuras, se deben a los polifenoles .
Los carotenoides cumplen dos funciones clave en las plantas y las algas: absorben la energía de la luz para su uso en la fotosíntesis y protegen la clorofila del fotodaño. [8] Los carotenoides que contienen anillos de beta-ionona no sustituidos (incluidos el betacaroteno , el alfa-caroteno , la beta- criptoxantina y el gamma-caroteno ) tienen actividad de la vitamina A (lo que significa que pueden convertirse en retinol ). En el ojo, la luteína , la meso-zeaxantina y la zeaxantina están presentes como pigmentos maculares cuya importancia en la función visual permanece bajo investigación clínica a partir de 2016.[1] [9] No hay pruebas suficientes para afirmar que los carotenoides tengan unafunciónantioxidante en los seres humanos o que los suplementos dietéticos decarotenoides reduzcan el riesgo o prevengan enfermedades.
Biosíntesis [ editar ]
Los componentes básicos de los carotenoides son el difosfato de isopentenilo (IPP) y el difosfato de dimetilalilo (DMAPP). [10] Estos dos isómeros de isopreno se utilizan para crear varios compuestos dependiendo de la ruta biológica utilizada para sintetizar los isómeros. [11] Se sabe que las plantas usan dos vías diferentes para la producción de IPP: la vía del ácido mevalónico citosólico (MVA) y el metileritritol 4-fosfato plastídico (MEP). [10] En animales, la producción de colesterol comienza creando IPP y DMAPP utilizando el MVA. [11] Para las plantas de producción de carotenoides, use MEP para generar IPP y DMAPP. [10]La ruta MEP da como resultado una mezcla 5: 1 de IPP: DMAPP. [11]El IPP y el DMAPP experimentan varias reacciones, lo que resulta en el principal precursor de carotenoides, el geranilgeranil difosfato (GGPP). El GGPP se puede convertir en carotenos o xantofilas si se realizan varios pasos diferentes dentro de la ruta biosintética de los carotenoides. [10]
Vía MEP [ editar ]
El gliceraldehído 3-fosfato y el piruvato , intermedios de la fotosíntesis , se convierten en 5-fosfato de desoxi-D-xilulosa (DXP) utilizando el catalizador DXP sintasa (DXS). La DXP reductoisomerasa reduce y reorganiza las moléculas dentro de DXP [10] en presencia de NADPH , [11] formando MEP. [10] A continuación, la MEP se convierte en 4- (citidina 5'-difosfos) -2-C-metil-D-eritritol (CDP-ME) en presencia de CTP a través de la enzima MEP citidililtransferasa. CDP-ME se convierte entonces, en presencia de ATP, a 2-fosfo-4- (citidina 5'-difosfo) -2-C-metil-D-eritritol (CDP-ME2P). La conversión a CDP-ME2P es catalizada por la enzima CDP-ME quinasa . A continuación, el CDP-ME2P se convierte en 2,4-ciclodifosfato de 2-C-metil-D-eritritol (MECDP). Esta reacción se produce cuando la MECDP sintasa cataliza la reacción y la CMP se elimina de la molécula CDP-ME2P. El MECDP se convierte luego en (e) -4-hidroxi-3-metilbut-2-en-1-ilfosfato (HMBDP) a través de la HMBDP sintasa en presencia de flavodoxina y NADPH. HMBDP se reduce a IPP en presencia de ferredoxina y NADPH por la enzima HMBDP reductasa . Los dos últimos pasos que involucran la HMBPD sintasa y la reductasa solo pueden ocurrir de forma completamente anaeróbica.ambientes El IPP puede entonces isomerizar a DMAPP a través de la isomerasa de IPP. [11]
Carotenoides ruta biosintética [ editar ]
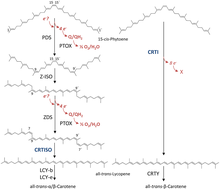
Dos moléculas de GGPP se condensan a través de la fitoeno sintasa(PSY), formando el isómero 15-cis de fitoeno . La conversión subsiguiente en todo el transcopopeno depende del organismo. Las bacterias y los hongos emplean una sola enzima, la fitoeno desaturasa(CRTI) bacteriana para la catálisis. Las plantas y las cianobacterias, sin embargo, utilizan cuatro enzimas para este proceso. [12] La primera de estas enzimas es una fitoeno desaturasa de tipo vegetal que introduce dos enlaces dobles adicionales en el 15-cis-fitoeno por deshidrogenacióne isomeriza dos de sus enlaces dobles existentes de trans a cisproduciendo 9,15,9'-tri-cis-ζ-caroteno. El doble enlace central de este tri-cis-ζ-caroteno es isomerizado por la zeta-caroteno isomerasa Z-ISO y el 9,9'-di-cis-ot-caroteno resultante se deshidrogenó nuevamente a través de una atur-caroteno desaturasa (ZDS ) . Esto nuevamente introduce dos dobles enlaces, lo que resulta en 7,9,7 ', 9'-tetra-cis-licopeno. CRTISO , una carotenoide isomerasa, es necesaria para convertir el cis -copopeno en un licopeno totalmente trans en presencia de FAD reducido .
Este licopeno todo trans es ciclado; La ciclación da lugar a la diversidad de carotenoides, que se puede distinguir en función de los grupos finales. Puede haber un anillo beta o un anillo épsilon, cada uno generado por una enzima diferente ( licopeno beta-ciclasa [beta-LCY] o licopeno épsilon-ciclasa [épsilon-LCY]). El alfa-caroteno se produce cuando el licopeno todo trans experimenta por primera vez una reacción con épsilon-LCY y luego una segunda reacción con un beta-LCY; mientras que el betacaroteno es producido por dos reacciones con beta-LCY. El alfa y el betacaroteno son los carotenoides más comunes en los fotosistemas de la planta.pero aún pueden convertirse más en xantofilas usando beta-hidrolasa y épsilon-hidrolasa, lo que lleva a una variedad de xantofilas. [10]
Reglamento [ editar ]
Se cree que tanto el DXS como el DXR son enzimas determinantes de la velocidad, lo que les permite regular los niveles de carotenoides. [10] Esto se descubrió en un experimento en el que DXS y DXR estaban sobreexpresados genéticamente, lo que llevó a un aumento de la expresión de carotenoides en las plántulas resultantes. [10] Además, se piensa que las chaperonas de la proteína J (J20) y la proteína de choque térmico 70 (Hsp70) están involucradas en la regulación postranscripcional de la actividad de DXS, de modo que los mutantes con actividad J20 defectuosa exhiben una actividad enzimática DXS reducida mientras acumulan DXS inactivo proteína. [13] La regulación también puede ser causada por toxinas externas que afectan las enzimas y proteínas requeridas para la síntesis. La ketoclomazona se deriva de los herbicidas.Se aplica al suelo y se une a la DXP sintasa. [11] Esto inhibe la DXP sintasa, previniendo la síntesis de DXP y deteniendo la vía MEP. [11] El uso de esta toxina conduce a niveles más bajos de carotenoides en plantas cultivadas en el suelo contaminado. [11] La fosmidomicina , un antibiótico , es un inhibidor competitivo de la DXP reductoisomerasa debido a su estructura similar a la de la enzima. [11] La aplicación de dicho antibiótico previene la reducción de DXP, deteniendo nuevamente la vía MEP. [11]
Estructura y función [ editar ]
La estructura de los carotenoides imparte habilidades biológicas, incluida la fotosíntesis , la fotoprotección , la coloración de las plantas y la señalización celular .
La estructura general del carotenoide es una cadena de polieno que consiste en 9-11 enlaces dobles y posiblemente termina en anillos. Esta estructura de dobles enlaces conjugados conduce a un alto potencial reductor, o la capacidad de transferir electrones a través de la molécula. [14] Los carotenoides pueden transferir electrones de una de dos maneras: 1) transferencia de singlete a singlete de carotenoide a clorofila , y 2) transferencia de triplete a triplete de clorofila a carotenoide. La transferencia singlet-singlet es una transferencia de estado de energía más baja y se utiliza durante la fotosíntesis. [15]La longitud de la cola de polieno permite la absorción de luz en el rango fotosintético; una vez que absorbe energía, se excita, luego transfiere los electrones excitados a la clorofila para la fotosíntesis. [14] La transferencia de triplete a triplete es un estado de mayor energía y es esencial en la fotoprotección. [15] Tanto la luz como el oxígeno producen especies dañinas durante la fotosíntesis, siendo las especies de oxígeno reactivas (ROS) las más dañinas . A medida que estos ROS de alta energía se producen en la clorofila, la energía se transfiere a la cola de polieno del carotenoide y experimenta una serie de reacciones en las cuales los electrones se mueven entre los enlaces carotenoides para encontrar el estado más equilibrado (estado de energía más baja) para el carotenoide. [14]
La longitud de los carotenoides también tiene un papel en la coloración de la planta, ya que la longitud de la cola de polieno determina qué longitudes de onda de la luz absorberá la planta. Las longitudes de onda que no se absorben se reflejan y son lo que vemos como el color de una planta. [14] Por lo tanto, las diferentes especies contendrán carotenoides con diferentes longitudes de cola que les permiten absorber y reflejar diferentes colores. [14]
Los carotenoides también participan en diferentes tipos de señalización celular. [15] Son capaces de señalar la producción de ácido absicísico , que regula el crecimiento de las plantas, la latencia de las semillas , la maduración y germinación de los embriones , la división y elongación celular , el crecimiento floral y las respuestas al estrés. [dieciséis]
Propiedades [ editar ]
Los carotenoides pertenecen a la categoría de tetraterpenoides (es decir, contienen 40 átomos de carbono, y se construyen a partir de cuatro unidades de terpeno que contienen 10 átomos de carbono). Estructuralmente, los carotenoides toman la forma de una cadena de hidrocarburo de polieno que a veces termina con anillos, y puede o no tener átomos de oxígeno adicionales unidos.
- Los carotenoides con moléculas que contienen oxígeno, como la luteína y la zeaxantina , se conocen como xantofilas .
- Los carotenoides no oxigenados (sin oxígeno) como el α-caroteno , el β-caroteno y el licopeno , se conocen como carotenos . Los carotenos típicamente contienen solo carbono e hidrógeno (es decir, son hidrocarburos ) y están en la subclase de hidrocarburos insaturados .
Su color, desde amarillo pálido hasta naranja brillante y rojo intenso, está directamente vinculado a su estructura. Las xantofilas son a menudo amarillas, de ahí su nombre de clase. Los dobles enlaces carbono-carbono interactúan entre sí en un proceso llamado conjugación , que permite que los electrones en la molécula se muevan libremente a través de estas áreas de la molécula. A medida que aumenta el número de dobles enlaces conjugados, los electrones asociados con los sistemas conjugados tienen más espacio para moverse y requieren menos energía para cambiar de estado. Esto hace que el rango de energías de la luz absorbida por la molécula disminuya. A medida que se absorben más longitudes de onda de la luz desde el extremo más largo del espectro visible, los compuestos adquieren un aspecto cada vez más rojo.
Los carotenoides suelen ser lipófilos debido a la presencia de largas cadenas alifáticas insaturadas como en algunos ácidos grasos . La absorción fisiológica de estas vitaminas liposolubles en humanos y otros organismos depende directamente de la presencia de grasas y sales biliares . [1]
Alimentos [ editar ]
El betacaroteno , que se encuentra en las calabazas , batatas , zanahorias y calabazas de invierno , es responsable de sus colores amarillo anaranjado. [1] Las zanahorias secas tienen la mayor cantidad de caroteno de cualquier alimento por porción de 100 gramos, medida en equivalentes de actividad de retinol (equivalentes de provitamina A). [17] La fruta gac vietnamita contiene la concentración más alta conocida del caropinoide licopeno . [18] Aunque verde, la col rizada , la espinaca , col rizada , y hojas de nabo contienen cantidades sustanciales de beta-caroteno.[1] La dieta de los flamencos es rica en carotenoides, impartiendo las plumas de color naranja de estas aves. [19]
Efectos fisiológicos [ editar ]
Las revisiones de los estudios epidemiológicos que buscan correlaciones entre el consumo de carotenoides en los alimentos y los resultados clínicos han llegado a varias conclusiones:
- Una revisión de 2016 que analiza las correlaciones entre las dietas ricas en frutas y verduras (algunas de las cuales son altas en carotenoides) y el cáncer de pulmón encontró un efecto protector de hasta 400 g / día. [20]
- Una revisión de 2015 encontró que los alimentos ricos en carotenoides parecen ser protectores contra los cánceres de cabeza y cuello . [21]
- Otra revisión de 2015 que analiza si los caretenoides pueden prevenir el cáncer de próstata encontró que aunque varios estudios encontraron que las correlaciones entre las dietas ricas en carotenoides parecen tener un efecto protector, faltan pruebas para determinar si esto se debe a los carotenoides en sí. [22]
- Una revisión de 2014 no encontró correlación entre el consumo de alimentos ricos en carotenoides y vitamina A y el riesgo de contraer la enfermedad de Parkinson . [23]
- Otra revisión de 2014 no encontró resultados contradictorios en los estudios de consumo de carotenoides en la dieta y el riesgo de contraer cáncer de mama . [24]
Los carotenoides también son componentes importantes de la melanina , pigmento marrón oscuro , que se encuentra en el cabello, la piel y los ojos. La melanina absorbe la luz de alta energía y protege estos órganos del daño intracelular.
- Varios estudios han observado los efectos positivos de las dietas altas en carotenoides sobre la textura, claridad, color, fuerza y elasticidad de la piel. [25] [26] [27]
- Un estudio de 1994 observó que las dietas altas en carotenoides ayudaron a reducir los síntomas de la fatiga visual (ojo seco, dolores de cabeza y visión borrosa) y mejoraron la visión nocturna. [28] [29]
Los humanos y otros animales son en su mayoría incapaces de sintetizar carotenoides, y deben obtenerlos a través de su dieta. Los carotenoides son una característica común y con frecuencia ornamental en los animales. Por ejemplo, el color rosa del salmón y la coloración roja de las langostas cocidas y las escamas del color amarillo de las lagartijas comunes se deben a los carotenoides. [30] [ citación necesitada ] Se ha propuesto que los carotenoides se usan en rasgos ornamentales (para ejemplos extremos, véanse las aves frailecillos ) porque, dadas sus propiedades fisiológicas y químicas, pueden usarse como indicadores visibles de salud individual y, por lo tanto, se usan Por los animales al seleccionar compañeros potenciales.[31]
Colores de plantas [ editar ]
Los carotenoides más comunes incluyen el licopeno y el precursor de la vitamina A β-caroteno. En las plantas, la luteína xantofila es el carotenoide más abundante y su papel en la prevención de enfermedades oculares relacionadas con la edad está actualmente bajo investigación. [9] La luteína y los otros pigmentos carotenoides que se encuentran en las hojas maduras a menudo no son evidentes debido a la presencia de enmascaramiento de clorofila . Cuando no hay clorofila, como en el follaje de otoño, predominan los amarillos y naranjas de los carotenoides. Por la misma razón, los colores carotenoides a menudo predominan en la fruta madura después de haber sido enmascarados por la desaparición de la clorofila.
Los carotenoides son responsables de los amarillos brillantes y naranjas que tiñen de hoja caduca follaje (como mueren las hojas de otoño ) de ciertas especies de madera dura como nogales , ceniza , arce , álamo amarillo , álamo , abedul , cerezo negro , sicomoro , álamo , sasafrás , y aliso . Los carotenoides son el pigmento dominante en la coloración de las hojas de otoño de aproximadamente el 15-30% de las especies de árboles. [32]Sin embargo, los rojos, los púrpuras y sus combinaciones combinadas que decoran el follaje otoñal generalmente provienen de otro grupo de pigmentos en las células llamadas antocianinas . A diferencia de los carotenoides, estos pigmentos no están presentes en la hoja durante toda la temporada de crecimiento, pero se producen activamente hacia fines del verano. [33]
Aroma productos químicos [ editar ]
Los productos de la degradación de los carotenoides, como las iononas , las damasconas y las damascenonas , también son sustancias químicas de fragancia importantes que se utilizan ampliamente en la industria de perfumes y fragancias. Tanto la β-damascenona como la β-ionona, aunque la concentración baja en los destilados de rosas son los compuestos clave que contribuyen al olor en las flores. De hecho, los dulces aromas florales presentes en el té negro , el tabaco envejecido , la uva y muchas frutas se deben a los compuestos aromáticos que resultan de la descomposición de los carotenoides.
Enfermedad [ editar ]
Algunos carotenoides son producidos por bacterias para protegerse del ataque inmune oxidativo. El pigmento dorado que le da a algunas cepas de Staphylococcus aureus su nombre ( aureus = golden) es un carotenoide llamado estafilocantina . Este carotenoide es un factor de virulencia con una acción antioxidante que ayuda al microbio a evadir la muerte por las especies reactivas de oxígeno utilizadas por el sistema inmunitario del huésped. [34]
Carotenoides naturales [ editar ]
- Hidrocarburos
- Lycopersene 7,8,11,12,15,7 ', 8', 11 ', 12', 15'-Decahydro-γ, γ-caroteno
- Fitoflueno
- Licopeno
- Hexahidrolcopeno 15- cis -7,8,11,12,7 ', 8'-Hexahydro-γ, γ-caroteno
- Torulene 3 ', 4'-Didehidro-β, γ-caroteno
- α-zeacaroteno 7 ', 8'-dihidro-ε, γ-caroteno
- Alcoholes
- Alloxantina
- Cynthiaxanthin
- Pectenoxantina
- Criptomonaxantina (3R, 3'R) -7,8,7 ', 8'-tetradehidro-β, β-caroteno-3,3'-diol
- Crustaxantina β, -Caroteno-3,4,3 ', 4'-tetrol
- Gazaniaxantina (3R) -5'-cis-β, γ-Caroten-3-ol
- OH-clorobacteno 1 ', 2'-dihidro-f, γ-caroten-1'-ol
- Loroxantina β, ε-Caroteno-3,19,3'-triol
- Luteína (3R, 3'R, 6'R) -β, ε-caroteno-3,3′-diol
- Lycoxanthin γ, γ-Caroten-16-ol
- Rhodopin 1,2-Dihydro-γ, γ-caroten-l-ol
- Rhodopinol aka Warmingol 13- cis -1,2-Dihydro-γ, γ-carotene-1,20-diol
- Saproxantina 3 ', 4'-Didehidro-1', 2'-dihidro-β, γ-caroteno-3,1'-diol
- Zeaxantina
- Glucósidos
- Oscilaxantina 2,2'-Bis (β-L-ramnopiranosiloxi) -3,4,3 ', 4'-tetradehidro-1,2,1', 2'-tetrahidro-γ, γ-caroteno-1,1'- diol
- Phleixantophophy 1 '- (β-D-Glucopyranosiloxi) -3', 4'-didehidro-1 ', 2'-dihidro-β, γ-caroten-2'-ol
- Éteres
- Rhodovibrin 1'-Methoxy-3 ', 4'-didehydro-1,2,1', 2'-tetrahydro-γ, γ-caroten-1-ol
- Esferoideno 1-metoxi-3,4-didehidro-1,2,7 ', 8'-tetrahidro-γ, γ-caroteno
- Epóxidos
- Diadinoxantina 5,6-Epoxi-7 ', 8'-didehidro-5,6-dihidro-caroteno-3,3-diol
- Luteoxantina 5,6: 5 ', 8'-Diepoxi-5,6,5', 8'-tetrahidro-β, β-caroteno-3,3'-diol
- Mutatoxantina
- Citroxantina
- 5,8-Epoxi-5,8-dihidro-β, β-caroteno-3,3'-diol de zeaxantina.
- Neochrome 5 ', 8'-Epoxy-6,7-didehydro-5,6,5', 8'-tetrahydro-β, β-carotene-3,5,3'-triol
- Foliar
- Trollichrome
- Vaucheriaxantina 5 ', 6'-Epoxi-6,7-didehidro-5,6,5', 6'-tetrahidro-β, β-caroteno-3,5,19,3'-tetrol
- Aldehídos
- Rodopinal
- Warmingone 13-cis-1-Hydroxy-1,2-dihydro-γ, γ-caroten-20-al
- Torularhodinaldehyde 3 ', 4'-Didehydro-β, γ-caroten-16'-al
- Ácidos y ésteres ácidos.
- Torularhodin 3 ', 4'-Didehydro-β, γ-caroten-16'-oic acid
- Torularhodin metil éster Metil 3 ', 4'-didehidro-β, γ-caroten-16'-oato
- Cetonas
- Astaceno
- Astaxantina
- Cantaxantina [35] también conocida como Aphanicin, Chlorellaxanthin β, β-Carotene-4,4'-dione
- Capsantina (3R, 3'S, 5'R) -3,3'-dihidroxi-β, κ-caroten-6'-one
- Capsorubina (3S, 5R, 3'S, 5'R) -3,3'-dihidroxi-κ, κ-caroteno-6,6'-diona
- Cryptocapsin (3'R, 5'R) -3'-Hydroxy-β, κ-caroten-6'-one
- 2,2'-dicetospiriloxantina 1,1'-dimetoxi-3,4,3 ', 4'-tetradehidro-1,2,1', 2'-tetrahidro-γ, γ-caroteno-2,2'-diona
- Echinenona β, β-caroten-4-ona
- 3'-hidroxiquinenona
- Flexixantina 3,1'-dihidroxi-3 ', 4'-didehidro-1', 2'-dihidro-β, γ-caroten-4-ona
- 3-OH-cantaxantina aka adonirubina aka fenicoxantina 3-hidroxi-β, β-caroteno-4,4'-diona
- Hydroxyspheriodenone 1'-Hydroxy-1-methoxy-3,4-didehydro-1,2,1 ', 2', 7 ', 8'-hexahydro-γ, γ-caroten-2-one
- Okenone 1'-Metoxi-1 ', 2'-dihidro-c, γ-caroten-4'-one
- Pectenolone 3,3'- Dihydroxy -7 ', 8'-didehydro-β, β-caroten-4-one
- Phoeniconone aka Dehydroadonirubin 3-Hydroxy-2,3-didehydro-β, β-carotene-4,4'-dione
- Phoenicopterone β, ε-caroten-4-one
- Rubixanthone 3-Hydroxy-β, γ-caroten-4'-one
- Sifonaxantina 3,19,3'-Trihidroxi-7,8-dihidro-β, ε-caroten-8-ona
- Esteres de alcoholes
- Astacein 3,3'-Bispalmitoyoxi-2,3,2 ', 3'-tetradehidro-β, β-caroteno-4,4'-diona o 3,3'-dihidroxi-2,3,2', 3'- dipalmitato de tetradehidro-β, β-caroteno-4,4'-diona
- Fucoxantina 3'-Acetoxi-5,6-epoxi-3,5'-dihidroxi-6 ', 7'-didehidro-5,6,7,8,5', 6'-hexahidro-β, β-caroten-8 -uno
- Isofucoxantina 3'-Acetoxi-3,5,5'-trihidroxi-6 ', 7'-didehidro-5,8,5', 6'-tetrahidro-β, β-caroten-8-ona
- Physalien
- Zeaxantina (3R, 3'R) -3,3'-bispalmitoyiloxi-β, β-caroteno o (3R, 3'R) -β, β-caroteno-3,3'-diol
- Siphonein 3,3'-dihidroxi-19-lauroiloxi-7,8-dihidro-β, ε-caroten-8-ona o 3,19,3'-trihidroxi-7,8-dihidro-β, ε-caroten-8 -un 19-laurato
- Apocarotenoides
- β-Apo-2'-carotenal 3 ', 4'-Didehidro-2'-apo-b-caroten-2'-al
- Apo-2-licopenal
- Apo-6'-lycopenal 6'-Apo-y-caroten-6'-al
- Azafrinaldehído 5,6-dihidroxi-5,6-dihidro-10'-apo-β-caroten-10'-al
- Bixin 6'-metil hidrógeno 9'-cis-6,6'-diapocaroteno-6,6'-dioato
- Citranaxantina 5 ', 6'-dihidro-5'-apo-β-caroten-6'-uno o 5', 6'-dihidro-5'-apo-18'-nor-β-caroten-6'-uno o 6'-metil-6'-apo-β-caroten-6'-one
- Crocetin 8,8'-Diapo-8,8'-carotenedioic acid
- Ácido crocetinsemialdehído 8'-oxo-8,8'-diapo-8-carotenoico
- Digentiobiosyl 8,8'-diapo-8,8'-carotenedioato de Crocin
- Hopkinsiaxantina 3-Hidroxi-7,8-didehidro-7 ', 8'-dihidro-7'-apo-b-caroteno-4,8'-diona o 3-hidroxi-8'-metil-7,8-didehidro 8'-apo-b-caroteno-4,8'-diona
- Apo-6'-licopenoato de metilo 6'-apo-y-caroten-6'-oato de metilo
- Paracentrona 3,5-dihidroxi-6,7-didehidro-5,6,7 ', 8'-tetrahidro-7'-apo-b-caroten-8'-uno o 3,5-dihidroxi-8'-metil- 6,7-didehidro-5,6-dihidro-8'-apo-b-caroten-8'-one
- Sintaxantina 7 ', 8'-dihidro-7'-apo-b-caroten-8'-one o 8'-metil-8'-apo-b-caroten-8'-one
- Nor- y seco-carotenoides
- Actinioerythrin 3,3'-Bisacyloxy-2,2'-dinor-b, b-carotene-4,4'-dione
- β-carotenona 5,6: 5 ', 6'-diseco-b, b-caroteno-5,6,5', 6'-tetrona
- Peridinina 3'-Acetoxi-5,6-epoxi-3,5'-dihidroxi-6 ', 7'-didehidro-5,6,5', 6'-tetrahidro-12 ', 13', 20'-trinor b, b-caroten-19,11-olide
- Pirroxantininol 5,6-epoxi-3,3'-dihidroxi-7 ', 8'-didehidro-5,6-dihidro-12', 13 ', 20'-trinor-b, b-caroten-19,11-olido
- Semi-α-carotenona 5,6-Seco-b, e-caroteno-5,6-diona
- Semi-β-carotenona 5,6-seco-b, b-caroteno-5,6-diona o 5 ', 6'-seco-b, b-caroteno-5', 6'-diona
- Tripasiaxantina 3-Hidroxisemi-b-carotenona 3'-Hidroxi-5,6-seco-b, b-caroteno-5,6-diona o 3-hidroxi-5 ', 6'-seco-b, b-caroteno-5 ', 6'-dione
- Retro-carotenoides y retro-apo-carotenoides
- Eschscholtzxanthin 4 ', 5'-Didehydro-4,5'-retro-b, b-carotene-3,3'-diol
- Eschscholtzxanthone 3'-Hydroxy-4 ', 5'-didehydro-4,5'-retro-b, b-caroten-3-one
- Rodoxantina 4 ', 5'-Didehidro-4,5'-retro-b, b-caroteno-3,3'-diona
- Tangeraxantina 3-hidroxi-5'-metil-4,5'-retro-5'-apo-b-caroten-5'-one o 3-hidroxi-4,5'-retro-5'-apo-b-caroten -5'-uno
- Carotenoides superiores
- Nonaprenoxanthin 2- (4-hidroxi-3-metil-2-butenil) -7' , 8' , 11' , 12'-tetrahidro-e, y-caroteno
- Decaprenoxantina 2,2'-Bis (4-hidroxi-3-metil-2-butenil) -e, e-caroteno
- Cp 450 2- [4-Hidroxi-3- (hidroximetil) -2-butenil] -2 '- (3-metil-2-butenil) -b, b-caroteno
- Cp 473 2 '- (4-Hidroxi-3-metil-2-butenil) -2- (3-metil-2-butenil) -3', 4'-didehidro-1 ', 2'-dihidro-b, y -caroten-1'-ol
- Bacterioruberin 2,2'-Bis (3-hidroxi-3-metilbutil) -3,4,3 ', 4'-tetradehidro-1,2,1', 2'-tetrahidro-y, y-caroteno-1,1 '-dio






No hay comentarios:
Publicar un comentario