Célula madre cancerosa
La célula madre cancerosa es un tipo hipotético de célula madre que formaríatumores mientras que tendría las propiedades de las células madres como autorenovación y la habilidad de diferenciarse en múltiples tipos de células. Una teoría sugiere que dichas células persisten en los tumores como una población distinta y causa la recaída y la metástasis al dar crecimiento a nuevos tumores. El desarrollo de terapias específicas apuntadas a las células madre cancerosas esperando mejorar la supervivencia y la calidad de vida de los pacientes concáncer, especialmente para los que sufren de metástasis.- .......................................................................:https://es.wikipedia.org/w/index.php?title=C%C3%A9lula_madre_cancerosa&printable=yes
La teoría de las células madre cancerígenas siempre ha sido polémica aunque podría ofrecer nuevas esperanzas para ganar la lucha contra el cáncer. ¿En qué consiste esta teoría y qué significa para la investigación del cáncer?
El cáncer posee una característica biológica importante: provoca que las células se dividan o proliferen de un modo descontrolado. La mayoría de las terapias actuales contra el cáncer emplean compuestos que interfieren con uno o varios mecanismos de proliferación celular. Estos tratamientos se basan en la aceptación de que las células sanas proliferan a una velocidad mucho menor que las células tumorales. Sin embargo, las células sanas también proliferan, de modo que las actuales terapias resultan altamente tóxicas y producen demasiados efectos secundarios, especialmente en aquellos órganos o tejidos en los que las células se renuevan con regularidad; tal es el caso del pelo, la sangre o la mucosa intestinal. Más importante aún es el hecho de que, aunque inicialmente estos compuestos son capaces de reducir el tamaño tumoral, muchos cánceres acaban por resultar incurables de modo que las recaídas ocurren en un buen número de casos.
¿Son las células madre cancerígenas las responsables de las recaídas?
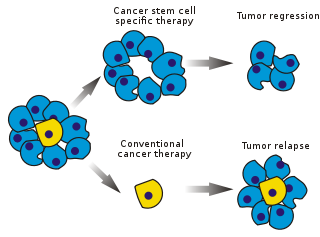
La teoría de las células madre cancerígenas (CSC, de sus siglas en inglés, Cancer Stem Cells) explica el origen de las recaídas del siguiente modo: sugiere que los tumores están mantenidos por una sub-población especial de células cancerígenas. De acuerdo con esta teoría, estas células son las únicas, de entre todas las que componen la masa tumoral, que pueden auto-renovarse (es decir, se copian a sí mismas) y, con ello, mantener el tumor. Debido a su carácter de células madre, las células madre cancerígenas apenas se verían afectadas por las terapias estándar; en cambio, serían capaces de sobrevivir y continuar dividiéndose, lo que traería consigo la reaparición del tumor con el paso del tiempo. Esto se podría relacionar con los efectos que la quimioterapia produce en otros tejidos, como el pelo: las células diferenciadas que forman la mayoría del pelo mueren durante el tratamiento, pero no le ocurre lo mismo a las células madre, responsables de mantener el crecimiento del cabello; cuando se termina la terapia, el pelo vuelve a crecer de modo normal.
La teoría de las células madre cancerígenas (CSC, de sus siglas en inglés, Cancer Stem Cells) explica el origen de las recaídas del siguiente modo: sugiere que los tumores están mantenidos por una sub-población especial de células cancerígenas. De acuerdo con esta teoría, estas células son las únicas, de entre todas las que componen la masa tumoral, que pueden auto-renovarse (es decir, se copian a sí mismas) y, con ello, mantener el tumor. Debido a su carácter de células madre, las células madre cancerígenas apenas se verían afectadas por las terapias estándar; en cambio, serían capaces de sobrevivir y continuar dividiéndose, lo que traería consigo la reaparición del tumor con el paso del tiempo. Esto se podría relacionar con los efectos que la quimioterapia produce en otros tejidos, como el pelo: las células diferenciadas que forman la mayoría del pelo mueren durante el tratamiento, pero no le ocurre lo mismo a las células madre, responsables de mantener el crecimiento del cabello; cuando se termina la terapia, el pelo vuelve a crecer de modo normal.
La teoría de las células madre cancerígenas, por tanto, mantiene que los tumores son tejidos basados en células madre, con una arquitectura muy similar a la presente en otros tejidos corporales, aunque con defectos que son los causantes de la enfermedad. Este punto de vista implica que el estudio de las células diferenciadas capaces de dividirse rápidamente y que son las que ocupan la mayor parte de la masa tumoral no nos aportaría mucha información sobre la causa del cáncer. En cambio, lo que necesitamos estudiar son las células madre cancerígenas, que se dividen más lentamente y que mantienen el tumor.
Una teoría con historia
Aunque fue propuesta hace casi 50 años, ha sido durante los últimos años cuando la teoría de las células madre cancerígenas ha ido ganando aceptación. La existencia de las células madre cancerígenas se ha demostrado en varios tipos de cáncer humano. Sin embargo, todavía hay quienes se oponen a esta teoría, particularmente entre los clínicos: defienden que la teoría principalmente representa un artefacto de laboratorio debido a que somos incapaces tecnológicamente de trasplantar tumores en animales de modo que el 100% de las células sean trasplantadas. En este sentido, argumentaría que el principal concepto de la teoría de las células madre cancerígenas no tiene nada que ver con el número exacto de células presentes en el tumor. Al contrario: la idea de esta teoría es que un tumor está compuesto de una mezcla de células que desempeñan funciones diferentes; y solamente un pequeño grupo de células en el tumor son capaces de iniciar y mantener el crecimiento maligno en el cuerpo. No obstante, existen diversos tipos de cáncer y algunos de ellos parecen no seguir el modelo de las células madre cancerígenas.
Aunque fue propuesta hace casi 50 años, ha sido durante los últimos años cuando la teoría de las células madre cancerígenas ha ido ganando aceptación. La existencia de las células madre cancerígenas se ha demostrado en varios tipos de cáncer humano. Sin embargo, todavía hay quienes se oponen a esta teoría, particularmente entre los clínicos: defienden que la teoría principalmente representa un artefacto de laboratorio debido a que somos incapaces tecnológicamente de trasplantar tumores en animales de modo que el 100% de las células sean trasplantadas. En este sentido, argumentaría que el principal concepto de la teoría de las células madre cancerígenas no tiene nada que ver con el número exacto de células presentes en el tumor. Al contrario: la idea de esta teoría es que un tumor está compuesto de una mezcla de células que desempeñan funciones diferentes; y solamente un pequeño grupo de células en el tumor son capaces de iniciar y mantener el crecimiento maligno en el cuerpo. No obstante, existen diversos tipos de cáncer y algunos de ellos parecen no seguir el modelo de las células madre cancerígenas.
Implicaciones significantes para futuras terapias e investigación
La existencia de células madre tumorales posee una implicación terapéutica de gran importancia: únicamente mediante la eliminación de las células madre cancerígenas es posible evitar las recaídas y conseguir una cura definitiva. Para ello, debemos ser capaces de dirigir la terapia específicamente contra las células madre cancerígenas, diferenciándolas de las célula madre normales que mantienen los tejidos sanos (las terapias que también destruyen las células madre normales serían letales para el paciente). Este punto sigue siendo el mayor reto a conseguir en los próximos años.
La existencia de células madre tumorales posee una implicación terapéutica de gran importancia: únicamente mediante la eliminación de las células madre cancerígenas es posible evitar las recaídas y conseguir una cura definitiva. Para ello, debemos ser capaces de dirigir la terapia específicamente contra las células madre cancerígenas, diferenciándolas de las célula madre normales que mantienen los tejidos sanos (las terapias que también destruyen las células madre normales serían letales para el paciente). Este punto sigue siendo el mayor reto a conseguir en los próximos años.
"Las terapias basadas en las células madre cancerígenas no deben reemplazar, sino complementar, las actuales aproximaciones terapéuticas."
Con la vista puesta en el futuro, existen evidencias que sugieren que el cáncer humano podría ser causado por algún tipo de reprogramación celular. En otras palabras, algunos genes causantes del cáncer (conocidos como “oncogenes”) se activan en las células y esto las “reprograma” para que se comporten de un modo diferente – se convierten en células madre cancerígenas. Si el potencial de crecimiento tumoral depende de la actividad de las células madre cancerígenas que presentan determinados oncogenes activados, será importante conocer, por tanto, cómo inactivar este proceso de reprogramación celular (ver el diagrama de arriba). En mi opinión, ésta es un área importante en la que centrar los esfuerzos en investigación. La formación de células tumorales como resultados de una reprogramación genética representa una nueva explicación de cómo se crean y mantienen las células del cáncer. Obviamente, las implicaciones prácticas que este nuevo punto de vista ofrece a las terapias contra el cáncer son enormes. Lo que está claro es que las terapias basadas en las células madre cancerígenas no deberían reemplazar a las aproximaciones terapéuticas actuales, sino complementarlas: la eliminación de la masa tumoral es necesaria en los primeros momentos del tratamiento, tanto si somos capaces de dirigir la terapia contra las células madre tumorales como si no. En los próximos años se verá si el optimismo sobre los nuevos tratamientos basados en la teoría de las células madre cancerígenas tiene su razón de ser o si, por el contrario, la inmensa complejidad de esta enfermedad continuará trastocando nuestros mejores esfuerzo por tratarla.

Célula madre mesenquimatosa
Las células madre mesenquimales también conocidas como células madre estromales o MSC (del inglés Mesenchymal Stem Cells o Mesenchymal Stromal Cells), son células multipotentes primitivas, con morfología fibroblastoide, originadas a partir de la capa germinal mesodermal, con la capacidad de diferenciarse en diversos tipos de células,1 18 incluyendo osteocitos (células óseas), condrocitos (células del cartílago), adipocitos (células grasas), mioblastos (precursores de células musculosas) cardiomiocitos (células del corazón), neuronas y astrocitos (Células gliales) tanto in vivo como in vitro.- ...........................................................:https://es.wikipedia.org/w/index.php?title=C%C3%A9lula_madre_mesenquimatosa&printable=yes
Las células madre mesenquimales (CMM) pueden producir varios tipos de células de los tejidos esqueléticos, tales como el cartílago, hueso y grasa. Científicos están investigando cómo las CMM pueden usarse para tratar enfermedades óseas y de cartílago. Algunas investigaciones basadas en las CMM están explorando terapias para otras enfermedades, pero la base científica de estas aplicaciones todavía no se ha establecido o aceptado ampliamente.
¿Sabías que...?
Las células madre mesenquimales pueden generar un 0.001-0.01% de todas las células de la médula ósea.
Las células madre mesenquimales crecen en monocapa en el fondo de los frascos de cultivo; magnificación 4x
Las células madre mesenquimales crecen en monocapa en el fondo de los frascos de cultivo; magnificación 10x
Células óseas procedentes de CMMs; la coloración proviene de una tinción usada para distinguir células óseas (tinción von Kossa)
Células grasas procedentes de CMMs; el color rojo viene de una tinción llamada ‘’Nile red O’’ usado para distinguir células grasas
¿Qué pueden hacer las células madre mesenquimales?
Las células madre mesenquimales (CMM) son un ejemplo de tejido o células madre ‘’adultas’’. Son ‘’pluripotentes’’, es decir, pueden producir más de un tipo de célula especializada del organismo, pero no todos los tipos. Las CMM pueden producir distintas células especializadas que se encuentran en los tejidos esqueléticos. Por ejemplo, se pueden diferenciar – o especializar – en células de cartílago (condrocitos), células óseas (osteoblastos) y células grasas (adipocitos). Esta células especializadas tienen cada una sus propias formas, estructuras y funciones, y cada una pertenece a un tejido particular.
Algunas investigaciones preliminares sugieren que las CMM también pueden diferenciarse en muchos tipos diferentes de células que no pertenecen a los tejidos esqueléticos, tales como células nerviosas, células del músculo cardíaco, células del hígado y células endoteliales, las cuales forman la capa interna de los vasos sanguíneos. Estos resultados no se han confirmado hasta la fecha. En algunos casos, parece que las CMM se pueden fusionar con células especializadas existentes, lo que conduce a falsas conclusiones acerca de la capacidad de las MSC para producir ciertos tipos de células. En otros casos, los resultados son un efecto artificial causado por productos químicos utilizados para cultivar las células en el laboratorio.
¿Dónde se encuentran las células madre mesenquimales?
Las CMM se encontraron originalmente en la médula ósea. Desde entonces, se piensa que existen también en una amplia variedad de tejidos, tales como en la sangre del cordón umbilical, tejido adiposos (grasa) y el músculo. Sin embargo, no se ha establecido todavía si las células tomadas de estos otros tejidos son realmente las mismas células, o similares a las células madre mesenquimales procedentes de la médula ósea.
La médula ósea contiene muchos tipos diferentes de células. Entre ellos se encuentran las células madre de la sangre (también llamadas células madre hematopoyéticas o HSC) y una variedad de diferentes tipos de células que pertenecen a un grupo llamado células ‘’mesenquimales’’. Sólo alrededor de un 0.001-0.01% de las células de la médula ósea soncélulas madre mesenquimales.
Es bastante fácil obtener una mezcla de diferentes tipos de células mesenquimales procedentes de la médula ósea, para utilizarlas en investigación. Pero el aislamiento de la pequeña fracción de células que son células madre mesenquimales es más complicado. Algunas de las células de esta mezcla son capaces de formar hueso y grasa, por ejemplo, pero no tienen todas las propiedades de las células madre mesenquimales. El reto hoy en día es identificar y seleccionar las células que se pueden auto-renovar (producir más copias de ellas mismas) y que puedan diferenciarse en los tres tipos de células – de hueso, cartílago y grasa. Los científicos aún no han llegado a un consenso sobre la mejor manera de hacer esto.
Desarrollo de nuevos tratamientos con células madre mesenquimales
Aún no hay tratamientos que utilicen CMM disponibles. Sin embargo, se están explorando varias posibilidades para usarlas en la clínica médica.
Reparación de hueso y cartílago
La capacidad de las MSC de diferenciarse en células óseas, llamadas osteoblastos, ha llevado a su uso en ensayos clínicos preliminares que investigan la seguridad de estos posibles métodos de reparación ósea. Estos estudios están considerando el posible tratamiento de defectos esqueléticos localizados (daño en un lugar determinado en el hueso).
La capacidad de las MSC de diferenciarse en células óseas, llamadas osteoblastos, ha llevado a su uso en ensayos clínicos preliminares que investigan la seguridad de estos posibles métodos de reparación ósea. Estos estudios están considerando el posible tratamiento de defectos esqueléticos localizados (daño en un lugar determinado en el hueso).
Otras investigaciones se centran en el uso de las CMM para reparar cartílago. El cartílago cubre los extremos de los huesos y permite que un hueso se deslice sobre el otro en las articulaciones. El cartílago puede ser dañado por una lesión repentina, como una caída, o durante un largo período por una enfermedad como la osteoartritis, una enfermedad muy dolorosa de las articulaciones. El cartílago no se repara bien después dañarse. El mejor tratamiento para reparar cartílago gravemente dañado es la cirugía, la cual se basa en reemplazar la articulación dañada por una artificial. Debido a que las CMM pueden diferenciarse en células de cartílago, llamadas condrocitos, los científicos esperan que las CMM puedan ser inyectadas en los pacientes para reparar y mantener el cartílago de sus articulaciones. Científicos también están investigando la posibilidad de que las CMM trasplantadas secreten algunas sustancias que dirigirán a las células del propio pacientes para reparar el daño.
Aún quedan muchos obstáculos que sobrepasar antes de que este tipo de tratamiento sea una realidad. Por ejemplo, cuando las CMM son trasplantadas, la mayoría de ellas son rápidamente eliminadas por el cuerpo. Científicos están trabajando en técnicas nuevas para trasplantar las MSC, tales como el desarrollo de estructuras tridimensionales o ‘’andamios’’ que imitan las condiciones de la parte del cuerpo donde las células son requeridas. Estos andamios mantendrán las células y las animará a diferenciarse en el tipo celular deseado.
Reparación del corazón y vasos sanguíneos
Estudios en ratones indican que las CMM pueden promover la formación de nuevos vasos sanguíneos mediante un proceso denominado neovascularización. Las CMM no pueden hacer nuevas células de los vasos sanguíneos por ellas mismas, pero pueden ayudar al proceso de neovascularización de distintas formas. Por ejemplo, pueden liberar proteínas que estimulan el crecimiento de otras células llamadas células precursoras endoteliales –células que se desarrollarán y formarán la capa interna de los vasos sanguíneos. Este tipo de estudios en animales ha llevado a los investigadores a esperar que las MSC puedan proporcionar una forma de reparar el daño de vaso sanguíneo vinculado a ataques cardíacos o enfermedades como la isquemia critica de las extremidades. Actualmente, un número de ensayos clínicos en fase inicial están utilizando MSC con pacientes, pero todavía no esta claro si los tratamientos serán eficaces.
Enfermedades inflamatorias y autoinmunes
Algunos estudios sugieren que las CMM son capaces de evitar la su detección por el sistema inmune y que pueden ser transplantadas de un paciente a otro sin riesgo de rechazo inmune por el organismo. Sin embargo, estas afirmaciones no han sido confirmadas por otros estudios, También se ha sugerido que las CMM pueden ser capaces de reducir la velocidad de multiplicación de las células inmunes en el cuerpo, así, podrían reducir la inflamación y ayudar a tratar el rechazo de trasplantes o enfermedades autoinmunes. Una vez más, esto tiene que ser confirmado, y se necesitan muchas mas evidencias para establecer si las CMM realmente podrían utilizarse para este tipo de aplicación.
Algunos estudios sugieren que las CMM son capaces de evitar la su detección por el sistema inmune y que pueden ser transplantadas de un paciente a otro sin riesgo de rechazo inmune por el organismo. Sin embargo, estas afirmaciones no han sido confirmadas por otros estudios, También se ha sugerido que las CMM pueden ser capaces de reducir la velocidad de multiplicación de las células inmunes en el cuerpo, así, podrían reducir la inflamación y ayudar a tratar el rechazo de trasplantes o enfermedades autoinmunes. Una vez más, esto tiene que ser confirmado, y se necesitan muchas mas evidencias para establecer si las CMM realmente podrían utilizarse para este tipo de aplicación.
Investigaciones actuales y su futuro
La investigación sobre terapias que emplean CMM se encuentra todavía en su infancia. Se necesita mucho más trabajo antes de que este tipo de terapias puedan emplearse rutinariamente en pacientes. Quedan pendientes algunas cuestiones acerca de cómo se pueden controlar estas células, cómo se comportarán cuando sean trasplantadas en el cuerpo, cómo pueden ser trasplantadas en el lugar adecuado para que funcionen eficazmente, y así, sucesivamente. Al estudiar cómo esta células trabajan e interactúan dentro del cuerpo, los investigadores esperan desarrollar nuevos tratamientos seguros y eficaces en el futuro.
No hay comentarios:
Publicar un comentario