Un enlace covalente entre dos átomos o grupos de átomos se produce cuando estos, para alcanzar el octeto estable, comparten electrones del último nivel.
La diferencia de electronegatividades entre los átomos no es suficientemente grande como para que se efectúe una transferencia de electrones. De esta forma, los dos átomos comparten uno o más pares electrónicos en un nuevo tipo de orbital, denominado orbital molecular.
Los enlaces covalentes se suelen producir entre elementos gaseosos o no metales.
La diferencia de electronegatividades entre los átomos no es suficientemente grande como para que se efectúe una transferencia de electrones. De esta forma, los dos átomos comparten uno o más pares electrónicos en un nuevo tipo de orbital, denominado orbital molecular.
Los enlaces covalentes se suelen producir entre elementos gaseosos o no metales.
Entre los dos átomos pueden compartirse uno, dos o tres pares de electrones, lo cual dará lugar a la formación de un enlace simple, doble o triple respectivamente. En la representación de Lewis, estos enlaces pueden representarse por una pequeña línea entre los átomos.
- Enlace sencillo: se comparten 2 electrones de la capa de valencia.
- Enlace doble: se comparten cuatro electrones, en dos pares, de la capa de valencia.
- Enlace triple: se comparten 6 electrones de la capa de valencia en 3 pares.
- Enlace cuádruple: es la unión de 8 electrones de la capa de valencia en 4 pares .
- Enlace quíntuple: es la unión de 10 electrones de la capa de valencia en 5 pares.
Otros Tipos de Enlaces:
| Enlace | Descripción | Propiedades Generales | Ejemplos |
| Iónico | Unión entre iones de distinto signo. Uno de loa átomos capta los electrones del otro. | · Enlaces muy fuertes · Alto punto de fusión(300-1000ºC) · Solubles en agua · Conductores de electricidad en agua | La sal común: Na+ + Cl- → NaCl |
| Covalente | Enlace en el que se comparten los electrones del último nivel. Así alcanzan el octeto estable. | · Tª de fusión elevada (> 1000ºC) · Malos conductores de electricidad · Alta dureza · Insolubles | El gas cloro: Cl- + Cl- → Cl2 |
| Metálico |
Unión entre los núcleos positivos
y la nube de electrones negativa. | · Tª de fusión muy elevada · Tª de ebullición muy elevada · Buenos conductores de electricidad · Dúctiles, maleables y alta dureza · Se oxidan con facilidad | Red cristalina del cobre: iones Cu2+ |
enlace covalente entre dos átomos se produce cuando estos átomos se unen, para alcanzar el octeto estable, compartiendo electrones del último nivel1 (excepto el Hidrógeno que alcanza la estabilidad cuando tiene 2 electrones). La diferencia de electronegatividad entre los átomos no es lo suficientemente grande como para que se produzca una unión de tipo iónica. Para que un enlace covalente se genere es necesario que la diferencia de electronegatividad entre átomos sea menor a 1,7.
De esta forma, los dos átomos comparten uno o más pares electrónicos en un nuevo tipo de orbital, denominado orbital molecular. Los enlaces covalentes se producen entre átomos de un mismo elemento no metal y entre distintos elementos no metales.
Cuando átomos distintos de no metales se unen una forma covalente, uno de ellos resultará más electronegativo que el otro, por lo que tenderá a atraer la nube electrónica del enlace hacia su núcleo, generando un dipolo eléctrico. Esta polarización permite que las moléculas del mismo compuesto se atraigan entre sí por fuerzas electrostáticas de distinta intensidad.
Por el contrario, cuando átomos de un mismo elemento no metálico se unen covalentemente, su diferencia de electronegatividad es cero y no se crean dipolos. Las moléculas entre sí poseen prácticamente una atracción nula.
En síntesis, en un enlace iónico, se produce la transferencia de electrones de un átomo a otro y en el enlace covalente, los electrones de enlace son compartidos por ambos átomos. En el enlace covalente, los dos átomos no metálicos comparten uno o más electrones, es decir, se unen a través de sus electrones en el último orbital, el cual depende del número atómicoen cuestión. Entre los dos átomos pueden compartirse uno, dos o tres pares de electrones, lo cual dará lugar a la formación de un enlace simple, doble o triple respectivamente. En la estructura de Lewis, estos enlaces pueden representarse por una pequeña línea entre los átomos.
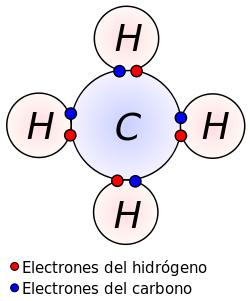
Los primeros conceptos de la unión covalente surgieron de este tipo de imagen de la molécula de carbono y hidrógeno. El enlace covalente está implícito en laestructura de Lewis indicando electrones compartidos entre los átomos.
Historia
El término "covalencia" en relación a la unión fue utilizada por primera vez en 1919 por Irving Langmuir en artículo del Journal of the American Chemical Society titulado «The Arrangement of Electrons in Atoms and Molecules» (La distribución de electrones en átomos y moléculas). En este, Langmuir escribió: «designaremos con el término covalencia al número de pares de electrones que un determinado átomo comparte con sus vecinos».2
La idea de la unión covalente se puede remontar varios años antes hasta Gilbert N. Lewis, quien en 1916 describió el intercambio de pares de electrones entre los átomos.3 Introdujo la notación de Lewis o notación de puntos de electrones o estructura de puntos de Lewis, en el que la valencia de los electrones (los de la capa exterior) se representa en forma de puntos en torno a los símbolos atómicos. Los pares de electrones localizados entre átomos representan enlaces covalentes. Múltiples parejas representan enlaces múltiples, tales como enlaces dobles y enlaces triples. Una forma alternativa de representación, que no se muestra aquí, tiene los pares de electrones de formación de enlaces representados como líneas sólidas.
Lewis propuso que un átomo forma suficientes enlaces covalentes para formar una capa electrónica exterior completa (o cerrada). En el diagrama del metano que se muestra aquí, el átomo de carbono tiene una valencia de cuatro y está, por lo tanto, rodeado por ocho electrones (la regla del octeto), cuatro del carbono mismo y cuatro de los hidrógenos unidos a él. Cada hidrógeno tiene una valencia de uno y está rodeado por dos electrones (una regla del dueto), su propio electrón más uno del carbono. El número de electrones corresponden a capas completas en la teoría cuántica del átomo; la capa exterior de un átomo de carbono es la capa n = 2, con capacidad para ocho electrones, mientras que la capa exterior (y única) de un átomo de hidrógeno es la capa n = 1, con capacidad para solo dos.
Si bien la idea de los pares de electrones compartidos proporciona una imagen cualitativa efectiva de la unión covalente, es necesaria la mecánica cuántica para entender la naturaleza de estas uniones y predecir las estructuras y propiedades de las moléculas simples. Walter Heitler y Fritz London dieron la primera explicación con éxito de un enlace químico aplicando la mecánica cuántica, en concreto del hidrógeno molecular, en 1927.4 Su trabajo se basó en el modelo de enlace de valencia, que asume que un enlace químico se forma cuando hay una buena coincidencia entre los orbitales atómicos de los átomos participantes.
Se sabe que estos orbitales atómicos tienen relaciones angulares específicas entre ellos, y por lo tanto el modelo de enlace de valencia pueden predecir con éxito los ángulos de enlace observados en moléculas simples.
Sin embargo la teoría del enlace covalente o también conocido como la idea de la compartición de electrones, el cual está basado en el átomo cúbico, se enfrentó a varias dificultades conceptuales, ya que esta teoría tuvo como competencia al modelo del enlace iónico. A pesar de esta rivalidad de estas dos Teorías, la teoría del enlace covalente fue aceptada hasta 1920. Niaz Y Rodríguez mencionan en su texto HISTORIA Y FILOSOFÍA DE LAS CIENCIAS: NECESIDAD DE SU INCORPORACIÓN EN LOS TEXTOS UNIVERSITARIOS DE CIENCIAS que Lewis reconoce que la estructura cúbica no puede representar el triple enlace y sugiere reemplazarlo por el átomo tetraédrico. Lewis asumió por muchos años que, si los electrones están apareados en el átomo magnéticamente, es fácil entender cómo dos electrones desapareados en átomos diferentes pueden acoplarse magnéticamente y formar el enlace no polar
Tipos de sustancias covalentes
Existen dos tipos de sustancias covalentes:
Sustancias covalentes moleculares: los enlaces covalentes forman moléculas que tienen las siguientes propiedades:
- Temperaturas de fusión y ebullición bajas.
- En condiciones normales de presión y temperatura (25 °C aprox.) pueden ser sólidos, líquidos o gaseosos.
- Son blandos en estado sólido.
- Son aislantes de la corriente eléctrica y el calor.
- Solubilidad: las moléculas polares son solubles en disolventes polares y las apolares son solubles en disolventes apolares (lo semejante disuelve a lo semejante).
- Ejemplos: dióxido de carbono, benceno, oxígeno, nitrógeno.
Redes o sustancias covalentes reticulares: Además, las sustancias covalentes forman redes cristalinas de un número indefinido de átomos, semejantes a los compuestos iónicos, que tienen estas propiedades:
- Elevadas temperaturas de fusión y ebullición.
- Son sólidos en Condiciones Normales.
- Son sustancias muy duras.
- Son aislantes (excepto el grafito).
- Son insolubles.
- Ejemplos: cuarzo, diamante.
Definición del enlace covalente
Considérense átomos de hidrógeno, a medida que se aproximan entre sí, se van haciendo notar las fuerzas que atraen a cadaelectrón al núcleo del otro átomo, hasta que dichas fuerzas de atracción se llegan a compensar con la repulsión que los electrones sienten entre sí. En ese punto, la molécula presenta la configuración más estable.
Lo que ha sucedido es que los orbitales de ambos electrones se han traslapado, de modo que ahora es imposible distinguir a qué átomo pertenece cada uno de los electrones.
Según los químicos S. Seese y G. William Daub, en la molécula de hidrógeno como en todas las sustancias covalentes se deben de tomar cuatro aspectos:
Primero: las propiedades de los átomos individuales sin combinar son muy distintos a las propiedades de las moléculas. Por ello cuando se escribe la fórmula química del hidrógeno se debe escribir como H2, debido a que es una molécula diatómica.
Segundo: los dos núcleos positivos atraen a los dos electrones con el fin de producir una molécula más estable que la de los átomos separados, en consecuencia se forma un enlace y con ello resulta una molécula más estable a comparación de la anterior. Debido a la atracción que ejercen los núcleos sobre los dos electrones se equilibra la repulsión que hay entre ellos, debido a esto es mayor la probabilidad de encontrar electrones en algún lugar situado entre dos núcleos.
Tercero: la distancia entre los núcleos es tal que las orbitales 1s tienen el máximo traslape, en el caso de la molécula de hidrógeno, la distancia entre los núcleos es aproximadamente de 0.74 Å. De otro modo, la distancia que existe entre dos átomos que se unen en forma covalente se llama longitud de enlace.
Cuarto: para "romper" los enlaces covalentes que hay en 1.0 g de hidrógeno gaseoso y para formar los átomos de hidrógeno se necesitan 52. 0 kcal.5
Sin embargo, cuando los átomos son distintos, los electrones compartidos no serán atraídos por igual, de modo que estos tenderán a aproximarse hacia el átomo más electronegativo, es decir, aquel que tenga una mayor apetencia de electrones. Este fenómeno se denomina polaridad (los átomos con mayor electronegatividad obtienen una polaridad más negativa, atrayendo los electrones compartidos hacia su núcleo), y resulta en un desplazamiento de las cargas dentro de la molécula.
Se podría decir que al átomo más electronegativo al cual,no le gusta compartir sus electrones con los demás átomos, y en el caso más extremo, deseará que el electrón le sea cedido sin condiciones formándose entonces un enlace iónico, de ahí que se diga que los enlaces covalentes polares tienen, en alguna medida, carácter iónico.
Cuando la diferencia de electronegatividades es nula (dos átomos iguales), el enlace formado será covalente puro; para una diferencia de electronegatividades de 1,9 el carácter iónico alcanza ya el 35%, y para una diferencia de 3, será del 49,5%.
Así pues, para diferencias de electronegatividades mayores de 1,7 el enlace adquirirá mayor carácter iónico.
Entre el oxígeno o flúor y los elementos de los grupos 1 y 2, esta diferencia será máxima y su carácter iónico también.
Cuando la diferencia tiene un valor de 0 a 1,7 será el carácter covalente el que predomine, como es el caso del enlace C-H. No obstante, según el químico Raymond Chang, esta diferencia de electronegatividad entre los átomos debe ser de 2,0 o mayor para que el enlace sea considerado iónico (Chang, 371).
Dependiendo de la diferencia de electronegatividad, el enlace covalente puede ser clasificado en covalente polar y covalente puro o apolar. Si la diferencia de electronegatividad está entre 0,8 y 1,7 es un enlace covalente polar, y si es inferior a 0,8 es covalente apolar.
Enlace covalente polar
Se forma entre átomos de diferentes elementos, y la diferencia de electronegatividad debe ser mayor que 0,4. En este enlace, los electrones son atraídos fundamentalmente por el núcleo del átomo más electronegativo, generando moléculas cuya nube electrónica presentará una zona con mayor densidad de carga negativa y otra con mayor densidad de carga positiva (dipolo).
Enlace covalente no polar
Se forma entre átomos iguales y la diferencia de electronegatividad debe ser cero o muy pequeña (menor que 0,8). En este enlace, los electrones son atraídos por ambos núcleos con la misma intensidad, generando moléculas cuya nube electrónica es uniforme.
| Sustancias polares | Sustancias no polares |
|---|---|
| Etano | Metanol |
| Tolueno | Fenol |
| isobutano | Acetona |
| n-Pentano | Ácido Propinoico |
Distintos tipos de enlaces covalentes
- Enlace simple: es un par electrónico compartido formado por un electrón perteneciente al último nivel de energía de cada átomo y se representa con una línea. Ejemplos: H-H, Cl-Cl
- Enlace doble: Formado por dos pares electrónicos compartidos, es decir por dos electrones pertenecientes al último nivel de energía de cada átomo y se representa con dos líneas paralelas. Ejemplo: O=O
- Enlace triple: Formado por tres pares electrónicos compartidos, es decir por tres electrones pertenecientes al último nivel de energía de cada átomo y se representa con tres líneas paralelas. Ejemplo: N≡N
- Enlace covalente dativo o de coordinacion: Es un par electrónico compartido por dos átomos pero ambos electrones son aportados por el mismo átomo. Se suele representar con una flecha (→).
Un ejemplo de una especie química que posee un enlace coordinado, el cual es el ion amonio (NH41+). El Ion amonio está constituido por un protón y amoniaco. Los compuestos en los que se encuentra un enlace coordinado se conocen con el nombre de compuestos de coordinación. Los Compuestos de coordinación o también denominados complejos, los cuales en su mayoría de los casos están unidos a varios aniones circundantes conocidos como ligandos.
Enlaces Covalentes
Los enlaces covalentes se definen como la unión que se produce entre 2 átomos por la compartición de 2 o más electrones de su capa externa con objeto de formar una molécula estable.
Un ejemplo claro es la molécula de Cloro, el cloro en estado natural se presenta como una molécula formada por 2 átomos de cloro, dichos átomos de cloro se encuentran unidos mediante un enlace covalente producido por la compartición de 2 electrones
Durante este proceso 2 átomos se han unido para formar una molécula, obviando la teoria de los orbitales moleculares enlazantes / antienlazantes y con objeto de explicarlo de una manera sencilla, podemos decir que 2 orbitales atómicos (Cl + Cl) se unen para formar un nuevo orbital molecular (Cl2).
Los orbitales se definen como las regiones de los átomos o moléculas donde se encuentran los electrones.
Dentro de los enlaces covalentes nos encontramos con 2 tipos de enlaces covalentes que se pueden originar:
- Enlace covalente polar
- Enlace covalente apolar
Enlace covalente polar
Se origina cuando uno de los átomos dispone de mayor fuerza de atracción de los electrones hacia su núcleo, como resultado se origina una molécula con parte negativa y otra parte positiva (dipolo).
Los enlaces covalentes polares siempre se producen cuando el enlace se realiza entre 2 átomos diferentes.
El grado de polaridad de la molécula resultante del enlace covalente, depende de la fuerza o atracción que atrae los electrones hacia un átomo, este concepto es definido mediante la electronegatividad.
Como ejemplos de sustancias que poseen en su estructura enlaces covalentes polares podemos citar el agua, alcohol isopropílico, metanol, butanol …
Se produce cuando ambos átomos disponen de la misma fuerza de atracción de los electrones hacia su mismo núcleo.
Los enlaces covalentes apolares siempre se producen cuando el enlace se realiza entre 2 átomos iguales o con el mismo grado de electronegatividad.
El concepto de molécula o material polar o apolar es de suma importancia para el estudio de los adhesivos, por lo general aquellas superficies que dispongan de moléculas o materiales polares en su superficie serán óptimas para conseguir fácilmente un adhesivado duradero en el tiempo.









No hay comentarios:
Publicar un comentario