Los granulocitos son células de la sangre caracterizadas por los modos de colorear los orgánulos de su citoplasma, en microscopía de luz. Se les conoce como leucocitos polimorfonucleares, debido a las formas variables de núcleo que pueden presentar. Sin embargo este término suele ser mal utilizado ya que solo es correcto para los neutrófilos y no para los basófilos ni los eosinófilos.
Hay tres tipos de granulocitos en la sangre humana:
Sus nombres derivan de las características coloraciones que adoptan por la sustancia que se utiliza para colorear los orgánulos de la célula; por ejemplo, el granulocito más abundante es el neutrófilo, cuyos orgánulos se colorean con tintes neutros o casi no adquieren el colorante. Los eosinófilos muestran una importante coloración rojiza (eosinofilia) mientras que los basófilos muestran afinidad por colorantes básicos adquiriendo una coloración azulada.
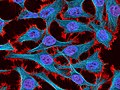
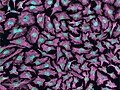
Las células HeLa (también conocidas como “células MePa” o simplemente “Hela”) son un tipo particular de células de cultivo celular, usadas en investigación científica. Es el linaje celular humano más antiguo y utilizado con mayor frecuencia.1 El linaje al cual pertenecen estas células deriva de una muestra de cáncer cérvico-uterino obtenida el 8 de febrero de 19512 de una paciente llamada Henrietta Lacks (de allí el acrónimo He{nrietta} La{cks}) quien falleció el 4 de octubre de ese mismo año debido al cáncer. El linaje HeLa ha mostrado ser particularmente duradero y prolífico, esto se ha demostrado puesto que contamina otros cultivos celulares usados también en investigación en los mismos laboratorios.
George Otto Gey y Henrietta Lacks
Las células fueron reproducidas por George Otto Gey poco antes del fallecimiento de Lacks en 1951. Este fue el primer linaje celular humano que probó ser exitoso al ser cultivado in vitro, lo cual fue un logro científico con grandes beneficios futuros para el campo de la investigación médica. Gey donó gratuitamente tanto las células como las herramientas y procesos que su laboratorio desarrolló a cualquier científico que los solicitara, con el simple propósito de beneficiar de este modo a la ciencia. Ni Lacks ni su familia le otorgaron a Gey permiso para cultivar las células, pero en ese momento, no era requerido ni se acostumbraba pedirlo.5 Las células fueron comercializadas más tarde, aunque nunca fueron patentadas en su forma original. En aquel entonces no existía, como ahora, requerimiento alguno de informar al paciente o a sus familiares sobre estos asuntos, ya que el material descartado u obtenido durante la cirugía, diagnóstico o terapia, es propiedad del médico y/o la institución médica. Este asunto y la situación de Lacks fueron discutidos en el caso Moore v. Regents of the University of California de la Suprema Corte de California. La corte dictaminó que el tejido y células desechadas de una persona no son de propiedad suya y por lo tanto pueden ser comercializados.6
Al principio, se decía que este linaje fue nombrado a partir de una mujer supuestamente llamada “Helen Lane” o “Helen Larson”, con el fin de preservar el anonimato de Lacks. A pesar de este esfuerzo, su nombre real fue usado por la prensa unos pocos años después de su muerte. Estas células son tratadas como células cancerígenas al haberse obtenido de una biopsia de una lesión visible en el cérvix de Lacks, como parte de su diagnóstico de cáncer. El debate respecto a la clasificación de estas células aún continúa.
Las células HeLa son llamadas “inmortales” ya que pueden dividirse un número ilimitado de veces en un cultivo de laboratorio si las condiciones fundamentales para la supervivencia de las células se cumplen (es decir, si son mantenidas y sostenidas en un ambiente adecuado). Hay muchas cepas de células HeLa que continúan evolucionando a través de su crecimiento en diversos cultivos celulares; sin embargo, todas las células HeLa descienden de las mismas células tumorales obtenidas de Lacks. Se ha estimado que el número total de células HeLa obtenidas mediante cultivos celulares excede en mucho al número total de células que llegaron a estar presentes en el cuerpo de Henrietta Lacks.7
Uso en investigación
Las células HeLa fueron usadas por Jonas Salk para probar la primera vacuna contra la poliomielitis en la década de 1950. A partir de entonces, las células HeLa han sido usadas para «investigar el cáncer, SIDA, los efectos de la radiación y sustancias tóxicas, mapeo génico y muchas otras actividades científicas».8 De acuerdo aRebecca Skloot, para el 2009, «más de 60 000 artículos científicos han sido publicados acerca de investigaciones hechas con HeLa, y el número se incrementa a un ritmo constante de más de 300 artículos por mes».6
Telomerasa
La línea celular HeLa fue derivada para su uso en la investigación del cáncer. Estas células proliferan anormalmente rápido, aún comparadas con otras células cancerígenas. En el libro The Immortal Life of Henrietta Lacks de Rebecca Skloot, la autora explica que las células HeLa tienen una versión activa de la telomerasa durante la división celular, que previene el acortamiento gradual de los telomeros, implicados en el envejecimiento y eventual muerte de la células. De este modo, las células HeLa eluden el límite de Hayflick, que es el número limitado de divisiones celulares que la mayoría de las células normales pueden llevar a cabo antes de morir en el cultivo celular.
Número cromosómico
La transferencia horizontal de genes del Virus del Papiloma Humano 18 (VPH 18) hacia células cérvico-uterinas humanas creó el genoma único de las células HeLa, el cual difiere de varias maneras de otros genomas emparentados, entre ellas el número de cromosomas. Las células HeLa poseen una carga cromosómica anormal de 82, con cuatro copias del cromosoma 12 y tres copias de los cromosomas 6, 8 y 17.
“Los virus del Papiloma Humano son integrados frecuentemente al ADN de células cérvico-uterinas cancerígenas. Mapeamos por Hibridación por Fluorescencia In Situ (FISH por sus siglas en inglés) cinco sitios de integración del VPH 18: tres en el cromosoma normal 8 en 8q24 y dos en cromosomas derivados, der(5)t(5;22;8)(q11;q11q13;q24) y der(22)t(8;22)(q24;q13), los cuales poseen material del cromosoma 8q24. Un incremento en la cantidad de copias de 8q24 fue detectado por CGH. Un FISH Dual-color con una prueba de mapeo c-MYC aplicadas a 8q24 revelaron colocalización con VPH18 en todos los sitios de integración, indicando que la dispersión y amplificación de las secuencias génicas de c-MYC ocurrieron después y fueron probablemente detonadas por la inserción del virus en un solo sitio de integración. Aberraciones cromosómicas numéricas y estructurales identificadas por SKY, desbalances genómicos detectados mediante CGH, así como la localización mediante FISH de integración del VPH18 en el locus c-MYC en células HeLa son datos celulares comunes y representativos de etapas avanzadas en carcinomas cérvicouterinos. El genoma HeLa ha sido notoriamente estable después de varios de años de cultivo continuo, por lo tanto, las alteraciones genéticas detectadas pudieron estar presentes en el tumor primario y reflejar eventos que han sido relevantes en el desarrollo del cáncer cérvicouterino.”9
Contaminación
Debido a su adaptabilidad para crecer en cajas de cultivo, las células HeLa en ocasiones son difíciles de controlar. Han probado ser una “mala hierba” persistente que contamina otros cultivos celulares en el mismo laboratorio, interfiriendo con otras investigaciones biológicas y forzando a los investigadores a invalidar muchos de los resultados de sus estudios. El grado de contaminación de las células HeLa entre otros tipos celulares es desconocido ya que pocos investigadores examinan la identidad o pureza de linajes celulares previamente establecidos. Ha sido demostrado que entre el 10 e incluso 20% de los linajes celulares in vitro están contaminados con células HeLa. Stanley Gartler, en 1967, y posteriormente Walter Nelson-Rees, en 1975, fueron los primeros en publicar acerca de la contaminación de diversos linajes celulares por HeLa.10
El escritor científico Michael Gold escribió acerca del problema de la contaminación por HeLa en su libro A Conspiracy of Cells. Describió el problema mundial persistente identificado por Nelson-Rees –que afecta incluso a los laboratorios de los mejores médicos, científicos e investigadores, incluido Jonas Salk– y muchos esfuerzos por hacerle frente, probablemente causando la debacle de algunas carreras. Según Gold, la contaminación por HeLa casi originó un incidente en la Guerra Fría: la URSS y Estados Unidos habían comenzado a cooperar en la guerra contra el cáncer, iniciada por el presidente Richard Nixon sólo para encontrar que las células que habían intercambiado estaban contaminadas con HeLa. Gold arguye que el problema en el caso HeLa estuvo amplificado por emociones, egos y una renuencia a admitir errores. Nelson-Rees explica:
“Es completamente humano –la falta de voluntad de tirar a la basura horas y horas de lo que se creía era una buena investigación… preocupaciones por poner en peligro una subvención que se está solicitando, las prisas por publicar primero. Y no se limita a la biología y a la investigación en cáncer. Muchos científicos de diversas disciplinas cometen los mismos errores y tienen los mismos problemas.”11
En lugar de enfocarse en cómo solucionar el problema de la contaminación por células HeLa, muchos científicos y escritores científicos continúan documentando este problema como una simple cuestión de contaminación –causado no por error humano o defectos, sino por la resistencia, proliferación o la apabullante naturaleza de HeLa.12 13 Datos recientes sugieren que la contaminación cruzada es aun un problema actual en cultivos celulares modernos.3 14
Imágenes adicionales
Helacyton gartleri
Por su habilidad de replicarse indefinidamente y su número de cromosomas diferente al humano, HeLa fueron descritas por Leigh Van Valen como un ejemplo de la creación contemporánea de una nueva especie, Helacyton gartleri. La especie fue nombrada en honor a Stanley M. Gartler, a quien Van Valen atribuye el descubrimiento del “notable éxito de esta especie”15 Su argumento sobre la especiación depende de tres aspectos:
- La incompatibilidad cromosómica de las células HeLa con los seres humanos.
- El nicho ecológico de las células HeLa.
- La habilidad de estas células de prevalecer y crecer sobrepasando los deseos de los cultivadores.
Esta definición no ha sido seguida por otras personas en la sociedad científica, ni ha sido notada ampliamente.
Además de proponer una nueva especie de células HeLa, Van Valen propuso en el mismo documento la nueva familia Helacytidae y el género Helacyton.15 El reconocimiento de los nombres de Van Valen y Maiorana , de cualquier manera, implica que “Helacyton gartleri” es un grupo parafilético de “Homo” y Hominidae, ya que está íntimamamente relacionado con “Homo Sapiens”.
¿Qué es la ELA?
La esclerosis lateral amiotrófica (ELA), a menudo conocida como la “enfermedad de Lou Gehrig”, es una enfermedad neurodegenerativa progresiva que afecta a las células nerviosas del cerebro y de la médula espinal. Las neuronas motoras van del cerebro a la médula espinal y de la médula espinal a los músculos de todo el cuerpo. Con el tiempo, la degeneración progresiva de las neuronas motoras producida por la ELA ocasiona la muerte de éstas. Cuando mueren las neuronas motoras, el cerebro pierde la capacidad de iniciar y controlar el movimiento de los músculos. Debido al efecto progresivo sobre la acción de los músculos voluntarios, los pacientes en las etapas finales de la enfermedad pueden quedar totalmente paralizados.
A-mio-trófica proviene del griego. "A" significa sin o carente. "Mio" se refiere a los músculos, y "trófica" significa alimentación: "Sin alimentación a los músculos". Cuando un músculo no es alimentado, se "atrofia" o se desgasta. "Lateral" identifica las áreas de la médula espinal donde se localizan partes de las células nerviosas que dan señales y controlan los músculos. A medida que esta área se va degenerando, produce la cicatrización o el endurecimiento ("esclerosis") en la región.
A medida que las neuronas motoras se van degenerando, dejan de enviar impulsos a las fibras musculares que normalmente resultan en el movimiento muscular. Los primeros síntomas de la ELA a menudo incluyen una mayor debilidad muscular, especialmente en brazos y piernas, en el habla, en la acción de tragar o en la respiración. Cuando los músculos dejan de recibir los mensajes de las neuronas motoras que requieren para funcionar, se empiezan a atrofiar (se vuelven más pequeños). Las extremidades se empiezan a ver más "delgadas", a medida que se atrofia el tejido muscular.
¿Qué tipos de nervios hacen funcionar el cuerpo adecuadamente?
(de La vida con ELA, Manual 1: ¿De qué se trata todo esto?)
El cuerpo tiene muchas clases de nervios. Hay los involucrados en el proceso del pensamiento, la memoria y en la detección de sensaciones (tales como caliente o frío, afilado o romo, etc.), y otros para la vista, el oído y otras funciones corporales. Los nervios que son afectados por la ELA son las neuronas motoras que producen movimientos voluntarios y fuerza muscular. Ejemplos de movimientos voluntarios son hacer el esfuerzo de alcanzar el teléfono o bajarse de la acera; estas acciones son controladas por los músculos de los brazos y piernas.
El corazón y el sistema digestivo también están hechos de músculo, pero de otra clase, y sus movimientos no están bajo control voluntario. Cuando el corazón late o se digiere una comida, todo ocurre automáticamente. Por lo tanto, el corazón y el sistema digestivo no están involucrados en la ELA. El respirar también pareciera ser involuntario. Recuerde, no obstante, que si bien no se puede detener el corazón, sí se puede aguantar la respiración, por lo que debe tener en mente que, con el tiempo, la ELA podría afectar la respiración.
Aunque por el momento no se entiende por completo qué es lo que causa la ELA, en los últimos años se ha obtenido un nuevo caudal de entendimiento científico respecto a la fisiología de esta enfermedad.
Si bien hoy en día no existe una cura o tratamiento que detenga o revierta la ELA, hay un medicamento aprobado por la FDA, riluzole, que modestamente frena el avance de la ELA, así como varios otros medicamentos en ensayos clínicos que brindan esperanza.
Es importante saber que hay dispositivos y terapias significativas que pueden controlar los síntomas de la ELA que ayudan a las personas a mantener tanta independencia como sea posible y prolongar la supervivencia. Es importante recordar que la ELA es una enfermedad bastante variable; no hay dos personas que lleven la misma vida o tengan las mismas experiencias. Existen casos médicamente documentados de personas en las que la ELA ‘se agota’, deja de avanzar o avanza a un ritmo muy lento. No importa cuál pueda ser su curso o situación individual, la ALS Association y su equipo médico están a su disposición.
Para enterarse de más relatos personales de gente que vive la vida plenamente, haga clic aquí. En palabras de un hombre: “He hecho que la ELA sea parte de mi vida, no mi vida completa”.



No hay comentarios:
Publicar un comentario