Constantes físicas
El magnetón de Bohr (símbolo  ) es una constante físicarelacionada con el momento magnético de los electrones. Específicamente, es la unidad natural —y el valor aproximado-— del momento magnético intrínseco de un electrón.4 Su valor se calculó por primera vez en 1911 por el físico rumano Ștefan Procopiu,5 6 y después en el verano de 1913 por el físico danés Niels Bohr.7
) es una constante físicarelacionada con el momento magnético de los electrones. Específicamente, es la unidad natural —y el valor aproximado-— del momento magnético intrínseco de un electrón.4 Su valor se calculó por primera vez en 1911 por el físico rumano Ștefan Procopiu,5 6 y después en el verano de 1913 por el físico danés Niels Bohr.7
 ) es una constante físicarelacionada con el momento magnético de los electrones. Específicamente, es la unidad natural —y el valor aproximado-— del momento magnético intrínseco de un electrón.4 Su valor se calculó por primera vez en 1911 por el físico rumano Ștefan Procopiu,5 6 y después en el verano de 1913 por el físico danés Niels Bohr.7
) es una constante físicarelacionada con el momento magnético de los electrones. Específicamente, es la unidad natural —y el valor aproximado-— del momento magnético intrínseco de un electrón.4 Su valor se calculó por primera vez en 1911 por el físico rumano Ștefan Procopiu,5 6 y después en el verano de 1913 por el físico danés Niels Bohr.7
En el Sistema Internacional de Unidades, se puede expresar en términos de otras constantes elementales como:
(S.I.)
donde:
 es la carga elemental,
es la carga elemental,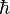 es la constante de Planck reducida,
es la constante de Planck reducida, es la masa en reposo del electrón
es la masa en reposo del electrón
mientras que en el sistema cegesimal es equivalente a:
(cegesimal)
donde  es la velocidad de la luz.
es la velocidad de la luz.
 es la velocidad de la luz.
es la velocidad de la luz.
En el Sistema Internacional de Unidades su valor es aproximadamente:
En unidades atómicas es adimensional, y su valor es simplemente:
Expresado en electronvoltios,
Momento Magnético Orbital del ElectrónDe la expresión clásica del momento magnético, m = IA, se puede deducir una expresión para el momento magnético de un electrón, en una órbita circular alrededor de un núcleo. Es proporcional al momento angular del electrón. La corriente efectiva es
| Índice Conceptos de la Ecuación de Schrödinger Conceptos del Hidrógeno | ||
| Atrás |
Momento Magnético OrbitalEl momento magnético asociado con una órbita de electrón viene dada por
|
La Tierra además de su movimiento orbital alrededor del Sol, tiene un movimiento de rotación alrededor de su eje. Por tanto, el momento angular total de la Tierra es la suma vectorial de su momento angular orbital y su momento angular de rotación alrededor de su eje.
Por analogía, un electrón ligado a un átomo también gira sobre sí mismo, pero no podemos calcular su momento angular de rotación del mismo modo que calculamos el de la Tierra en función de su masa, radio y velocidad angular.
La idea de que el electrón tiene un movimiento de rotación fue propuesta en 1926 por G. Uhlenbeck y S. Goudsmit para explicar las características de los espectros de átomos con un solo electrón. La existencia del espín (rotación) del electrón está confirmada por muchos resultados experimentales, y se manifiesta de forma muy directa en el experimento de Stern-Gerlach, realizado en 1924.
En la simulación de este experimento, se comprobará la existencia del espín del electrón observando que un haz de átomos se divide en dos trazas simétricas al eje X. A partir de la medida de la desviación del haz, determinaremos el valor del magnetón de Bohr.
La simulación es similar al experimento de Thomson que realizamos para determinar la naturaleza de los denominados rayos catódicos y medir la razón entre la carga y la masa del electrón.
La experiencia de Stern-Gerlach se completa en otra página para contar cuantos átomos se depositan en la placa a uno y otro lado del origen, a una temperatura dada, comprobando que el momento magnético medio de los átomos depositados es inversamente proporcional a la temperatura absoluta (ley de Curie).
Descripción
Se postula la existencia de un momento angular intrínseco del electrón llamado espín S . Como el electrón es una partícula cargada, el espín del electrón debe dar lugar a un momento magnético µ intrínseco o de espín. La relación que existente entre el vector momento magnético y el espín esdonde g se denomina razón giromagnética del electrón, su valor experimental es aproximadamente 2.
| El número de orientaciones del vector momento angular respecto a un eje Z fijo es 2S+1, tenemos para el caso del espín S=1/2 que la componente Z tiene dos valores permitidos mB se denomina magnetón de Bohr. |
La energía de un dipolo magnético µ en un campo magnético B que tiene la dirección del eje Z es el producto escalar
U=-µ·B=-µz·B=±µB·B
Si B es variable en la dirección Z, el dipolo magnético experimenta una fuerza
| que lo desviará de su trayectoria rectilínea. Si el dipolo magnético es paralelo al campo magnético, tiende a moverse en la dirección en la que el campo magnético aumenta, mientras que si el dipolo magnético es antiparalelo al campo magnético se moverá en la dirección en la que el campo magnético disminuye. |
Se selecciona un haz de átomos de una velocidad dada y se le hace atravesar una región en la que existe un campo magnético no homogéneo, tal como se muestra en la figura.
- Movimiento del átomo en la región en la que se ha establecido un gradiente de campo magnético
Suponiendo que el gradiente de campo magnético es constante, la aceleración a lo largo del eje Z es constante, a lo largo del eje X es cero. Tenemos un movimiento curvilíneo bajo aceleración constante.
Si la región en la que hay un gradiente de campo magnético tiene una anchura L, la desviación que experimenta el haz, véase la figura, vale
- Movimiento del átomo fuera de dicha región
Cuando el átomo de masa m abandona la región en la que hay un gradiente de campo magnético, sigue una trayectoria rectilínea con velocidad igual a la que tenía al abandonar la citada región. Las componentes de la velocidad serán
La desviación total en la pantalla será
Midiendo d despejamos en dicha ecuación el valor mB del magnetón de Bohr.
| Bohr magneton | ||||
| Value | 927.400 968 x 10-26 J T-1 | |||
| Standard uncertainty | 0.000 020 x 10-26 J T-1 | |||
| Relative standard uncertainty | 2.2 x 10-8 | |||
| Concise form | 927.400 968(20) x 10-26 J T-1 | |||
| Click here for correlation coefficient of this constant with other constants | ||||
| ||||




No hay comentarios:
Publicar un comentario