La actina es una familia de proteínas multifuncionales globularesque forman microfilamentos . Se encuentra esencialmente en todas las células eucariotas (la única excepción conocida es el esperma nematodo ), donde puede estar presente en una concentración de más de 100 µM ; su masa es aproximadamente de 42 kDa , con un diámetro de 4 a 7 nm.
Una proteína actina es la subunidad monomérica de dos tipos de filamentos en las células: microfilamentos , uno de los tres componentes principales del citoesqueleto , y filamentos delgados, parte del aparato contráctil en las células musculares . Puede estar presente como un monómero libre llamado G-actina (globular) o como parte de un microfilamento de polímero lineal llamado F-actina (filamentoso), ambos esenciales para funciones celulares tan importantes como la movilidad y la contracción de las célulasdurante la división celular .
La actina participa en muchos procesos celulares importantes, como la contracción muscular , la motilidad celular , la división celular y la citocinesis , el movimiento de vesículas y orgánulos , la señalización celular y el establecimiento y mantenimiento de las uniones celulares y la forma celular. Muchos de estos procesos están mediados por interacciones extensas e íntimas de la actina con las membranas celulares . [2] En vertebrados, tres grupos principales de isoformas de actina , alfa , beta y gammahan sido identificados Las alfa actinas, que se encuentran en los tejidos musculares, son un componente importante del aparato contráctil. Las actinas beta y gamma coexisten en la mayoría de los tipos de células como componentes del citoesqueleto y como mediadores de la motilidad celular interna . Se cree que el rango diverso de estructuras formadas por la actina que le permite cumplir con un rango tan amplio de funciones se regula a través de la unión de la tropomiosina a lo largo de los filamentos. [3]
La capacidad de una célula para formar microfilamentos dinámicamente proporciona el andamiaje que le permite remodelarse rápidamente en respuesta a su entorno oa las señales internas del organismo , por ejemplo, para aumentar la absorción de la membrana celular o aumentar la adhesión celular para formar tejido celular . Otras enzimas u orgánulos , como los cilios, pueden anclarse a este andamio para controlar la deformación de la membrana celular externa , lo que permite la endocitosis y la citocinesis . También puede producir movimiento por sí mismo o con la ayuda de motores moleculares.. Por lo tanto, la actina contribuye a procesos tales como el transporte intracelular de vesículas y orgánulos, así como a la contracción muscular y la migración celular . Por lo tanto, desempeña un papel importante en la embriogénesis , la curación de heridas y la invasividad de las células cancerosas . El origen evolutivo de la actina se remonta a las células procariotas , que tienen proteínas equivalentes. [4] Los homólogos de actina de procariotas y arqueas se polimerizan en diferentes filamentos helicoidales o lineales que consisten en una o múltiples cadenas. Sin embargo, los contactos en la hebra y los sitios de unión a nucleótidos se conservan en procariotas y en arqueas. [5]Por último, la actina desempeña un papel importante en el control de la expresión génica .
Un gran número de enfermedades y enfermedades son causadas por mutaciones en los alelos de los genes que regulan la producción de actina o de sus proteínas asociadas. La producción de actina también es clave para el proceso de infección por algunos microorganismos patógenos . Las mutaciones en los diferentes genes que regulan la producción de actina en humanos pueden causar enfermedades musculares , variaciones en el tamaño y la función del corazón y sordera . La composición del citoesqueleto también está relacionada con la patogenicidad de las bacterias y virus intracelulares., particularmente en los procesos relacionados con evadir las acciones del sistema inmunológico .

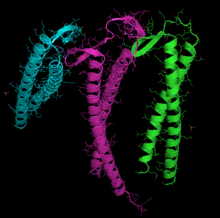
G-actina (código PDB 1j6z) en representación de dibujos animados con ADP y el catión divalente resaltado. La imagen se ha renderizado con PyMol (DeLano, WL El sistema de gráficos moleculares de PyMOL (2002) DeLano Scientific, San Carlos, CA, EE. UU.)
Descubrimiento y la investigación temprana [ editar ]
La actina se observó por primera vez de manera experimental en 1887 por WD Halliburton , quien extrajo una proteína del músculo que "coagulaba" las preparaciones de miosina que él denominó "fermentos de miosina". [7] Sin embargo, Halliburton no pudo perfeccionar más sus hallazgos, y el descubrimiento de la actina se atribuye a Brunó Ferenc Straub , un joven bioquímico que trabaja en el laboratorio de Albert Szent-Györgyi en el Instituto de Química Médica de la Universidad de Szeged. , Hungría .
En 1942, Straub desarrolló una nueva técnica para extraer proteína muscular que le permitió aislar cantidades sustanciales de actina relativamente pura . El método de Straub es esencialmente el mismo que se usa en los laboratorios actuales. Szent-Gyorgyi había descrito previamente la forma más viscosa de la miosina producida por las extracciones musculares lentas como miosina "activada" y, dado que la proteína de Straub produjo el efecto activador, se denominó actina . Agregar ATP a una mezcla de ambas proteínas (llamada actomiosina ) causa una disminución de la viscosidad. Las hostilidades de la Segunda Guerra Mundial significaron que Szent-Gyorgyi y Straub no pudieron publicar el trabajo en Occidente. revistas científicas . Por lo tanto, la actina solo se hizo conocida en Occidente en 1945, cuando su artículo se publicó como un suplemento de la Acta Physiologica Scandinavica . [8] Straub continuó trabajando con actina, y en 1950 informó que la actina contiene ATP unido [9] y que, durante la polimerización de la proteína en microfilamentos , el nucleótido se hidroliza a ADPy fosfato inorgánico (que permanecen unidos al microfilamento) . Straub sugirió que la transformación de la actina unida a ATP en una actina unida a ADP desempeñó un papel en la contracción muscular. De hecho, esto es cierto sólo enmúsculo liso , y no fue apoyado a través de la experimentación hasta 2001. [9] [10]
La secuenciación de aminoácidos de la actina fue completada por M. Elzinga y colaboradores en 1973. [11] La estructura cristalina de la actina G fue resuelta en 1990 por Kabsch y sus colegas. [12] En el mismo año, Holmes y sus colegas propusieron un modelo para la F-actina después de experimentos que utilizan la co-cristalización con diferentes proteínas. [13] El procedimiento de co-cristalización con diferentes proteínas se utilizó repetidamente durante los años siguientes, hasta que en 2001 la proteína aislada se cristalizó junto con ADP. Sin embargo, todavía no existe una estructura de rayos X de alta resolución de F-actina. La cristalización de F-actina fue posible debido al uso de una rodaminaConjugado que impide la polimerización al bloquear el aminoácido cys-374 . [1] Christine Oriol-Audit murió el mismo año en que cristalizó por primera vez la actina, pero fue la investigadora que en 1977 cristalizó por primera vez la actina en ausencia de proteínas de unión a actina (ABP). Sin embargo, los cristales resultantes eran demasiado pequeños para la tecnología disponible de la época. [14]
Aunque actualmente no existe un modelo de alta resolución de la forma filamentosa de la actina, en 2008 el equipo de Sawaya pudo producir un modelo más exacto de su estructura basado en múltiples cristales de dímeros de actina que se unen en diferentes lugares. [15] Este modelo ha sido posteriormente refinado por Sawaya y Lorenz. Otros enfoques, como el uso de microscopía crioelectrónica y la radiación de sincrotrón, han permitido recientemente aumentar la resolución y comprender mejor la naturaleza de las interacciones y los cambios conformacionales implicados en la formación de filamentos de actina. [16] [17] [18]
Estructura [ editar ]
Su secuencia de aminoácidos es también una de las proteínas mejor conservadas, ya que ha cambiado poco a lo largo del curso de la evolución , diferenciándose en no más del 20% en especies tan diversas como las algas y los seres humanos . [19] Por lo tanto, se considera que tiene una estructura optimizada . [4] Tiene dos características distintivas: es una enzima que hidroliza lentamente la ATP , la "moneda de energía universal" de los procesos biológicos. Sin embargo, la ATP es necesaria para mantener su integridad estructural. Su eficiente estructura está formada por una forma casi única.Proceso de plegado . Además, es capaz de realizar más interacciones que cualquier otra proteína, lo que le permite realizar una variedad más amplia de funciones que otras proteínas en casi todos los niveles de la vida celular. [4] La miosina es un ejemplo de una proteína que se une a la actina. Otro ejemplo es la villina , que puede tejer actina en haces o cortar los filamentos dependiendo de la concentración de cationes de calcio en el medio circundante. [20]
La actina es una de las proteínas más abundantes en los eucariotas , donde se encuentra en todo el citoplasma. [20] De hecho, en las fibras musculares comprende el 20% del total de proteínas celulares en peso y entre el 1% y el 5% en otras células. Sin embargo, no hay un solo tipo de actina; Los genes que codifican la actina se definen como una familia de genes (una familia que en las plantas contiene más de 60 elementos, incluidos los genes y pseudogenes y en los seres humanos más de 30 elementos). [4] [21] Esto significa que la información genética de cada individuo contiene instrucciones que generan variantes de actina (llamadas isoformas) que poseen funciones ligeramente diferentes. Esto, a su vez, significa que los organismos eucariotas expresan diferentes genes que dan lugar a: α-actina, que se encuentra en estructuras contráctiles; β-actina, que se encuentra en el borde en expansión de las células que utilizan la proyección de sus estructuras celulares como sus medios de movilidad; y γ-actina, que se encuentra en los filamentos de las fibras de estrés . [22] Además de las similitudes que existen entre las isoformas de un organismo, también existe una conservación evolutiva en la estructura y función incluso entre los organismos contenidos en diferentes dominios eucarióticos : en las bacterias el homólogo de actina MreBse ha identificado, que es una proteína que es capaz de polimerizar en microfilamentos; [4] [17] y en archaea el homólogo Ta0583 es aún más similar a las actinas eucariotas. [23]
La actina celular tiene dos formas: glóbulos monoméricos llamados actina G y filamentos poliméricos llamados actina F (es decir, como filamentos formados por muchos monómeros de actina G). La actina F también se puede describir como un microfilamento. Dos hebras de actina F paralelas deben girar 166 grados para quedar correctamente una encima de la otra. Esto crea la estructura de doble hélice de los microfilamentos que se encuentran en el citoesqueleto. Los microfilamentos miden aproximadamente 7 nm de diámetro y la hélice se repite cada 37 nm. Cada molécula de actina se une a una molécula de trifosfato de adenosina (ATP) o difosfato de adenosina (ADP) que se asocia con un Mg 2+catión. Las formas más comunes de actina, en comparación con todas las combinaciones posibles, son la ATP-G-Actina y la ADP-F-actina. [24] [25]
G-Actina [ editar ]
Las imágenes de microscopía electrónica de barrido indican que la actina G tiene una estructura globular; sin embargo, la cristalografía de rayos X muestra que cada uno de estos glóbulos está formado por dos lóbulos separados por una hendidura. Esta estructura representa el "pliegue de ATPasa", que es un centro de catálisis enzimática que se une a ATP y Mg2 + e hidroliza el primero a ADP más fosfato . Este pliegue es un motivo estructural conservado que también se encuentra en otras proteínas que interactúan con los nucleótidos trifosfato , como la hexocinasa (una enzima usada en el metabolismo energético ) o en las proteínas Hsp70 (una familia de proteínas que juega un papel importante en el plegamiento de proteínas).[26] La G-actina solo es funcional cuando contiene ADP o ATP en su hendidura, pero la forma que está unida al ATP predomina en las células cuando la actina está presente en su estado libre. [24]
El modelo de actina por cristalografía de rayos X producido por Kabsch a partir del tejido muscular estriado de los conejos es el más utilizado en los estudios estructurales, ya que fue el primero en purificarse . La actina G cristalizada por Kabsch tiene un tamaño aproximado de 67 x 40 x 37 Å , tiene una masa molecular de 41,785 Da y un punto isoeléctrico estimado de 4.8. Su carga neta a pH = 7 es -7. [11] [27]
- Estructura primaria
Elzinga y sus colaboradores determinaron primero la secuencia peptídica completa para este tipo de actina en 1973, y el trabajo posterior del mismo autor agregó más detalles al modelo. Contiene 374 residuos de aminoácidos. Su extremo N es altamente ácido y comienza con un aspartato acetilado en su grupo amino. Mientras que su término C es alcalino y está formado por una fenilalaninaprecedida por una cisteína , que tiene un grado de importancia funcional. Ambos extremos están muy cerca del subdominio I. Una N τ -metilhistidina anómalase encuentra en la posición 73. [27]
- Estructura terciaria - dominios
La estructura terciaria está formada por dos dominiosconocidos como grande y pequeño, que están separados por una hendidura centrada alrededor de la ubicación del enlace con ATP - ADP + P i . Debajo de esto hay una muesca más profunda llamada "surco". En el estado nativo , a pesar de sus nombres, ambos tienen una profundidad comparable. [11]
La convención normal en topología.estudios significa que una proteína se muestra con el dominio más grande en el lado izquierdo y el dominio más pequeño en el lado derecho. En esta posición, el dominio más pequeño se divide a su vez en dos: subdominio I (posición inferior, residuos 1-32, 70-144 y 338-374) y subdominio II (posición superior, residuos 33-69). El dominio más grande también se divide en dos: subdominio III (inferior, residuos 145-180 y 270-337) y subdominio IV (superior, residuos 181-269). Las áreas expuestas de los subdominios I y III se conocen como los extremos "de púas", mientras que las áreas expuestas de los dominios II y IV se denominan los extremos "en punta". Esta nomenclatura se refiere al hecho de que, debido a la pequeña masa de subdominio La actina II es polar, la importancia de esto se discutirá más adelante en la discusión sobre la dinámica de ensamblaje. Algunos autores llaman a los subdominios Ia, Ib, IIa y IIb.[28]
- Otras estructuras importantes
La estructura supersecundaria más notable es una hoja beta de cinco cadenas que se compone de un β-meandro y una β-α-β en el sentido de las agujas del reloj. Está presente en ambos dominios, lo que sugiere que la proteína surgió de la duplicación de genes. [12]
- El sitio de unión al nucleótido de adenosina está ubicado entre dos estructuras en forma de horquilla betapertenecientes a los dominios I y III. Los residuos que están involucrados son Asp11-Lys18 y Asp154-His161 respectivamente.
- El sitio de unión al catión divalente está ubicado justo debajo del nucleótido de adenosina. In vivo , la mayoría de las veces está formado por Mg 2+ o Ca 2+, mientras que in vitro está formado por una estructura quelante formada por Lys18 y dos oxígenos de los fosfatos α y β del nucleótido . Este calcio está coordinado con seis moléculas de agua que son retenidas por los aminoácidos Asp11 , Asp154 y Gln137.. Forman un complejo con el nucleótido que restringe los movimientos de la llamada región "bisagra", ubicada entre los residuos 137 y 144. Esto mantiene la forma nativa de la proteína hasta que su retiro desnaturaliza el monómero de actina. Esta región también es importante porque determina si la hendidura de la proteína está en la conformación "abierta" o "cerrada". [1] [28]
- Es muy probable que haya al menos otros tres centros con una menor afinidad (intermedio) y otros con una baja afinidad por los cationes divalentes. Se ha sugerido que estos centros pueden desempeñar un papel en la polimerización de la actina al actuar durante la etapa de activación. [28]
- Hay una estructura en el subdominio 2 que se denomina "bucle D" porque se enlaza con la DNasa I , se encuentra entre los residuos His40 y Gly48 . Tiene la apariencia de un elemento desordenado en la mayoría de los cristales, pero se parece a una lámina β cuando está complejada con DNasa I. Se ha propuesto que el evento clave en la polimerización es probablemente la propagación de un cambio conformacional a partir de Centro del enlace con el nucleótido de este dominio, que cambia de un bucle a una espiral. [1] Sin embargo, esta hipótesis ha sido refutada por otros estudios. [29]
F-actina [ editar ]
La descripción clásica de F-actina indica que tiene una estructura filamentosa que puede considerarse una hélice levorotatoria monocatenaria con una rotación de 166 ° alrededor del eje helicoidal y una traslación axial de 27.5 Å , o una hélice dextrorotatoria monocatenaria con un espaciamiento cruzado de 350-380 Å, con cada actina rodeada por cuatro más. [30] La simetría del polímero de actina en 2.17 subunidades por giro de una hélice es incompatible con la formación de cristales , que solo es posible con una simetría de exactamente 2, 3, 4 o 6 subunidades por turno. Por lo tanto, se deben construir modelos que expliquen estas anomalías utilizando datos de microscopía electrónica., Crio-microscopía electrónica , la cristalización de dímeros en diferentes posiciones y de difracción de rayos-X . [17] [18] Cabe señalar que no es correcto hablar de una "estructura" para una molécula tan dinámica como el filamento de actina. En realidad, hablamos de distintos estados estructurales, en estos casos, la medición de la traslación axial permanece constante en 27.5 Å, mientras que los datos de rotación de la subunidad muestran una variabilidad considerable, con desplazamientos de hasta el 10% desde su posición óptima comúnmente vista. Algunas proteínas, como la cofilina, parecen aumentar el ángulo de giro, pero nuevamente esto podría interpretarse como el establecimiento de diferentes estados estructurales. Estos podrían ser importantes en el proceso de polimerización. [31]
Hay menos acuerdo con respecto a las mediciones del radio de giro y del grosor del filamento: mientras que los primeros modelos asignaron una longitud de 25 Å, los datos actuales de difracción de rayos X, respaldados por microscopía crioelectrónica sugieren una longitud de 23.7 Å. Estos estudios han demostrado los puntos de contacto precisos entre los monómeros. Algunos se forman con unidades de la misma cadena, entre el extremo "de púas" en un monómero y el extremo "en punta" del siguiente. Mientras que los monómeros en las cadenas adyacentes hacen contacto lateral a través de proyecciones del subdominio IV, siendo las proyecciones más importantes las formadas por el extremo C y el enlace hidrófobo formado por tres cuerpos que involucran los residuos 39-42, 201-203 y 286. Este modelo sugiere que un filamento está formado por monómeros en una formación de "hoja", en la que los subdominios giran sobre sí mismos,MreB . [17]
Se considera que el polímero de actina F tiene polaridad estructural debido al hecho de que todas las subunidades de microfilamento apuntan hacia el mismo extremo. Esto da lugar a una convención de denominación: el extremo que posee una subunidad de actina que tiene su sitio de unión ATP expuesto se denomina "(-) final", mientras que el extremo opuesto, donde la hendidura se dirige a un monómero adyacente diferente, se denomina " (+) fin ". [22] Los términos "en punta" y "púa" que se refieren a los dos extremos de los microfilamentos derivan de su aparición bajo microscopía electrónica de transmisión cuando las muestras se examinan siguiendo una técnica de preparación llamada "decoración".. Esta miosina forma enlaces polares con monómeros de actina, dando lugar a una configuración que parece flechas con estiramientos de plumas a lo largo de su eje, donde el eje es la actina y los estiramientos son la miosina. Siguiendo esta lógica, el final del microfilamento que no tiene ninguna miosina sobresaliente se llama el punto de la flecha (- extremo) y el otro extremo se llama el extremo de púas (+ extremo). [32] Un fragmento S1 está compuesto por los dominios de cabeza y cuello de la miosina II . En condiciones fisiológicas, la G-actina (la forma del monómero ) se transforma en F-actina (la forma del polímero ) por el ATP, donde el papel del ATP es esencial. [33]
El filamento helicoidal de actina F que se encuentra en los músculos también contiene una molécula de tropomiosina , que es una proteína de 40 nanómetros de largo que se envuelve alrededor de la hélice de actina F. [18] Durante la fase de reposo, la tropomiosina cubre los sitios activos de la actina, por lo que la interacción actina-miosina no puede tener lugar y producir una contracción muscular. Hay otras moléculas de proteínas unidas a la rosca tropomiosina, éstas son las troponinas que tienen tres polímeros: troponina I , troponina T y troponina C . [34]
Plegado [ editar ]
La actina puede adquirir espontáneamente una gran parte de su estructura terciaria . [36] Sin embargo, la forma en que adquiere su forma completamente funcional a partir de su forma nativa recién sintetizada es especial y casi única en la química de proteínas. El motivo de esta ruta especial podría ser la necesidad de evitar la presencia de monómeros de actina plegados incorrectamente, que podrían ser tóxicos, ya que pueden actuar como terminadores de polimerización ineficientes. Sin embargo, es clave para establecer la estabilidad del citoesqueleto y, además, es un proceso esencial para coordinar el ciclo celular . [37] [38]
Se requiere CCT para garantizar que el plegado se realice correctamente. La TCC es una chaperona molecular citosólica del grupo II (o chaperonina, una proteína que ayuda en el plegamiento de otras estructuras macromoleculares). La TCC está formada por un anillo doble de ocho subunidades diferentes (heterooctaméricas) y se diferencia de otras chaperonas moleculares, particularmente de su homólogo GroELque se encuentra en la Archaea , ya que no requiere que una co-chaperona actúe como una tapa Sobre la cavidad catalítica central . Los sustratos se unen a CCT a través de dominios específicos. Inicialmente se pensó que solo se unía con actina y tubulina , aunque la inmunoprecipitación recientelos estudios han demostrado que interactúa con un gran número de polipéptidos , que posiblemente funcionan como sustratos . Actúa a través de cambios conformacionales dependientes de ATP que en ocasiones requieren varias rondas de liberación y catálisis para completar una reacción. [39]
Para completar con éxito su plegamiento, tanto la actina como la tubulina necesitan interactuar con otra proteína llamada prefoldina , que es un complejo heterohexamérico (formado por seis subunidades distintas), en una interacción tan específica que las moléculas han coevolucionado [ cita requerida ] . Los complejos de actina con prefoldina mientras aún se está formando, cuando tiene aproximadamente 145 aminoácidos de longitud, específicamente aquellos en el extremo N-terminal. [40]
Se utilizan diferentes subunidades de reconocimiento para la actina o la tubulina, aunque existe cierta superposición. En la actina, las subunidades que se unen con la prefoldina son probablemente PFD3 y PFD4, que se unen en dos lugares, uno entre los residuos 60-79 y el otro entre los residuos 170-198. La actina se reconoce, se carga y se entrega a la chaperonina citosólica (CCT) en una conformación abierta por el extremo interior de los "tentáculos" del prefoldín (ver la imagen y la nota). [36] El contacto cuando se administra la actina es tan breve que El complejo terciario no se forma, liberando inmediatamente el prefoldín. [35]
El CCT luego causa el plegamiento secuencial de la actina formando enlaces con sus subunidades en lugar de simplemente encerrarlo en su cavidad. [41] Es por esto que posee áreas de reconocimiento específicas en su dominio β apical. La primera etapa en el plegado consiste en el reconocimiento de los residuos 245-249. A continuación, otros determinantes establecen contacto. [42] Tanto la actina como la tubulina se unen a CCT en conformaciones abiertas en ausencia de ATP. En el caso de la actina, dos subunidades se unen durante cada cambio conformacional, mientras que para la tubulina se lleva a cabo con cuatro subunidades. La actina tiene secuencias de unión específicas, que interactúan con las subunidades δ y β-CCT o con δ-CCT y ε-CCT. Después de que AMP-PNP se une a CCT, los sustratos se mueven dentro de la cavidad del chaperonin. También parece que en el caso de la actina, laLa proteína CAP se requiere como un posible cofactor en los estados finales de plegamiento de la actina. [38]
La manera exacta por la cual este proceso está regulado aún no se entiende completamente, pero se sabe que la proteína PhLP3 (una proteína similar a la fosducina ) inhibe su actividad a través de la formación de un complejo terciario. [39]
Mecanismo catalítico de la ATPasa [ editar ]
La actina es una ATPasa , lo que significa que es una enzima que hidroliza el ATP. Este grupo de enzimas se caracteriza por sus lentas tasas de reacción. Se sabe que esta ATPasa está "activa", es decir, su velocidad aumenta unas 40,000 veces cuando la actina forma parte de un filamento. [31] Un valor de referencia para esta tasa de hidrólisis en condiciones ideales es de alrededor de 0,3 s -1 . Luego, la P i permanece unida a la actina junto al ADP durante mucho tiempo, hasta que se libera de forma cooperativa del interior del filamento. [43] [44]
Los detalles moleculares exactos del mecanismo catalítico todavía no se entienden completamente. Aunque hay mucho debate sobre este tema, parece seguro que se requiere una conformación "cerrada" para la hidrólisis de ATP, y se piensa que los residuos que están involucrados en el proceso se mueven a la distancia apropiada. [31]El ácido glutámico Glu137 es uno de los residuos clave, que se encuentra en el subdominio 1. Su función es unir la molécula de agua que produce un ataque nucleófilo en el enlace γ-fosfato del ATP, mientras que el nucleótido está fuertemente unido a los subdominios 3 y 4. La lentitud del proceso catalítico se debe a la gran distancia y la posición sesgada de la molécula de agua en relación con el reactivo. Es muy probable que el cambio conformacional producido por la rotación de los dominios entre las formas G y F de la actina haga que el Glu137 se acerque más y permita su hidrólisis. Este modelo sugiere que la polimerización y la función de la ATPasa se desacoplarían de inmediato. [17] [18] La transformación "abierta" a "cerrada" entre las formas G y F y sus implicaciones sobre el movimiento relativo de varios residuos clave y la formación de cables de agua se han caracterizado en la dinámica molecular y en las simulaciones QM / MM .




No hay comentarios:
Publicar un comentario