Funciones y ubicación [ editar ]
La actina forma filamentos ('F-actina' o microfilamentos ) que son elementos esenciales del citoesqueletoeucariota , capaces de experimentar una dinámica de polimerización y despolimerización muy rápida. En la mayoría de las células, los filamentos de actina forman redes de mayor escala que son esenciales para muchas funciones clave en las células: [74]
- Varios tipos de redes de actina (hechas de filamentos de actina) brindan soporte mecánico a las células y proporcionan rutas de tráfico a través del citoplasma para ayudar a la transducción de señales.
- El rápido montaje y desmontaje de la red de actina permite que las células migren ( migración de células ).
- En las células musculares metazoarias , es el andamio sobre el cual las proteínas de la miosina generan fuerza para apoyar la contracción muscular.
- En células no musculares, será una pista para el transporte de carga miosinas (miosinas no convencionales) como la miosina V y VI. Las miosinas no convencionales utilizan la hidrólisis de ATP para transportar carga, como vesículas y orgánulos, de forma dirigida mucho más rápido que la difusión. La miosina V camina hacia el extremo de púas de los filamentos de actina, mientras que la miosina VI camina hacia el extremo puntiagudo. La mayoría de los filamentos de actina están dispuestos con el extremo barbado hacia la membrana celular y el extremo puntiagudo hacia el interior celular. Esta disposición permite que la miosina V sea un motor efectivo para la exportación de cargas, y la miosina VI sea un motor efectivo para la importación.
La proteína actina se encuentra tanto en el citoplasma como en el núcleo celular . [75] Su ubicación está regulada por las vías de transducción de señales de la membrana celular que integran los estímulos que recibe una célula estimulando la reestructuración de las redes de actina en respuesta. En Dictyostelium , se ha encontrado que la fosfolipasa D interviene en las vías del inositol fosfato . [76] Los filamentos de actina son particularmente estables y abundantes en las fibras musculares . Dentro del sarcomero(la unidad morfológica y fisiológica básica de las fibras musculares) la actina está presente en las bandas I y A; La miosina también está presente en este último. [77]
Citoesqueleto [ editar ]
Los microfilamentos participan en el movimiento de todas las células móviles, incluidos los tipos no musculares, y los fármacos que interrumpen la organización de la actina F (como las citocalasinas ) afectan la actividad de estas células. La actina comprende el 2% de la cantidad total de proteínas en los hepatocitos , el 10% en los fibroblastos, el 15% en las amebas y hasta el 50-80% en las plaquetas activadas . [78] Hay varios tipos diferentes de actina con estructuras y funciones ligeramente diferentes. Esto significa que la α-actina se encuentra exclusivamente en las fibras musculares., mientras que los tipos β y γ se encuentran en otras células. Además, como los últimos tipos tienen una alta tasa de rotación, la mayoría de ellos se encuentran fuera de las estructuras permanentes. Esto significa que los microfilamentos encontrados en células distintas a las células musculares están presentes en dos formas: [79]
- Redes de microfilamento : las células animales comúnmente tienen una corteza celular debajo de la membrana celular que contiene un gran número de microfilamentos, lo que excluye la presencia de orgánulos. Esta red está conectada con numerosas células receptoras que retransmiten señales al exterior de una célula.
- Paquetes de microfilamentos : estos microfilamentos extremadamente largos se encuentran en redes y, en asociación con proteínas contráctiles como la miosina no muscular , están involucrados en el movimiento de sustancias a nivel intracelular.
- Anillos de actina periódicos : una estructura periódica construida con anillos de actina uniformemente espaciados se encuentra específicamente en los axones (no en las dendritas ). [80] En esta estructura, los anillos de actina, junto con los tetrámeros de espectrina que enlazan los anillos de actina vecinos, forman un citoesqueleto cohesivo que soporta la membrana del axón. La periodicidad de la estructura también puede regular los canales de iones de sodio en los axones.
Levaduras [ editar ]
El citoesqueleto de actina es clave para los procesos de endocitosis , citocinesis , determinación de la polaridad celular y morfogénesis en levaduras . Además de confiar en la actina, estos procesos implican 20 o 30 proteínas asociadas, todas ellas con un alto grado de conservación evolutiva, junto con muchas moléculas de señalización. Juntos, estos elementos permiten un ensamblaje espacial y temporalmente modulado que define la respuesta de una célula a los estímulos internos y externos. [81]
Las levaduras contienen tres elementos principales asociados con la actina: parches, cables y anillos que, a pesar de estar presentes durante mucho tiempo, están sujetos a un equilibrio dinámico debido a la continua polimerización y despolimerización. Poseen varias proteínas accesorias que incluyen ADF / cofilina, que tiene un peso molecular de 16 kDa y está codificada por un solo gen, llamado COF1 ; Aip1, un cofactor de cofilina que promueve el desmontaje de los microfilamentos; Srv2 / CAP, un regulador del proceso relacionado con las proteínas adenilato ciclasa ; una profilina con un peso molecular de aproximadamente 14 kDa que se asocia con monómeros de actina; y twinfilin, una proteína de 40 kDa involucrada en la organización de parches. [81]
Plantas [ editar ]
Los estudios del genoma de las plantas han revelado la existencia de proteínas isovariantes dentro de la familia de genes de la actina. Dentro de Arabidopsis thaliana , un dicotiledóneo utilizado como organismo modelo , hay diez tipos de actina, nueve tipos de α-tubulinas, seis β-tubulinas, seis profilinas y docenas de miosinas. Esta diversidad se explica por la necesidad evolutiva de poseer variantes que difieren ligeramente en su expresión temporal y espacial. [4] La mayoría de estas proteínas se expresaron conjuntamente en el tejido analizado. Las redes de actina se distribuyen en todo el citoplasma de las células que se han cultivado in vitro.. Hay una concentración de la red alrededor del núcleo que está conectada a través de radios a la corteza celular, esta red es altamente dinámica, con una polimerización y despolimerización continuas. [82]
Aunque la mayoría de las células vegetales tienen una pared celular que define su morfología e impide su movimiento, sus microfilamentos pueden generar suficiente fuerza para lograr una serie de actividades celulares, como las corrientes citoplásmicas generadas por los microfilamentos y la miosina. La actina también participa en el movimiento de los orgánulos y en la morfogénesis celular, que involucra la división celular , así como la elongación y diferenciación de la célula. [84]
Las proteínas más notables asociadas con el citoesqueleto de actina en las plantas incluyen: [84] villina , que pertenece a la misma familia que la gelsolina / severina y es capaz de cortar microfilamentos y unirse a monómeros de actina en presencia de cationes de calcio; fimbrina , que es capaz de reconocer y unir los monómeros de actina y que está involucrada en la formación de redes (mediante un proceso de regulación diferente al de los animales y las levaduras); [85] forminas , que son capaces de actuar como un agente de nucleación de polimerización de actina F; La miosina , un motor molecular típico que es específico de los eucariotas y que en Arabidopsis thalianaestá codificado por 17 genes en dos clases distintas; CHUP1, que puede unirse a la actina y está implicada en la distribución espacial de los cloroplastos en la célula; KAM1 / MUR3 que define la morfología del aparato de Golgi, así como la composición de los xiloglucanos en la pared celular; NtWLIM1, que facilita la aparición de estructuras celulares de actina; y ERD10, que participa en la asociación de orgánulos dentro de membranas y microfilamentos y que parece desempeñar un papel que está involucrado en la reacción de un organismo al estrés .
Actina nuclear [ editar ]
La actina nuclear fue notada y descrita por primera vez en 1977 por Clark y Merriam. [86] Los autores describen una proteína presente en la fracción nuclear, obtenida de ovocitos de Xenopus laevis , que muestra las mismas características que la actina del músculo esquelético. Desde entonces, ha habido muchos informes científicos sobre la estructura y las funciones de la actina en el núcleo (para una revisión, véase: Hofmann 2009. [87] ) El nivel controlado de actina en el núcleo, su interacción con las proteínas de unión a la actina (ABP) y la presencia de diferentes isoformas permite que la actina desempeñe un papel importante en muchos procesos nucleares importantes.
Transporte de actina a través de la membrana nuclear [ editar ]
La secuencia de actina no contiene una señal de localización nuclear. El pequeño tamaño de la actina (aproximadamente 43 kDa) le permite ingresar al núcleo por difusión pasiva. [88] Sin embargo, la actina se transporta entre el citoplasma y el núcleo con bastante rapidez, lo que indica la existencia de transporte activo. La importación de actina en el núcleo (probablemente en un complejo con cofilina) se ve facilitada por la proteína importin importin 9. [89]
El bajo nivel de actina en el núcleo parece ser muy importante, porque la actina tiene dos señales de exportación nuclear (NES) en su secuencia. La actina microinyectada se elimina rápidamente del núcleo al citoplasma. La actina se exporta al menos de dos maneras, a través de exportin 1 (EXP1) y exportin 6 (Exp6). [90] [91]
Las modificaciones específicas, como la SUMOilación, permiten la retención de actina nuclear. Se demostró que una mutación que previene la SUMOilación provoca una rápida exportación de beta actina desde el núcleo. [92]
Sobre la base de los resultados experimentales, se puede proponer un mecanismo general de transporte de actina nuclear: [92] [93]
- En el citoplasma la cofilina se une a los monómeros de actina ADP. Este complejo se importa activamente en el núcleo.
- Una mayor concentración de ATP en el núcleo (en comparación con el citoplasma) promueve el intercambio de ADP a ATP en el complejo actina-cofilina. Esto debilita la fuerza de unión de estas dos proteínas.
- El complejo de cofilina-actina finalmente se disocia después de la fosforilación de la cofilina por la quinasa LIM nuclear.
- La actina es SUMOylated y en esta forma se conserva dentro del núcleo.
- La actina puede formar complejos con profilina y dejar el núcleo a través de la exportación 6.
La organización de la actina nuclear [ editar ]
La actina nuclear existe principalmente como un monómero, pero también puede formar oligómeros dinámicos y polímeros cortos. [94] [95] [96] La organización de la actina nuclear varía en diferentes tipos de células. Por ejemplo, en los ovocitos de Xenopus (con un nivel de actina nuclear más alto en comparación con las células somáticas), la actina forma filamentos, que estabilizan la arquitectura del núcleo. Estos filamentos se pueden observar bajo el microscopio gracias a la tinción con faloidina conjugada con fluoróforos. [86] [88]
En el núcleo de células somáticas, sin embargo, no podemos observar ningún filamento de actina utilizando esta técnica. [97] El ensayo de inhibición de la ADNasa I, hasta ahora la única prueba que permite la cuantificación de la actina polimerizada directamente en muestras biológicas, ha revelado que la actina nuclear endógena se produce principalmente en forma monomérica. [96]
El nivel de actina controlado con precisión en el núcleo celular, más bajo que en el citoplasma, evita la formación de filamentos. La polimerización también se reduce por el acceso limitado a los monómeros de actina, que se unen en complejos con ABPs, principalmente cofilina. [93]
Isoformas de actina en el núcleo celular [ editar ]
Se presta poca atención a las isoformas de actina, sin embargo, se ha demostrado que diferentes isoformas de actina están presentes en el núcleo celular. Las isoformas de actina, a pesar de su alta similitud de secuencia, tienen diferentes propiedades bioquímicas, como la cinética de polimerización y despolimerización. [98] También muestran diferentes localizaciones y funciones.
El nivel de isoformas de actina, tanto en el citoplasma como en el núcleo, puede cambiar, por ejemplo, en respuesta a la estimulación del crecimiento celular o la detención de la proliferación y la actividad transcripcional. [99]
Las inquietudes de investigación sobre la actina nuclear suelen centrarse en la isoforma beta. [100] [101] [102] [103]Sin embargo, el uso de anticuerpos dirigidos contra diferentes isoformas de actina permite identificar no solo el beta citoplasmático en el núcleo celular, sino también:
- gamma actina en los núcleos celulares del melanoma humano, [96]
- Actina del músculo esquelético alfa en los núcleos de los mioblastos de ratón, [104]
- La gamma actina citoplásmica y también la actina del músculo liso alfa en el núcleo del fibroblasto de ratón fetal [105]
La presencia de diferentes isoformas de actina puede tener un efecto significativo en su función en los procesos nucleares, especialmente porque el nivel de las isoformas individuales se puede controlar de forma independiente. [96]
Funciones de actina nuclear [ editar ]
Las funciones de la actina en el núcleo están asociadas con su capacidad de polimerización, interacción con la variedad de ABP y con elementos estructurales del núcleo. La actina nuclear está involucrada en:
- Arquitectura del núcleo : la interacción de la actina con la espectrina alfa II y otras proteínas es importante para mantener la forma adecuada del núcleo [106] [107] Existe una conexión dinámica entre la actina y el núcleo celular a través de las proteínas del dominio KASH. La envoltura y la interrupción de esta conexión conducen a un cambio en la morfología nuclear. [108]
- Transcripción - la actina participa en la reorganización de la cromatina. [75] [100] [109] [110] el inicio de la transcripción e interactúa con el complejo de transcripción. [111] La actina participa en la regulación de la estructura de la cromatina [112] [113] [114] interactúa con la ARN polimerasa I, [103] II [101] y III [102] En la transcripción de Pol I, actina y miosina ( MYO1C , que se une al ADN) actúa como un motor molecular. Para la transcripción de Pol II, la β-actina es necesaria para la formación del complejo de preiniciación. Pol III contiene β-actina como una subunidad. La actina también puede ser un componente de los complejos de remodelación de la cromatina, así como las partículas pre-mRNP (es decir, el ARN mensajero precursor incluido en las proteínas), y está involucrado en la exportación nuclear de ARN y proteínas. [115]
- Regulación de la actividad de los genes : la actina se une a las regiones reguladoras de diferentes tipos de genes [116] [117] [118] [119] La capacidad de actina para regular la actividad de los genes se utiliza en el método de reprogramación molecular, que permite que las células diferenciadas vuelvan a su estado embrionario estado [118] [120]
- Translocación del fragmento de cromosoma activado desde la región de la membrana a la eucromatina, donde comienza la transcripción. El movimiento requiere la interacción de actina y miosina [121] [122]
- Integración de diferentes compartimentos celulares . La actina es una molécula que integra la vía de transducción de señales citoplásmicas y nucleares. [123] Un ejemplo es la activación de la transcripción en respuesta a la estimulación del suero de células in vitro . [124] [125] [126]
- Respuesta inmune : la actina nuclear se polimeriza con la estimulación del receptor de células T y se requiere para la expresión de citoquinas y la producción de anticuerpos in vivo . [127]
Debido a su capacidad para los cambios conformacionales y la interacción con muchas proteínas, la actina actúa como un regulador de la formación y la actividad de complejos de proteínas como el complejo transcripcional. [111]
Contracción muscular [ editar ]
Esquema de una contracción muscular [ editar ]
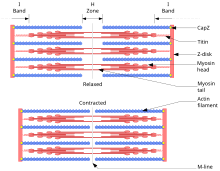
En las células musculares, las miofibrillas de actomiosina componengran parte del material citoplásmico. Estas miofibrillas están hechas de filamentos finos de actina (típicamente de alrededor de 7 nm de diámetro) y filamentos gruesos de la miosina de proteína motora (típicamente de alrededor de 15 nm de diámetro). [128] Estas miofibrillas usan energía derivada de ATP para crear movimientos de las células, como la contracción muscular . [128] Usando la hidrólisis de ATP para obtener energía, las cabezas de miosina experimentan un ciclo durante el cual se unen a los filamentos delgados, ejercen una tensión y luego, dependiendo de la carga, realizan un golpe de energía que hace que los filamentos delgados se deslicen, acortándose el músculo.
En los paquetes contráctiles, la proteína alfa- actinina que contiene la actina separa cada filamento delgado en ± 35 nm. Este aumento en la distancia permite que los filamentos gruesos entren e interactúen entre sí, permitiendo la deformación o contracción. En la deformación, un extremo de la miosina se une a la membrana plasmática , mientras que el otro "camina" hacia el extremo positivo del filamento de actina. Esto lleva a la membrana a una forma diferente en relación con la corteza celular. Para la contracción, la molécula de miosina generalmente está unida a dos filamentos separados y ambos extremos "caminan" simultáneamente hacia el extremo positivo de su filamento, deslizando los filamentos de actina más cerca uno del otro. Esto resulta en el acortamiento, o contracción, del paquete de actina (pero no el filamento). Este mecanismo es responsable de la contracción muscular y la citocinesis , la división de una célula en dos.
El papel de la actina en la contracción muscular [ editar ]
El filamento helicoidal de actina F que se encuentra en los músculos también contiene una molécula de tropomiosina , una proteína de 40 nanómetros que se envuelve alrededor de la hélice de actina F. Durante la fase de reposo, la tropomiosina cubre los sitios activos de la actina de modo que la interacción actina-miosina no puede tener lugar y produce una contracción muscular (la interacción da lugar a un movimiento entre las dos proteínas que, al repetirse muchas veces, produce una contracción) . Hay otras moléculas de proteínas unidas a la rosca tropomiosina, estos incluyen las troponinas que tienen tres polímeros: I troponina , la troponina T y troponina C . [34]La función reguladora de la tropomiosina depende de su interacción con la troponina en presencia de iones Ca 2+ . [129]
Tanto la actina como la miosina participan en la contracción muscular y la relajación y constituyen el 90% de las proteínas musculares. [130] El proceso general se inicia mediante una señal externa, generalmente a través de un potencial de acción que estimula al músculo, que contiene células especializadas cuyos interiores son ricos en filamentos de actina y miosina. El ciclo de contracción-relajación comprende los siguientes pasos: [77]
- La despolarización de la sarcolema y transmisión de un potencial de acción a través de los túbulos T .
- Apertura del retículo sarcoplásmico ‘s Ca 2+ canales.
- Aumento de las concentraciones de Ca 2+ citosólico y la interacción de estos cationes con la troponina causando un cambio conformacional en su estructura . Esto, a su vez, altera la estructura de la tropomiosina, que cubre el sitio activo de la actina, lo que permite la formación de enlaces cruzados de miosina-actina (esta última está presente como filamentos delgados). [34]
- El movimiento de las cabezas de miosina sobre los filamentos delgados, puede implicar ATP o ser independiente de ATP. El mecanismo anterior, mediada por ATPasa actividad en las cabezas de miosina, provoca el movimiento de los filamentos de actina hacia el Z-disco .
- Captura de Ca 2+ por el retículo sarcoplásmico, causando un nuevo cambio conformacional en la tropomiosina que inhibe la interacción actina-miosina.


No hay comentarios:
Publicar un comentario