Diagramas epónimos
diagrama de Moeller.
Para comprender el diagrama, utiliza la siguiente tabla:
| h | s | p | d | f |
|---|---|---|---|---|
Para encontrar la distribución electrónica se escriben las notaciones en forma diagonal desde arriba hacia abajo y de derecha a izquierda (seguir colores):
Obtención del diagrama de Moeller:
El Diagrama de Moeller recopila en una tabla una serie de datos que proporcionan los números cuánticos n (nivel de orbitales), l (Caracterización del orbital, s, p, d o f),m (orientación del orbital en el espacio), y s (espín, igual siempre a +1/2 ó -1/2).
Salvo en el caso de s, los valores de todos los números cuánticos se obtienen a partir del valor de n:
- n: NÚMERO CUÁNTICO PRINCIPAL (n), toma valores enteros positivos {1,2,3,4...}n c Z(+), ya que es el "número del nivel".
- l: NÚMERO CUÁNTICO DEL MOMENTO ANGULAR ORBITAL (l), toma todos los valores enteros desde 0 hasta (n-1) → {0,1,2,...,(n-1)}; n c Z. Caracteriza el tipo de orbital en función del nivel, n.
- m: NÚMERO CUÁNTICO MAGNÉTICO (m), toma todos los valores enteros desde (-l) hasta (+l) (incluidos los extremos) → {(-l),...,0,...,(+l)}n c Z. Indica la orientación espacial del orbital,cir todas sus características:
- n=1 (primer nivel de orbitales):
-
- l =0 → Esto da orbitales de tipo s (llamados así por la palabra sharp)
-
- m=0 → Un valor, una orientación, con lo que sólo hay un orbital tipo s en el nivel 1 (n=1). El orbital es, por lo tanto llamado 1s (se le añada como prefijo el valor de n). ya que en el
-
- s= +1/2.
- n=2 (segundo nivel de orbitales):
- l=0,1:
- l=0 indica orbitales tipo s, y siempre hay uno porque para l=0, m sólo tiene un valor, 0 → El orbital es 2s.
- l=1 indica orbitales tipo p, y siempre hay 3, tantos como valores de m ({-1,0,+1}), y hay uno por cada dirección o eje en el espacio: 2px, 2py y 2pz. Llamados p de la palabra principal.
-
- m: (ya calculado)
- s: (se mantiene con sus dos mismos valores, que tienen que ver con el espín de los electrones, no con los orbitales).
- n=3 (tercer nivel de orbitales):
-
- l=0,1,2:
- l=0, como ya se calculó, nos da un orbital s→ 3s.
- l=1, como ya se calculó, da 3 orbitales p→ 3px, 3py y 3pz.
- l=2 indica orbitales d, y hay 5, pues m= -2,-1,0,+1,+2. Reciben los nombres: 3dz^2, 3dx^2y^2, 3dy^2z^2, 3dxy, 3dyz. Llamados d de la palabra diffuse.
- n=4 (cuarto nivel de orbitales):
- l=0,1,2,3:
- * l=0 → 4s.
- l=1 → 4px, 4py y 4pz.
- l=2 → 4dz^2, 4dx^2y^2, 4dy^2z^2, 4dxy, 4dyz.
- l=3 indica orbitales tipo f, y hay 7, pues m = -3,-2,-1,0,+1,+2,+3, con lo que hay 7 orbitales 4f. Llamados f de la palabra fundamental.
Así, y teniendo en cuenta que cada orbital tiene un máximo de 2 electrones, según el principio de exclusión de Pauli, éstos son los orbitales existentes en la configuración electrónica de los átomos, recogida de forma más sencilla en el diagrama de Moeller. Si bien hay más niveles, y, por lo tanto, más valores posibles para l, no existen en la práctica más tipos de orbitales, ya que, hasta la fecha, no ha sido descubierto ningún elemento químico cuyos átomos tengan tan elevado número de electrones como para requerir otro tipo más de orbital, algo también influido por el orden de llenado de los orbitales (véase el diagrama de Moeller, más arriba).

diagrama de Moody es la representación gráfica en escala doblemente logarítmica del factor de fricción en función del número de Reynolds y la rugosidad relativa de una tubería, diagrama hecho por Lewis Ferry Moody.
En la ecuación de Darcy-Weisbach aparece el término 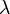 que representa el factor de fricción de Darcy, conocido también como coeficiente de fricción. El cálculo de este coeficiente no es inmediato y no existe una única fórmula para calcularlo en todas las situaciones posibles.
que representa el factor de fricción de Darcy, conocido también como coeficiente de fricción. El cálculo de este coeficiente no es inmediato y no existe una única fórmula para calcularlo en todas las situaciones posibles.
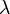 que representa el factor de fricción de Darcy, conocido también como coeficiente de fricción. El cálculo de este coeficiente no es inmediato y no existe una única fórmula para calcularlo en todas las situaciones posibles.
que representa el factor de fricción de Darcy, conocido también como coeficiente de fricción. El cálculo de este coeficiente no es inmediato y no existe una única fórmula para calcularlo en todas las situaciones posibles.
Se pueden distinguir dos situaciones diferentes, el caso en que el flujo sea laminar y el caso en que el flujo sea turbulento. En el caso de flujo laminar se usa una de las expresiones de la ecuación de Poiseuille; en el caso de flujo turbulento se puede usar la ecuación de Colebrook-White además de algunas otras cómo ecuación de Barr,ecuación de Miller, ecuación de Haaland.
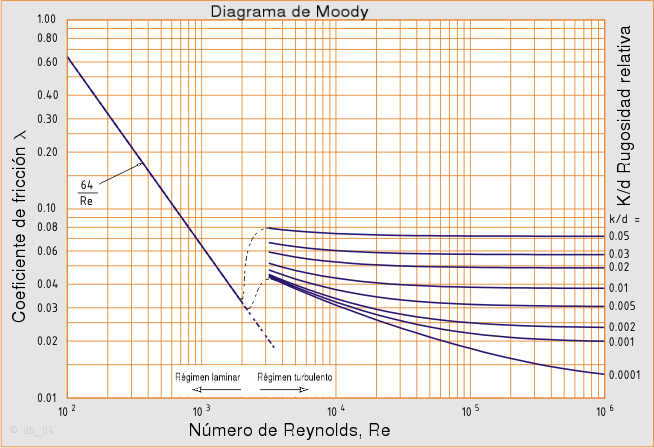
En el caso de flujo laminar el factor de fricción depende únicamente del número de Reynolds. Para flujo turbulento, el factor de fricción depende tanto del número de Reynolds como de la rugosidad relativa de la tubería, por eso en este caso se representa mediante una familia de curvas, una para cada valor del parámetro  , donde k es el valor de la rugosidad absoluta, es decir la longitud (habitualmente en milímetros) de la rugosidad directamente medible en la tubería.
, donde k es el valor de la rugosidad absoluta, es decir la longitud (habitualmente en milímetros) de la rugosidad directamente medible en la tubería.
 , donde k es el valor de la rugosidad absoluta, es decir la longitud (habitualmente en milímetros) de la rugosidad directamente medible en la tubería.
, donde k es el valor de la rugosidad absoluta, es decir la longitud (habitualmente en milímetros) de la rugosidad directamente medible en la tubería.
En la siguiente imagen se puede observar el aspecto del diagrama de Moody.
Expresión matemática
k/D = rugosidad relativa total
Re = Número de Reynolds
λ = factor de fricción
D = diámetro interno de la cañería
k/D = rugosidad relativa
Re = Número de Reynolds
λ = factor de fricción
k/D = rugosidad relativa
Re = Número de Reynolds
λ = factor de fricción
diagrama Nassi-Shneiderman (o NSD por sus siglas en inglés), también conocido como diagrama de Chapin1 2 es una representación gráfica que muestra el diseño de un programa estructurado.
Fue desarrollado en 1972 por Isaac Nassi y Ben Shneiderman. Este diagrama también es conocido como estructograma, ya que sirve para representar la estructura de los programas. Combina la descripción textual del pseudocódigo con la representación gráfica del diagrama de flujo.
Descripción
Basado en un diseño top-down (de lo complejo a lo simple), el problema que se debe resolver se divide en subproblemas cada vez más pequeños - y simples - hasta que solo queden instrucciones simples y construcciones para el control de flujo. El diagrama Nassi-Shneiderman refleja la descomposición del problema en una forma simple usando cajas anidadas para representar cada uno de los subproblemas. Para mantener una consistencia con los fundamentos de la programación estructurada, los diagramas Nassi-Shneiderman no tienen representación para las instrucciones GOTO.
Los diagramas Nassi-Shneiderman se utilizan muy raramente en las tareas de programación formal. Su nivel de abstracción es muy cercano al código de la programación estructurada y ciertas modificaciones requieren que se redibuje todo el diagrama.
Los diagramas Nassi-Shneiderman son (la mayoría de las veces) isomórficos con los diagramas de flujo. Todo lo que se puede representar con un diagrama Nassi-Shneiderman se puede representar con un diagrama de flujo. Las únicas excepciones se dan en las instrucciones GOTO, break y continue.




No hay comentarios:
Publicar un comentario