Acoplamiento de Glaser (1869) es una reacción orgánica, el más antiguo de los acoplamientos acetilénicos, consiste en la reacción de sales del ion cuproso, tales como bromuro de cobre (I), y un oxidante, por ejemplo el oxígeno triplete. La base utilizada en la reacción original es amoniaco.1 2
Mecanismo
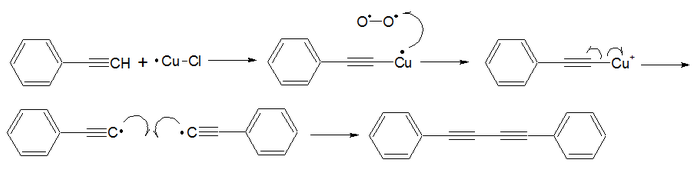
El mecanismo comienza con la desprotonación del extremo alquilacetilénico por acción del ion cuproso, dando como resultado el alquilacetiluro cuproso. Este intermediario se oxida al ion cúprico (Cu III) con el oxígeno triplete, por lo que da inicio a una reacción de radicales libres:3
- Iniciación: Se rompe el enlace Carbono-Cobre, recuperando el catión cuproso.
- Propagación: El catión cuproso formado puede reaccionar con otra molécula de alquino.
- Terminación: Dos radicales alquilalquinilo se unen formando un enlace σ.
Acoplamiento de Eglinton
El Acoplamiento de Eglinton4 es una modificación del acoplamiento de Glaser en donde dos alquinos terminales se acoplan directamente, empleando una sal de cobre (II), como por ejemplo acetato de cobre, y piridina como base.
La reacción de Eglinton5 se ha utilizado para sintetizar una serie de antibióticos fúngicos y es importante para la formación de enlaces carbono-carbono a través delacoplamiento oxidativo de alquinos.6
Este procedimiento ha sido utilizado en la síntesis de ciclooctadecenona.7 Otro ejemplo es la síntesis de difenildiacetileno a partir de fenilacetileno.
acoplamiento diazoico (o acoplamiento azoico o copulación diazoica o copulación azoica) es una reacción de sustitución electrófila aromática entre una sal de diazonio y un anillo aromático activado, como pueden ser una anilina o un fenol, siendo el producto de la reacción un azoderivado. Esta reacción es importante en la producción de colorantes (colorantes azoicos) e indicadores de pH, tales como la tartracina o el anaranjado de metilo.
Mecanismo
 |
| Mecanismo animado |
La reacción aldólica de Mukaiyama es la adición nucleofílica de éteres enólicos de sililo a un aldehído, catalizada por ácidos de Lewis, tales como el trifluoruro de boro o el cloruro de titanio.37 38 La reacción aldólica de Mukaiyama no sigue el modelo de Zimmerman-Traxler. Carreira describió una metodología asimétrica particularmente útil con acetales de sililcetena debido a su elevado grado de enantioselectividad y sustratos susceptibles.39
El método funciona con aldehídos alifáticos no ramificados, que suelen ser electrófilos pobres para los procesos asimétricos, catalíticos. Esto puede deberse a la pobre diferenciación electrónica y estérica entre sus enantiocaras.
El proceso aldólico vinílico análogo de Mukaiyama puede ser efectuado en forma catalítica y asimétrica. El ejemplo mostrado a continuación funciona eficientemente para aldehídos aromáticos (pero no alifáticos) y se cree que el mecanismo involucra un dienolato quiral de metal.






No hay comentarios:
Publicar un comentario