registrador de bucle implantable ( ILR ), también conocido como monitor cardíaco insertable , es un pequeño dispositivo del tamaño de un paquete de goma de mascar o dispositivo dememoria USB que se implanta justo debajo de la piel del tórax para el monitoreo cardíaco (es decir, registrar la actividad eléctrica del corazón ).
Operación [ editar ]
El ILR controla la actividad eléctrica del corazón, almacenando continuamente información en su memoria circular (el "bucle" del nombre) como electrocardiogramas (ECG). La actividad anormal, como la arritmia (latidos cardíacos irregulares) se registra al "congelar" un segmento de la memoria para una revisión posterior. Por lo general, se pueden almacenar hasta tres episodios de actividad anormal, [2] con el episodio más reciente reemplazando al más antiguo. [3]
La grabación se puede activar de dos maneras. Primero, la grabación puede activarse automáticamente de acuerdo con los rangos de frecuencia cardíaca definidos previamente y configurados en el ILR por el médico. Si la frecuencia cardíaca cae por debajo, o aumenta por encima de las frecuencias establecidas, el ILR registrará sin el conocimiento del paciente. La segunda forma en que el ILR registra es a través de un "activador de paciente" de mano, mediante el cual el paciente inicia una grabación presionando un botón cuando nota síntomas como latidos omitidos, mareos o vértigo. [4] El ILR registra "congelando" la información eléctrica que precede, durante y después de los síntomas, en el formato de un electrocardiograma., que se parece a una computadora portátil. [4]
Usos [ editar ]
El ILR es una herramienta de diagnóstico útil cuando los pacientes experimentan síntomas como síncope(desmayos), convulsiones , palpitaciones recurrentes , mareos o mareos regularmente pero no con la frecuencia suficiente para ser capturados por un monitor externo de 24 horas o 30 días. Debido a la larga duración de la batería del ILR (hasta 3 años), el corazón puede ser monitoreado durante un período prolongado.
Los nuevos dispositivos pueden almacenar un total de 60 minutos de grabaciones en su memoria. Treinta minutos se reservan para el almacenamiento automático de arritmias según los criterios preprogramados. Los 30 minutos restantes se pueden dividir en un número seleccionable de ranuras para almacenar grabaciones retrógradas activadas manualmente como respuesta a los síntomas (desmayos, palpitaciones, etc.) que pueden ser causados por una arritmia. [4]
Inserción [ editar ]
La ILR es implantada por un electrofisiólogo bajo anestesia local . Se hace una pequeña incisión (alrededor de 3 a 4 cm o 1,5 pulgadas) justo al lado del esternón debajo de la línea del pezón, generalmente en el lado izquierdo del paciente. [5] Se crea un bolsillo debajo de la piel y el ILR se coloca en el bolsillo. Los pacientes pueden ir a casa el día del procedimiento con pocas restricciones en las actividades. [4] Los moretones y las molestias en el área del implante pueden persistir durante varias semanas.
Se instruye a los pacientes sobre el uso del activador y se les recomienda programar una cita con su médico después de usarlo para que la información almacenada en el ILR pueda recuperarse para su diagnóstico.
deflexión intrinsicoidea , también denominado tiempo pico de la onda R , se mide desde el comienzo del complejo QRS hasta el pico de la onda R. La deflexión intrinsicoide refleja el vector de despolarización desde el endocardio hasta el epicardio.
En presencia de bloqueo de rama o hipertrofia ventricular, el impulso de despolarización tarda más de lo normal en alcanzar el electrodo de registro. Esto retrasa el inicio de la deflexión intrínseca. Esta prolongación o retraso es un criterio importante para diagnosticar el bloqueo de rama y la hipertrofia ventricular. El inicio de la deflexión intrinsicoide> 0.05 segundos (poco más de una caja pequeña) se usa como un criterio no relacionado con el voltaje para diagnosticar la hipertrofia ventricular izquierda .
K v 7.1 ( KvLQT1 ) es una proteína del canal de potasiocuya subunidad primaria en humanos está codificada por el gen KCNQ1 . [5] K v 7.1 es un canal de potasio dependiente de voltaje presente en las membranas de las células de tejido cardíaco y en el oído interno neuronas entre otros tejidos. En las células cardíacas , K v 7.1 media la corriente I Ks (o K + rectificación retardada lenta ) que contribuye a la repolarización de la célula, terminando el potencial de acción cardíaco y por lo tanto la contracción del corazón .
Estructura [ editar ]
KvLQT1 está formado por seis dominios S1-S6 que abarcan la membrana, dos dominios intracelulares y un bucle de poros. [6] El canal KvLQT1 está formado por cuatro subunidades KCNQ1, que forman el canal de iones real.
Función [ editar ]
Este gen codifica una proteína para un canal de potasio dependiente de voltaje requerido para la fase de repolarización del potencial de acción cardíaco. El producto génico puede formar heteromultímeros con otras dos proteínas del canal de potasio, KCNE1 y KCNE3 . El gen está ubicado en una región del cromosoma 11 que contiene una gran cantidad de genes contiguos que están impresos de manera anormal en el cáncer y en el síndrome de Beckwith-Wiedemann . Se han descrito dos transcripciones alternativas que codifican distintas isoformas. [7]
Importancia clínica [ editar ]
Las mutaciones en el gen pueden dar lugar a una proteína defectuosa y varias formas de arritmias hereditarias como el síndrome de QT largo [8] que es una prolongación del intervalo QT de la repolarización cardíaca, síndrome de QT corto , [8] y Familial fibrilación auricular . KvLQT1 también se expresa en el páncreas y se ha demostrado que los pacientes con síndrome de QT largo KvLQT1 tienen hipoglucemia hiperinsulinémica después de una carga de glucosa oral. [9] Las corrientes que surgen de K v 7.1 en sistemas de sobreexpresión nunca han sido recapituladas en tejidos nativos - K v7.1 siempre se encuentra en tejidos nativos con una subunidad moduladora. En el tejido cardíaco, estas subunidades comprenden KCNE1 y yotiao. Aunque fisiológicamente irrelevantes, homotetramérica K V 7.1 canales también muestran una forma única de tipo C inactivación que alcanza el equilibrio rápidamente, permitiendo que las corrientes de KvLQT1 a meseta. Esto es diferente de la inactivación observada en las corrientes de tipo A, que causa una rápida decadencia de la corriente.
Ligandos [ editar ]
- ML277: activador de canal potente y selectivo [10]
Interacciones [ editar ]
KvLQT1 también puede asociarse con cualquiera de los cinco miembros de la familia de proteínas KCNE, pero las interacciones con KCNE1 , KCNE2 , KCNE3 son las únicas interacciones dentro de esta familia de proteínas que afectan al corazón humano. KCNE2, KCNE4 y KCNE5 han demostrado tener un efecto inhibitorio sobre la funcionalidad de KvLQT1, mientras que KCNE1 y KCNE3 son activadores de KvLQT1. [6]KvLQT1 puede asociarse con KCNE1 y KCNE4 con los efectos de activación de KCNE1 anulando los efectos inhibitorios de KCNE4 en el canal de KvLQT1, y KvLQT1 comúnmente se asociará con dos a cuatro proteínas KCNE diferentes para poder funcionar. [6] Sin embargo, KvLQT1 se asocia más comúnmente con KCNE1 y forma el complejo KvLQT1 / KCNE1, ya que solo se ha visto que funciona in vivo cuando se asocia con otra proteína. [6] KCNQ1 formará un heterómero con KCNE1 para retardar su activación y aumentar la densidad de corriente en la membrana plasmática de la neurona. [6] [12] Además de asociarse con proteínas KCNE, el dominio yuxtamembranoso N-terminal de KvLQT1 también puede asociarse con SGK1 , que estimula la corriente del rectificador de potasio retardada lenta. Dado que SGK1 requiere integridad estructural para estimular KvLQT1 / KCNE1, cualquier mutación presente en la proteína KvLQT1 puede resultar en una reducción de la estimulación de este canal por SGK1. [13] Se sabe que las mutaciones generales en KvLQT1 causan una disminución en esta corriente de rectificación de potasio retardada lenta, potenciales de acción cardíacos más largos y una tendencia a tener taquiarritmias. [12]
KvLQT1 / KCNE1 [ editar ]
KCNE1 (minK), puede ensamblarse con KvLQT1 para formar un canal rectificador de potasio retardado lento. KCNE1 retarda la inactivación de KvLQT1 cuando las dos proteínas forman un complejo heteromérico, y la amplitud de la corriente aumenta mucho en comparación con los canales homotetraméricos WT-KvLQT1 . KCNE1 se asocia con la región de poros de KvLQT1, y su dominio transmembrana contribuye al filtro de selectividad de este complejo de canales heteroméricos. [12] La hélice alfa de la proteína KCNE1 interactúa con el dominio de poros S5 / S6 y con el dominio S4 del canal KvLQT1. Esto resulta en modificaciones estructurales del sensor de voltaje y el filtro de selectividad del canal KvLQT1. [14] Las mutaciones en la subunidad alfa de este complejo, KvLQT1 o en la subunidad beta, KCNE1, pueden conducir al síndrome de QT largo u otras deformidades rítmicas cardíacas. [13] Cuando se asocia con KCNE1, el canal KvLQT1 se activa mucho más lentamente y con un potencial de membrana más positivo . Se cree que dos proteínas KCNE1 interactúan con un canal tetramérico KvLQT1, ya que los datos experimentales sugieren que hay 4 subunidades alfa y 2 subunidades beta en este complejo. [14] Los canales KVLQT1 / KCNE1 se captan de la membrana plasmática a través de un mecanismo dependiente de RAB5 , pero se insertan en la membrana mediante RAB11 , una GTPasa .
| KCNQ1 | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Identificadores | |||||||||||||||||||||||||
| Alias | KCNQ1 , ATFB1, ATFB3, JLNS1, KCNA8, KCNA9, KVLQT1, Kv1.9, Kv7.1, LQT1, RWS, SQT2, WRS, subfamilia de canal con voltaje de potasio Q miembro 1 | ||||||||||||||||||||||||
| IDs externas | OMIM: 607542 MGI: 108083 HomoloGene: 85014 GeneCards: KCNQ1 | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
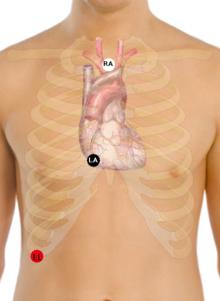
Una derivación de Lewis (también llamada derivación S5 ) es una derivación de ECG modificada que se utiliza para detectar ondas de aleteo auricular cuando se sospecha clínicamente de aleteo auricular, según los signos y síntomas, pero no está definitivamente demostrada en el ECG estándar de 12 derivaciones. Para crear el Lewis Lead, el electrodo del brazo derecho se mueve al manubrio adyacente al esternón . Luego, el electrodo del brazo izquierdo se mueve hacia la derecha, quinto espacio intercostal adyacente al esternón. El electrodo de la pierna izquierda se coloca en el margen costal inferior derecho. El Lewis Lead se lee luego como Lead I en el ECG y, ya que en la mayoría de los pacientes será aproximadamente perpendicular a la onda de despolarización ventricular.Las ondas de aleteo auricular pueden ser más evidentes.



No hay comentarios:
Publicar un comentario