Las células de Kurloff (también conocidas como células de Foà-Kurloff [1] ), que se encuentran en la sangre y los órganos de cobayas , contienen gránulos secretores grandes (también conocidos como cuerpos de Kurloff) de función desconocida. También se encuentran en la capibara . Los científicos especulan que estas células junto con la asparaginasa pueden ser las que le dan a las propiedades resistentes al cáncer del conejillo de indias (Sharon Vanderlip, DVM). La célula de Kurloff tiene actividad citotóxica NK in vitro.
Un linfoblasto es un linfocito ingenuo modificado con morfología celular alterada. Ocurre cuando el linfocito es activado por un antígeno (de las células presentadoras de antígeno) y aumenta en volumen por el crecimiento del núcleo y el citoplasma, así como por la síntesis de nuevos ARNm y proteínas. Luego, el linfoblasto comienza a dividirse de dos a cuatro veces cada 24 horas durante 3-5 días, con un solo linfoblasto que produce aproximadamente 1000 clones de su linfocito original, cada uno de los cuales comparte la especificidad original del antígeno. Finalmente, las células en división se diferencian en células efectoras, conocidas como células plasmáticas (para células B), células T citotóxicas y células T cooperadoras. [1]
Los linfoblastos también pueden referirse a células inmaduras que típicamente se diferencian para formar linfocitos maduros . [2] Normalmente, los linfoblastos se encuentran en la médula ósea, pero en la leucemia linfoblástica aguda (LLA), los linfoblastos proliferan de manera incontrolable y se encuentran en grandes cantidades en la sangre periférica.
El tamaño es de entre 10 y 20 μm. [3]
Aunque comúnmente el linfoblasto se refiere a una célula precursora en la maduración de los leucocitos , el uso de este término a veces es inconsistente. El Consorcio de Investigación de Leucemia Linfocítica Crónica define un linfoblasto como "Un linfocito que se ha vuelto más grande después de ser estimulado por un antígeno. Los linfoblastos se parecen a los linfocitos inmaduros, y se creía que eran células precursoras". [4] Comúnmente, cuando se habla de leucemia, "explosión" se usa como una abreviatura de linfoblastos.
Los linfoblastos se pueden distinguir microscópicamente de los mieloblastos por tener nucleolos menos distintos, más cromatina condensada y ausencia de gránulos citoplásmicos. Sin embargo, estas distinciones morfológicas no son absolutas y un diagnóstico definitivo se basa en la inmunotinción de anticuerpos para la presencia de un grupo único de receptores de diferenciación .
Las células de la sangre periférica son los componentes celulares de la sangre , que consisten en glóbulos rojos (eritrocitos), glóbulos blancos (leucocitos) y plaquetas , que se encuentran dentro del grupo de sangre circulante y no están secuestradas en el sistema linfático , bazo , hígado . o médula ósea .
Las células dendríticas plasmocitoides (pDC, por sus siglas en inglés) son un tipo raro de células inmunitarias que se sabe que secretan grandes cantidades de interferón tipo 1 (IFN) en respuesta a una infección viral. Circulan en la sangre y se encuentran en los órganos linfoides periféricos. Se desarrollan a partir de células madre hematopoyéticas de la médula ósea y constituyen <0 de="" font="" nbsp="">las células mononucleares de sangre periférica (PBMC). [1] Además de los mecanismos antivirales, los pDC se consideran claves para vincular los sistemas inmunitarios innatos y adaptativos. Sin embargo, los pDC también son responsables de participar y exacerbar ciertas enfermedades autoinmunes como el lupus . [2] Los pDC también son las células malignas que causan una enfermedad rara.Trastorno hematológico , neoplasia de células dendríticas plasmocitoides blásticas .
Desarrollo y características [ editar ]
En la médula ósea, los progenitores de células dendríticas comunes que expresan los receptores Flt3 ( CD135 ) pueden dar lugar a pDC. La señalización de Flt3 o CD135 induce la diferenciación y proliferación de pDC, aunque sus mecanismos no se entienden completamente. Se cree que la activación de la rapamicina (mTOR) dependiente de la fosfoinositida 3-quinasa (PI3K) regula esta vía de señalización. También se ha encontrado que el factor de transcripción E2-2 desempeña un papel clave para influir en el compromiso de linaje de un progenitor común de DC en su curso para convertirse en un pDC. [4]
A diferencia de las células dendríticas convencionales (CDC) que dejan la médula ósea como precursoras, las CDP dejan la médula ósea para ir a los órganos linfoides y la sangre periférica al completar el desarrollo. Las células dendríticas plasmocitoides también se distinguen de las CDC debido a su capacidad para producir cantidades significativas de interferón tipo 1. [5] La maduración de pDC se inicia cuando la célula entra en contacto con un virus, lo que provoca la regulación positiva del MHC de clase I y del MHC de clase II , las moléculas coestimulantes CD80 , CD86 , CD83 y el receptor de quimiocinas cc 7 (CCR7) y la producción de interferón disminuye gradualmente. La expresión de CCR7 hace que el pDC madurado migre a un ganglio linfático donde podrá estimular e interactuar con las células T. [6]
En los seres humanos, los pDC muestran morfología de las células plasmáticas y expresan CD4 , HLA-DR , CD123 , antígeno dendrítico de células derivadas de la sangre 2 ( BDCA-2 ), receptor tipo Toll (TLR) 7 y TLR9dentro de los compartimentos endosomal. La expresión de TLR 7 y TLR 9 permite que los pDC interactúen con los ácidos nucleicos víricos y del huésped. El TLR 7 y el TLR 9 detectan el ARN de cadena simple y las secuencias de ADN de CpG sin metilar , respectivamente. [7] ILT7 y BDCA -4 también se expresan en las superficies de pDC humanas, aunque sus vías de señalización aún son oscuras. Sin embargo, hay especulaciones de que la interacción entre ILT7 y BST2Puede tener un efecto regulador negativo en la producción de interferón de la célula. [8] A diferencia de las células dendríticas mieloides , los antígenos mieloides como CD11b , CD11c , CD13 , CD14 y CD33 no están presentes en las superficies de pDC. Además, los pDC expresan los marcadores CD123, CD303 (BDCA-2) y CD304 a diferencia de otros tipos de células dendríticas. [9]
Neoplasia de células dendríticas plasmocitoides blásticas [ editar ]
La neoplasia de células dendríticas plasmocitoides blásticas es un tipo raro de cáncer mieloide en el que los PDC malignos se infiltran en la piel, la médula ósea, el sistema nervioso central y otros tejidos. Por lo general, la enfermedad se presenta con lesiones en la piel (p. Ej. Nódulos, tumores, pápulas , parches similares a hematomas y / o úlceras) que ocurren con mayor frecuencia en la cabeza, la cara y la parte superior del torso. [3]Esta presentación puede ir acompañada de infiltraciones de CPC en otros tejidos para producir ganglios linfáticos inflamados , agrandamiento del hígado, bazo agrandado, síntomas de disfunción del sistema nervioso central y anormalidades similares en senos, ojos, riñones, pulmones, tracto gastrointestinal, hueso , senos, oídos y / o testículos. [10]La enfermedad también puede presentarse como una leucemia pDC , es decir, niveles aumentados de pDC malignos en la sangre (es decir,> 2% de las células nucleadas) y en la médula ósea y evidencia (es decir, citopenias ) de insuficiencia de la médula ósea . [10] La neoplasia de células dendríticas plasmocitoides blásticas tiene una alta tasa de recurrencia después de los tratamientos iniciales con diversos regímenes de quimioterapia. En consecuencia, la enfermedad tiene un mal pronóstico general y se están estudiando nuevos tratamientos quimioterapéuticos y nuevos fármacos no quimioterapéuticos para mejorar la situación. [11]
Role In Immunity [ editar ]
Tras la estimulación y posterior activación de TLR7 y TLR9, estas células producen grandes cantidades (hasta 1.000 veces más que otros tipos de células) de interferón de tipo I (principalmente IFN-α y IFN-β ), que son compuestos antivirales críticos que median una Amplia gama de efectos e inducción de la maduración del pDC. Por ejemplo, la secreción de interferón tipo 1 desencadena células asesinas naturales para producir IFNγ altiempo que activa la diferenciación de las células B. [12] Además, también pueden producir las citocinas IL-12 , IL-6 y TNF-α , lo que ayuda a reclutar otras células inmunitarias para el sitio de la infección. [13]
Debido a que son capaces de activar otras células inmunitarias, los pDC sirven como un puente entre la inmunidad innata y la adaptativa . La capacidad de un pDC para estimular las células T se incrementa después de la maduración. Como se mencionó anteriormente, la maduración también induce la expresión de moléculas MHC Clase I y Clase II en pDC, lo que permite a la célula optimizar sus capacidades de presentación de antígenos. El MHC clase I en las superficies de pDC puede activar las células T CD8 +, mientras que se ha encontrado que el MHC clase II activa las células T CD4 +. También se cree que los pDC pueden promover tanto la activación como la tolerancia de las células T. [14]
Papel en la autoinmunidad y enfermedades [ editar ]
Psoriasis [ editar ]
Los pacientes que sufren de psoriasis por lo general exhiben lesiones en la piel donde se acumulan los CDP. La inhibición de los pDC de la secreción de IFN disminuyó la apariencia de las lesiones cutáneas. Cuando el ADN se libera a través de la apoptosis de una célula huésped infectada, se producen anticuerpos contra el propio ADN del huésped. (ver autoanticuerpo ). Estos anticuerpos anti-ADN del ADN son capaces de estimular las pDC que secretan IFN, lo que favorece la actividad de la inmunidad adaptativa. [15]
Lupus [ editar ]
Si bien la capacidad del pDC para producir en masa el interferón tipo 1 puede ser eficaz para atacar una infección viral, también puede conducir al lupus eritematoso sistémico si no se regula adecuadamente. La producción de interferón tipo 1 está fuertemente correlacionada con la progresión del lupus, y se piensa que conduce a una maduración excesiva de los pDC y la activación de las células B, entre muchos otros efectos. En pacientes con lupus, los niveles de pDC en la sangre circulante disminuyen, la mayoría de los pDC han migrado hacia los tejidos inflamados y afectados. [dieciséis]
VIH [ editar ]
La producción en masa de interferón tipo 1 puede dar resultados positivos y negativos en respuesta al VIH . Aunque el interferón tipo 1 es eficaz para facilitar la maduración de las pDC y para matar las células T infectadas, la eliminación excesiva de las células T infectadas puede tener efectos perjudiciales y debilitar aún más el sistema inmunitario comprometido del paciente. [17] Los pDC por sí mismos no pueden ser infectados por el VIH, pero detectan marcadores virales como el ssRNA y están afectados por su capacidad de producir interferón. Sin embargo, parece que en el VIH, las CDP no solo pierden sus propiedades secretoras de interferón sino que también mueren, acelerando la progresión de la enfermedad. [18]Las disminuciones en la vida útil de pDC no infectadas han resultado en disminuciones en las células T CD4 + que comprometen aún más las defensas inmunológicas del paciente contra el VIH. Por lo tanto, mantener el equilibrio y la regulación de la actividad de la pDC es crucial para un pronóstico más positivo en pacientes con VIH.
| Células cromafines medulares | |
|---|---|
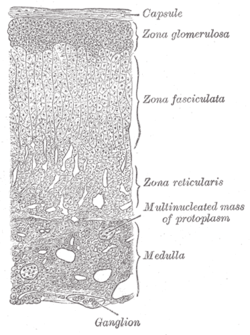
Glándula suprarrenal. (Médula etiquetada en la parte inferior derecha.)
| |
| Detalles | |
| Ubicación | Glándula suprarrenal de la médula |
| Identificadores | |
| latín | endocrinocito medular |
| TH | H3.08.02.6.00015 |
| Términos anatómicos de la microanatomía. | |
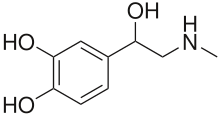
Las células cromafines , también los feocromocitos , son células neuroendocrinas que se encuentran principalmente en la médula de las glándulas suprarrenales en los mamíferos . Estas células cumplen una variedad de funciones, como la respuesta al estrés, el control del dióxido de carbono y las concentraciones de oxígeno en el cuerpo, el mantenimiento de la respiración y la regulación de la presión arterial. [1] Están muy cerca de los ganglios simpáticospresinápticos del sistema nervioso simpático , con los que se comunican, y estructuralmente son similares a las neuronas simpáticas post-sinápticas. Para activar las células cromafines, el nervio esplácnico.El sistema nervioso simpático libera acetilcolina, que luego se une a los receptores nicotínicos de acetilcolina en la médula suprarrenal. Esto provoca la liberación de catecolaminas. Las células cromafines liberan catecolaminas : ~ 80% de adrenalina( epinefrina ) y ~ 20% de noradrenalina ( norepinefrina ) en la circulación sistémica para efectos sistémicos en múltiples órganos (similar a las neuronas secretoras del hipotálamo ), y también pueden enviar señales de paracrina . De ahí que se denominen células neuroendocrinas.
Estructura [ editar ]
Hay dos tipos de células que se originan en la cresta neural y están relacionadas con el sistema nervioso simpático (se originan en una célula llamada simpatogonia): [2]
1) Neuroblastos : estas células migran, durante la cuarta a la quinta semana de desarrollo fetal en humanos, en ambos lados de la médula espinal hacia la región justo detrás de la aorta dorsal que forma las dos cadenas de los ganglios simpáticos (cadena simpática). De estos ganglios, las fibras simpáticas postsinápticas surgirán y se extenderán hacia su órgano objetivo. Algunas de estas células migrarán a la médula suprarrenal para formar células de los ganglios simpáticos dentro de la médula suprarrenal (sin fibras simpáticas postsinápticas). Un tumor que surge de estas células se llama neuroblastoma. [3]
2) Células cromafines (o feocromocitos): estas células migrarán al área adyacente a los ganglios simpáticos (de ahí el nombre de paraganglia) y a la médula suprarrenal, donde serán el tipo de células más abundante. El grupo extraadrenal más grande de células cromafines en mamíferos es el órgano de Zuckerkandl . [4] Los tumores que surgen de estas células se llaman paragangliomas o feocromocitomas. Estos términos se pueden usar indistintamente, pero generalmente paraganglioma se refiere a un tumor originado por células cromafines fuera de la glándula suprarrenal, que también puede denominarse feocromocitoma extraadrenal, mientras que el feocromocitoma generalmente se refiere a un tumor que se origina en las células cromafines dentro de la glándula suprarrenal. [2]
Las células cromafines también se asientan cerca del nervio vago y las arterias carótidas . En concentraciones más bajas, las células cromafines extra-adrenales también residen en la pared de la vejiga , la próstata y detrás del hígado .
En los no mamíferos, las células cromafines se encuentran en una variedad de lugares, generalmente no organizados como un órgano individual, y pueden estar sin inervación, confiando solo en las señales endocrinaso paracrinas para la secreción. [5] [6]
Función [ editar ]
Las células cromafines de la médula suprarrenal están inervadas por el nervio esplácnico y secretan adrenalina ( epinefrina ), noradrenalina ( norepinefrina ), algo de dopamina , encefalina y péptidos que contienen encefalina y otras pocas hormonas en el torrente sanguíneo . La adrenalina y la noradrenalina secretadas desempeñan un papel importante en la respuesta del sistema nervioso simpático, comúnmente llamada respuesta de lucha o huida . Las encefalinas y los péptidos que contienen encefalina están relacionados, pero son distintos de los péptidos endógenos llamados endorfinas.(que se secretan de la pituitaria); todos estos péptidos se unen a los receptores opioides y producen respuestas analgésicas (y otras). Las hormonas se secretan de los gránulos de cromafina; aquí es donde la enzima dopamina β-hidroxilasa cataliza la conversión de dopamina a noradrenalina. [7]Existen distintas formas de células N y E (también células Na y A en la nomenclatura británica - noradrenalina y adrenalina); los primeros producen norepinefrina, los últimos surgen de las células N a través de la interacción con glucocorticoides y convierten la norepinefrina en epinefrina. [8]
Importancia clínica [ editar ]
Neoplasias derivadas de estas células son feocromocitomas (también llamados paragangliomas cromafines o simpático, en contraste con no cromafines o parasimpáticas paragangliomas de células del glomus). A veces, solo las neoplasias de origen suprarrenal se denominan feocromocitomas, mientras que otras se denominan paragangliomas extraadrenales.
La insuficiencia cardíaca [ editar ]
Después de la insuficiencia cardíaca , el cuerpo aumenta la actividad simpática hacia la médula suprarrenal como mecanismo compensatorio para aumentar la frecuencia cardíaca y el gasto cardíaco . Este aumento de la actividad simpática conduce a un aumento crónico de la síntesis y la secreción de catecolaminas de las células cromafines suprarrenales. Este aumento crónico de la secreción de epinefrina y norepinefrina provoca la desensibilización de las células cromafines a las catecolaminas, lo que resulta en una disminución de la producción y la presencia de receptores α 2 adrenérgicos en su membrana celular. Esta desensibilización y regulación a la baja de los receptores adrenérgicos α 2 es causada por la regulación positiva de la enzima Adrenal G proteína acoplada al receptor quinasa 2 ( GRK2) que elimina efectivamente la retroalimentación negativa normal de tipo autocrino que normalmente evita que las células produzcan en exceso las catecolaminas y la reemplaza con un circuito de retroalimentación positiva en el que una mayor secreción provoca una secreción mayor. [9] Esta regulación al alza de GRK2 también está acompañada por la regulación al alza y el aumento de la producción de la enzima tirosina hidroxilasa , que cataliza la etapa limitante de la velocidad de la síntesis de catecolamina. [10]
Historia [ editar ]
La palabra 'Chromaffin' viene de un baúl de cromo y afinidad . Se nombran como tales porque se pueden visualizar tiñendo con sales de cromo . Las sales de cromo oxidan y polimerizan las catecolaminas para formar un color marrón, más fuertemente en las células que secretan noradrenalina. Las células cromafines también se llaman feocromocitos.
Las células enterocromafines se llaman así debido a su similitud histológica con las células cromafines (también se tiñen de amarillo cuando se tratan con sales de cromo), pero su función es bastante diferente y no son derivados de la cresta neural.
Los paraganglios son grupos de células cromafines o células glómicas cerca de los ganglios simpáticos.




No hay comentarios:
Publicar un comentario