delta- v es simplemente un cambio en la velocidad . El delta de las letras mayúsculas griegas es el símbolo matemático estándar para representar el cambio en cierta cantidad.
Dependiendo de la situación, delta- v puede ser un vector espacial ( v ) o escalar (Δ v ). En cualquier caso, es igual a la aceleración (vector o escalar) integrada en el tiempo:
- (versión vectorial)
- (versión escalar)
Si la aceleración es constante, el cambio en la velocidad se puede expresar como:
dónde:
- v 0 o v 0 es la velocidad inicial (en el tiempo t 0 ),
- v 1 o v 1 es la velocidad posterior (en el tiempo t 1 ).
El cambio en la velocidad es útil en muchos casos, como determinar el cambio en el momento ( impulso ), donde:, dónde es el impulso y m es la masa.
| Densidad | |
|---|---|
Simbolos comunes
| ρ D |
| Unidad SI | kg / m 3 |
La densidad , o más precisamente, la densidad de masa volumétrica de una sustancia es su masa por unidad de volumen . El símbolo más utilizado para la densidad es ρ (la letra griega minúscula rho ), aunque también se puede usar la letra D latina . Matemáticamente, la densidad se define como una masa dividida por volumen: [1]
donde ρ es la densidad, m es la masa y V es el volumen. En algunos casos (por ejemplo, en la industria de petróleo y gas de los Estados Unidos), la densidad se define de manera general como su peso por unidad de volumen , [2] aunque esto es científicamente inexacto; esta cantidad se denomina específicamente peso específico .
Para una sustancia pura, la densidad tiene el mismo valor numérico que su concentración en masa . Los diferentes materiales suelen tener diferentes densidades, y la densidad puede ser relevante para la flotabilidad , la pureza y el embalaje . El osmio y el iridio son los elementos más densos conocidos en condiciones estándar de temperatura y presión, pero ciertos compuestos químicos pueden ser más densos.
Para simplificar las comparaciones de densidad a través de diferentes sistemas de unidades, a veces se reemplaza por la " densidad relativa " o " gravedad específica " de la cantidad sin dimensiones , es decir, la relación de la densidad del material a la de un material estándar, generalmente agua. Por lo tanto, una densidad relativa menor que uno significa que la sustancia flota en el agua.
La densidad de un material varía con la temperatura y la presión. Esta variación es típicamente pequeña para sólidos y líquidos, pero mucho mayor para los gases. Aumentar la presión sobre un objeto disminuye el volumen del objeto y, por lo tanto, aumenta su densidad. Aumentar la temperatura de una sustancia (con algunas excepciones) disminuye su densidad al aumentar su volumen. En la mayoría de los materiales, el calentamiento de la parte inferior de un fluido da como resultado la convección del calor desde la parte inferior hasta la parte superior, debido a la disminución de la densidad del fluido calentado. Esto hace que se eleve en relación con un material más denso sin calentar.
El recíproco de la densidad de una sustancia se denomina ocasionalmente su volumen específico , un término que a veces se usa en termodinámica . La densidad es una propiedad intensivaen el sentido de que aumentar la cantidad de una sustancia no aumenta su densidad; más bien aumenta su masa.
Historia
En un cuento bien conocido pero probablemente apócrifo, a Arquímedes se le dio la tarea de determinar si el orfebre del rey Hiero estaba malversando oro durante la fabricación de una corona de oro dedicada a los dioses y reemplazándola por otra aleación más barata . [3] Arquímedes sabía que la corona de forma irregular podría ser aplastada en un cubo cuyo volumen se podría calcular fácilmente y comparar con la masa; Pero el rey no aprobó esto. Desconcertado, se dice que Arquímedes tomó un baño de inmersión y observó desde el ascenso del agua al entrar que podía calcular el volumen de la corona de oro a través del desplazamientodel agua. Tras este descubrimiento, saltó de su baño y corrió desnudo por las calles gritando "¡Eureka! ¡Eureka!" (Εύρηκα! Griego "Lo he encontrado"). Como resultado, el término " eureka " entró en el lenguaje común y se usa hoy para indicar un momento de iluminación.
La historia apareció por primera vez en forma escrita en los libros de arquitectura de Vitruvio , dos siglos después de lo que supuestamente tuvo lugar. [4] Algunos eruditos han dudado de la exactitud de esta historia, diciendo entre otras cosas que el método habría requerido mediciones precisas que hubieran sido difíciles de realizar en ese momento. [5] [6]
De la ecuación para densidad ( ρ = m / V ), la densidad de masa tiene unidades de masa divididas por volumen. Como hay muchas unidades de masa y volumen que cubren diferentes magnitudes, hay un gran número de unidades para la densidad de masa en uso. La unidad SI de kilogramo por metro cúbico (kg / m 3 ) y la unidad cgs de gramo por centímetro cúbico (g / cm 3 ) son probablemente las unidades más utilizadas para la densidad. Un g / cm 3 es igual a mil kg / m 3. Un centímetro cúbico (abreviatura cc) es igual a un mililitro. En la industria, otras unidades de masa y / o volumen más grandes o más pequeñas son a menudo más prácticas y se pueden usar las unidades tradicionales de los Estados Unidos . Vea a continuación una lista de algunas de las unidades de densidad más comunes.
Medida de densidad
Existen varias técnicas y estándares para la medición de la densidad de los materiales. Tales técnicas incluyen el uso de un hidrómetro (un método de flotabilidad para líquidos), un equilibrio hidrostático (un método de flotabilidad para líquidos y sólidos), un método de cuerpo sumergido (un método de flotabilidad para líquidos), un picnómetro (líquidos y sólidos), un comparador de aire picnómetro ( sólidos), densitómetro oscilante (líquidos), así como verter y golpear (sólidos). [7] Sin embargo, cada método o técnica individual mide diferentes tipos de densidad (por ejemplo, densidad aparente, densidad esquelética, etc.) y, por lo tanto, es necesario comprender el tipo de densidad que se está midiendo, así como el tipo de material en cuestión.
Materiales homogéneos
La densidad en todos los puntos de un objeto homogéneo es igual a su masa total dividida por su volumen total. La masa se mide normalmente con una escala o equilibrio ; el volumen puede medirse directamente (a partir de la geometría del objeto) o por el desplazamiento de un fluido. Para determinar la densidad de un líquido o un gas, un hidrómetro , un dasymeter o un medidor de flujo de Coriolis se puede utilizar, respectivamente. De manera similar, el pesaje hidrostático utiliza el desplazamiento del agua debido a un objeto sumergido para determinar la densidad del objeto.
Materiales heterogéneos
Si el cuerpo no es homogéneo, entonces su densidad varía entre las diferentes regiones del objeto. En ese caso, la densidad alrededor de una ubicación determinada se determina al calcular la densidad de un volumen pequeño alrededor de esa ubicación. En el límite de un volumen infinitesimal, la densidad de un objeto no homogéneo en un punto se convierte en:, dónde Es un volumen elemental en posición. . La masa del cuerpo puede entonces expresarse como
Materiales no compactos
En la práctica, los materiales a granel como el azúcar, la arena o la nieve contienen vacíos. Muchos materiales existen en la naturaleza como escamas, pellets o gránulos.
Los vacíos son regiones que contienen algo más que el material considerado. Comúnmente, el vacío es aire, pero también puede ser vacío, líquido, sólido o un gas o mezcla gaseosa diferente.
El volumen de volumen de un material, incluida la fracción vacía, se obtiene a menudo mediante una medición simple (por ejemplo, con una taza de medición calibrada) o geométricamente a partir de dimensiones conocidas.
La masa dividida por el volumen de volumen determina la densidad aparente . Esto no es lo mismo que la densidad de masa volumétrica.
Para determinar la densidad de masa volumétrica, primero se debe descontar el volumen de la fracción vacía. A veces esto puede ser determinado por el razonamiento geométrico. Para el empaquetamiento cerrado de esferas iguales, la fracción no vacía puede ser a lo sumo aproximadamente el 74%. También se puede determinar empíricamente. Sin embargo, algunos materiales a granel, como la arena, tienen una fracción de vacío variableque depende de cómo se agita o vierte el material. Puede ser suelto o compacto, con más o menos espacio de aire dependiendo de la manipulación.
En la práctica, la fracción vacía no es necesariamente aire, ni siquiera gaseosa. En el caso de la arena, podría ser agua, lo que puede ser ventajoso para la medición, ya que la fracción de vacío para la arena saturada en agua, una vez que las burbujas de aire se eliminan completamente, es potencialmente más consistente que la arena seca medida con un vacío de aire.
En el caso de materiales no compactos, también se debe tener cuidado al determinar la masa de la muestra de material. Si el material está bajo presión (comúnmente la presión del aire ambiente en la superficie de la tierra), la determinación de la masa a partir de un peso de muestra medido podría tener que tener en cuenta los efectos de flotabilidad debidos a la densidad del componente vacío, dependiendo de cómo se realizó la medición. En el caso de la arena seca, la arena es mucho más densa que el aire que el efecto de flotación se suele descuidar (menos de una parte en mil).
El cambio de masa al desplazar un material vacío con otro mientras se mantiene el volumen constante puede usarse para estimar la fracción vacía, si la diferencia en la densidad de los dos materiales vacíos se conoce de manera confiable.
Cambios de densidad
En general, la densidad se puede cambiar cambiando la presión o la temperatura . El aumento de la presión siempre aumenta la densidad de un material. El aumento de la temperatura generalmente disminuye la densidad, pero hay excepciones notables a esta generalización. Por ejemplo, la densidad del agua aumenta entre su punto de fusión a 0 ° C y 4 ° C; Un comportamiento similar se observa en el silicio a bajas temperaturas.
El efecto de la presión y la temperatura sobre las densidades de líquidos y sólidos es pequeño. La compresibilidad para un líquido o sólido típico es de 10 −6 bar −1 (1 bar = 0.1 MPa) y una expansividad térmicatípica es de 10 −5 K −1 . Esto se traduce aproximadamente en la necesidad de alrededor de diez mil veces la presión atmosférica para reducir el volumen de una sustancia en un uno por ciento. (Aunque las presiones necesarias pueden ser mil veces más pequeñas para el suelo arenoso y algunas arcillas). Una expansión de volumen del uno por ciento generalmente requiere un aumento de la temperatura del orden de miles de grados centígrados .
En contraste, la densidad de los gases está fuertemente afectada por la presión. La densidad de un gas ideal es
donde M es la masa molar , P es la presión, R es la constante de gas universal y T es la temperatura absoluta . Esto significa que la densidad de un gas ideal puede duplicarse duplicando la presión o reduciendo a la mitad la temperatura absoluta.
En el caso de la expansión térmica volumétrica a presión constante y pequeños intervalos de temperatura, la dependencia de la densidad de la temperatura es:
dónde es la densidad a una temperatura de referencia, es el coeficiente de expansión térmica del material a temperaturas cercanas a .
Densidad de soluciones
La densidad de una solución es la suma de las concentraciones de masa (masivas) de los componentes de esa solución.
La concentración de masa (masiva) de cada componente dado ρ i en una solución suma a la densidad de la solución.
Expresado en función de las densidades de los componentes puros de la mezcla y su participación en el volumen, permite la determinación del exceso de volúmenes molares :
siempre que no haya interacción entre los componentes.
Conociendo la relación entre los volúmenes excesivos y los coeficientes de actividad de los componentes, se pueden determinar los coeficientes de actividad.
Densidades
Varios materiales
- Los elementos químicos seleccionados se enumeran aquí. Para las densidades de todos los elementos químicos, ver Lista de elementos químicos
| Material | ρ (kg / m 3 )[nota 1] | Notas |
|---|---|---|
| Hidrógeno | 0.0898 | |
| Helio | 0.179 | |
| Aerografita | 0.2 | [nota 2] [8] [9] |
| Microlatticia metalica. | 0.9 | [nota 2] |
| Aerogel | 1.0 | [nota 2] |
| Aire | 1.2 | Al nivel del mar |
| Hexafluoruro de tungsteno | 12.4 | Uno de los gases más pesados conocidos en condiciones estándar. |
| Hidrógeno líquido | 70 | A aprox. −255 ° C |
| Espuma de poliestireno | 75 | Aprox. [10] |
| corcho | 240 | Aprox. [10] |
| Pino | 373 | [11] |
| Litio | 535 | |
| Madera | 700 | Sazonado, típico [12] [13] |
| Roble | 710 | [11] |
| Potasio | 860 | [14] |
| Hielo | 916.7 | A temperatura <0 c="" font=""> |
| Aceite de cocina | 910–930 | |
| Sodio | 970 | |
| Agua (fresca) | 1,000 | A 4 ° C, la temperatura de su densidad máxima. |
| Agua (sal) | 1,030 | 3% |
| Oxígeno líquido | 1.141 | A aprox. −219 ° C |
| Nylon | 1.150 | |
| Plástica | 1,175 | Aprox .; Para polipropileno y PETE / PVC. |
| Tetracloroeteno | 1,622 | |
| Magnesio | 1,740 | |
| Berilio | 1,850 | |
| Glicerol | 1.261 | [15] |
| Hormigón | 2,400 | [16] [17] |
| Silicio | 2,330 | |
| Aluminio | 2,700 | |
| Diyodometano | 3,325 | Líquido a temperatura ambiente. |
| Diamante | 3.500 | |
| Titanio | 4,540 | |
| Selenio | 4,800 | |
| Vanadio | 6,100 | |
| Antimonio | 6,690 | |
| Zinc | 7,000 | |
| Cromo | 7,200 | |
| Estaño | 7,310 | |
| Manganeso | 7,325 | Aprox. |
| Planchar | 7,870 | |
| Niobio | 8,570 | |
| Latón | 8,600 | [17] |
| Cadmio | 8,650 | |
| Cobalto | 8,900 | |
| Níquel | 8,900 | |
| Cobre | 8,940 | |
| Bismuto | 9,750 | |
| Molibdeno | 10,220 | |
| Plata | 10,500 | |
| Dirigir | 11,340 | |
| Torio | 11,700 | |
| Rodio | 12,410 | |
| Mercurio | 13,546 | |
| Tantalio | 16.600 | |
| Uranio | 18.800 | |
| Tungsteno | 19,300 | |
| Oro | 19,320 | |
| Plutonio | 19,840 | |
| Renio | 21,020 | |
| Platino | 21,450 | |
| Iridio | 22,420 | |
| Osmio | 22,570 | |
| Notas: | ||
Otros
| Entidad | ρ (kg / m 3) | Notas |
|---|---|---|
| Medio interestelar | 1 × 10 −19 | Suponiendo 90% H, 10% He; variable T |
| La tierra | 5,515 | Densidad media [18] |
| El núcleo interno de la tierra. | 13,000 | Aprox., Como se indica en la Tierra . [19] |
| El núcleo del sol. | 33,000–160,000 | Aprox. [20] |
| Agujero negro super-masivo | 9 × 10 5 | La densidad de un agujero negro de 4,5 millones de masa solar con un radio de horizonte de Evento es de 13,5 millones de km. |
| enano blancoEstrella | 2.1 × 10 9 | Aprox. [21] |
| Núcleos atómicos | 2,3 × 10 17 | No depende mucho del tamaño del núcleo [22] |
| Estrella neutrón | 1 × 10 18 | |
| Agujero negro de masa estelar | 1 × 10 18 | La densidad de un agujero negro de 4 masas solares. El radio del horizonte de eventos es de 12 km. |
Agua
| Temperatura. (° C) [nota 1] | Densidad (kg / m 3 ) |
|---|---|
| −30 | 983.854 |
| −20 | 993.547 |
| −10 | 998.117 |
| 0 | 999.8395 |
| 4 | 999.9720 |
| 10 | 999.7026 |
| 15 | 999.1026 |
| 20 | 998.2071 |
| 22 | 997.7735 |
| 25 | 997.0479 |
| 30 | 995.6502 |
| 40 | 992.2 |
| 60 | 983.2 |
| 80 | 971.8 |
| 100 | 958.4 |
Notas:
| |
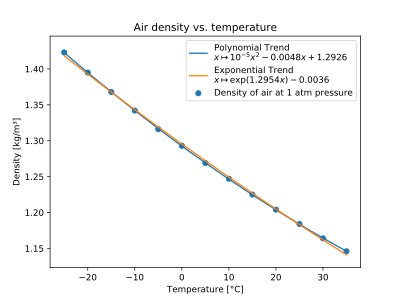
Aire
| T (° C) | ρ (kg / m 3 ) |
|---|---|
| −25 | 1.423 |
| −20 | 1.395 |
| −15 | 1.368 |
| −10 | 1.342 |
| −5 | 1.316 |
| 0 | 1.293 |
| 5 | 1.269 |
| 10 | 1.247 |
| 15 | 1.225 |
| 20 | 1.204 |
| 25 | 1.184 |
| 30 | 1.164 |
| 35 | 1.146 |
Volúmenes molares de fase líquida y sólida de elementos.
Unidades comunes
- kilogramo por metro cúbico (kg / m 3 )
El litro y las toneladas métricas no son parte del SI, pero su uso es aceptable, lo que lleva a las siguientes unidades:
- kilogramo por litro (kg / l)
- gramo por mililitro (g / mL)
- tonelada métrica por metro cúbico (t / m 3 )
Las densidades que utilizan las siguientes unidades métricas tienen exactamente el mismo valor numérico, una milésima parte del valor en (kg / m 3 ). El agua líquida tiene una densidad de aproximadamente 1 kg / dm 3 , lo que hace que cualquiera de estas unidades SI sea numéricamente conveniente de usar, ya que la mayoría de los sólidos y líquidos tienen densidades entre 0,1 y 20 kg / dm 3 .
- kilogramo por decímetro cúbico (kg / dm 3 )
- gramo por centímetro cúbico (g / cm 3 )
- 1 g / cm 3 = 1000 kg / m 3
- megagramo (tonelada métrica) por metro cúbico (Mg / m 3 )
- Avoirdupois onza por pulgada cúbica (1 g / cc ≈ 0.578036672 oz / cu in)
- Avoirdupois onza por onza líquida (1 g / cc ≈ 1.04317556 oz / fl. Oz = 1.04317556 lb / pinta)
- Avoirdupois libra por pulgada cúbica (1 g / cc ≈ 0.036127292 lb / cu in)
- libra por pie cúbico (1 g / cc ≈ 62.427961 lb / cu ft)
- libra por yarda cúbica (1 g / cc ≈ 1685.5549 lb / cu yd)
- libra por galón de líquido estadounidense (1 g / cc ≈ 8.34540445 lb / gal)
- libra por bushel estadounidense (1 g / cc ≈ 77.6888513 lb / bu)
- babosa por pie cúbico
Las unidades imperiales que difieren de las anteriores (como el galón imperial y el bushel difieren de las unidades de los EE. UU.) En la práctica rara vez se utilizan, aunque se encuentran en documentos más antiguos. El galón imperial se basó en el concepto de que una onza de agua líquida imperial tendría una masa de una onza de Avoirdupois, y de hecho 1 g / cc ≈ 1.00224129 onzas por onza de fluido imperial = 10.0224129 libras por galón imperial. La densidad de los metales preciosos podría estar basada en onzas y libras de Troya , una posible causa de confusión.




















No hay comentarios:
Publicar un comentario