marcapasos cardíaco , es decir, el marcapasos natural del corazón. En la mayoría de los seres humanos, la concentración de células marcapasos en elEl nodo sinoauricular (SA) es el marcapasos natural, y el ritmo resultante es un ritmo sinusal .
A veces, un marcapasos ectópico marca el ritmo, si el nodo SA está dañado o si el sistema de conducción eléctrica del corazón tiene problemas. Las arritmias cardíacas pueden causar un bloqueo cardíaco , en el que las contracciones pierden cualquier ritmo útil. En humanos, y ocasionalmente en animales, se puede usar un dispositivo mecánico llamado marcapasos artificial (o simplemente "marcapasos") después de dañar el sistema de conducción intrínseca del cuerpo para producir estos impulsos sintéticamente.

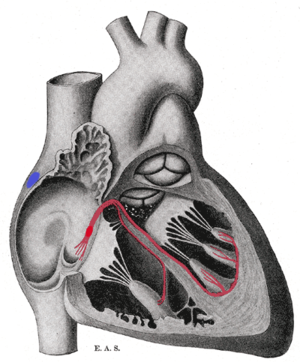
Imagen que muestra el marcapasos cardíaco o nodo SA, el marcapasos normal dentro del sistema de conducción eléctrica del corazón.
Control [ editar ]
Primaria (nodo SA) [ editar ]
El uno por ciento de los cardiomiocitos en el miocardio posee la capacidad de generar impulsos eléctricos (o potenciales de acción) de manera espontánea.
Una porción especializada del corazón, llamada nódulo sinoauricular (nodo SA), es responsable de la propagación auricular de este potencial.
Una porción especializada del corazón, llamada nódulo sinoauricular (nodo SA), es responsable de la propagación auricular de este potencial.
El nódulo sinoauricular ( nodo SA ) es un grupo de células ubicadas en la pared de la aurícula derecha , cerca de la entrada de la vena cava superior . Estas células son los cardiomiocitos modificados . Poseen filamentos contráctiles rudimentarios, pero se contraen relativamente débilmente en comparación con las células contráctiles cardíacas. [1]
Las células marcapasos están conectadas a células contráctiles vecinas a través de uniones , lo que les permite despolarizar localmente las células adyacentes. Las uniones de brecha permiten el paso de cationes positivos desde la despolarización de la célula del marcapasos hasta las células contráctiles adyacentes. Esto inicia la despolarización y el potencial de acción eventual en células contráctiles. Tener cardiomiocitos conectados a través de uniones de brecha permite que todas las células contráctiles del corazón actúen de manera coordinada y se contraigan como una unidad. Todo el tiempo está sincronizado con las células del marcapasos; esta es la propiedad que permite a las células marcapasos controlar la contracción en todos los demás cardiomiocitos.
Las células en el nodo SA se despolarizan espontáneamente , lo que finalmente produce una contracción, aproximadamente 100 veces por minuto. Esta tasa nativa se modifica constantemente por la actividad de las fibras nerviosas simpáticas y parasimpáticas a través del sistema nervioso autónomo , de modo que la tasa cardíaca promedio en reposo en humanos adultos es de aproximadamente 70 latidos por minuto. Debido a que el nódulo sinoauricular es responsable del resto de la actividad eléctrica del corazón, a veces se le llama el marcapasos primario .
Secundaria (unión AV y Bundle of His) [ editar ]
Si el nodo SA no funciona correctamente y no puede controlar la frecuencia cardíaca, un grupo de células más abajo en el corazón se convertirá en el marcapasos ectópico del corazón. Estas células forman el nodo Atrioventricular (o nodo AV ), que es un área entre la aurícula izquierda y el ventrículo derecho dentro del tabique auricular, que asumirá la responsabilidad del marcapasos.
Las células del nodo AV normalmente se descargan a aproximadamente 40-60 latidos por minuto, y se denominan marcapasos secundario .
Más abajo, el sistema de conducción eléctrica del corazón es el paquete de His . Las ramas izquierda y derecha de este paquete, y las fibras de Purkinje , también producirán un potencial de acción espontánea a una velocidad de 30-40 latidos por minuto, por lo que si los nodos SA y AV no funcionan, estas células pueden convertirse en marcapasos. Es importante darse cuenta de que estas células iniciarán los potenciales de acción y la contracción a un ritmo mucho más bajo que las células primarias o secundarias del marcapasos.
El nodo SA controla la tasa de contracción de todo el músculo cardíaco porque sus células tienen la tasa más rápida de despolarización espontánea, por lo que inician los potenciales de acción más rápido. El potencial de acción generado por el nodo SA pasa por el sistema de conducción eléctrica del corazón y despolariza las otras células marcapasos potenciales (nodo AV) para iniciar potenciales de acción antes de que estas otras células tengan la oportunidad de generar su propio potencial de acción espontáneo, por lo tanto se contraen y propagan los impulsos eléctricos al ritmo establecido por las células del nodo SA. Esta es la conducción normal de la actividad eléctrica en el corazón.
La generación de potenciales de acción [ editar ]
Hay 3 etapas principales en la generación de un potencial de acción en una célula marcapasos. Dado que las etapas son análogas a la contracción de las células musculares cardíacas , tienen el mismo sistema de denominación. Esto puede llevar a cierta confusión. No hay fase 1 o 2, solo fases 0, 3 y 4.
Fase 4 - Potencial de marcapasos [ editar ]
La clave para el disparo rítmico de las células marcapasos es que, a diferencia de otras neuronas en el cuerpo, estas células se despolarizarán lentamente por sí mismas y no necesitarán inervación externa del sistema nervioso autónomo para disparar potenciales de acción.
Como en todas las demás células, el potencial de reposo de una célula marcapasos (-60mV a -70mV) es causado por una salida continua o "fuga" de iones de potasio a través de las proteínas del canal iónico en la membrana que rodea a las células. Sin embargo, en las células marcapasos, esta permeabilidad del potasio (eflujo) disminuye a medida que pasa el tiempo, lo que provoca una despolarización lenta. Además, existe un flujo interno lento y continuo de sodio , denominado corriente "graciosa" o marcapasos.. Estos dos cambios relativos en la concentración de iones despolarizan lentamente (hacen más positivo) el potencial de membrana interno (voltaje) de la célula, dando a estas células su potencial de marcapasos. Cuando el potencial de membrana se despolariza a aproximadamente -40 mV, ha alcanzado el umbral (las células entran en la fase 0), lo que permite que se genere un potencial de acción.
Fase 0 - Upstroke [ editar ]
Aunque es mucho más rápido que la despolarización de la fase 4, la carrera ascendente en una célula marcapasos es lenta en comparación con la de un axón .
Los nódulos SA y AV no tienen canales de sodio rápidos como las neuronas, y la despolarización es causada principalmente por un flujo lento de iones de calcio. (La corriente divertida también aumenta). El calcio ingresa a la célula a través de canales de calcio sensibles al voltaje que se abren cuando se alcanza el umbral. Este influjo de calcio produce la fase ascendente del potencial de acción, lo que resulta en la reversión del potencial de membrana a un pico de aproximadamente + 10 mV. Es importante tener en cuenta que el calcio intracelular provoca la contracción muscular en las células contráctiles, y es el ion efector. En las células del marcapasos, la fase 0 depende de la activación de los canales de calcio tipo Len lugar de la activación de canales rápidos de sodio activados por voltaje, que son responsables de iniciar potenciales de acción en células contráctiles (sin marcapasos). Por esta razón, la pendiente de la fase ascendente del potencial de acción del marcapasos es más gradual que la de la célula contráctil (imagen 2). [7]
Fase 3 - Repolarización [ editar ]
La inversión del potencial de membrana desencadena la apertura de los canales de fuga de potasio, lo que resulta en la rápida pérdida de iones de potasio desde el interior de la célula, lo que provoca la repolarización (V m se vuelve más negativa). Los canales de calcio también se inactivan poco después de abrirse. Además, a medida que los canales de sodio se inactivan, la permeabilidad del sodio en la célula disminuye. Estos cambios en la concentración de iones repolarizan lentamente la célula al potencial de membrana en reposo (-60mV). Otra nota importante en esta fase es que las bombas iónicas restauran las concentraciones de iones al estado potencial de acción previa. La bomba iónica del intercambiador de sodio-calcio funciona para bombear el calcio fuera del espacio intracelular, relajando así efectivamente la célula. La bomba de sodio / potasio.restaura las concentraciones de iones de sodio y potasio bombeando sodio fuera de la célula y bombeando (intercambiando) potasio dentro de la célula. Restaurar estas concentraciones de iones es vital porque permite que la célula se reinicie y le permita repetir el proceso de despolarización espontánea que lleva a la activación de un potencial de acción.
Importancia clínica [ editar ]
Daño al nodo SA [ editar ]
Si el nodo SA no funciona, o el impulso generado en el nodo SA se bloquea antes de que descienda por el sistema de conducción eléctrica, un grupo de células más abajo en el corazón se convertirá en su marcapasos. [2] Este centro suele estar representado por células dentro del nodo atrioventricular ( nodo AV), que es un área entre las aurículas y los ventrículos , dentro del tabique auricular . Si el nodo AV también falla, las fibras de Purkinje pueden ocasionalmente actuar como el marcapasos predeterminado o de "escape". La razón por la que las células de Purkinje normalmente no controlan la frecuencia cardíaca es que generan potenciales de acción a una frecuencia más baja que los nodos AV o SA.
Este artículo necesita citas adicionales para su verificación . ( agosto de 2016 ) ( Aprenda cómo y cuándo eliminar este mensaje de plantilla )
|
| Terapia de resincronización cardíaca. | |
|---|---|
 | |
| ICD-9-CM | 00.51 , 00.54 |
| Malla | D058409 |
| eMedicina | 1839506-dispositivos |
La terapia de resincronización cardíaca ( TRC ) consiste en la inserción de electrodos en los ventrículos izquierdo y derecho del corazón, así como en ocasiones en la aurícula derecha , para tratar la insuficiencia cardíaca mediante la coordinación de la función de los ventrículos izquierdo y derecho. [1]
La TRC está indicada en pacientes que sufren una fracción de eyección baja (generalmente <35 font="" indica="" nbsp="" que="">insuficiencia cardíaca , donde la actividad eléctrica se ha visto comprometida, con una duración prolongada del QRS hasta> 120 ms . [2]
La inserción de electrodos en los ventrículos se realiza bajo anestesia local , con acceso a los ventrículos más comúnmente a través de la vena subclavia , aunque el acceso puede ser conferido desde las venas axilares o cefálicas . El acceso ventricular derecho es directo, mientras que el acceso ventricular izquierdo se confiere a través del seno coronario(CS).
Los desfibriladores CRT (CRT-D) también incorporan la función adicional de un cardioversor-desfibrilador implantable (ICD), para terminar rápidamente un ritmo cardíaco anormalmente rápido y potencialmente mortal. La TRC y la TRC-D se han convertido en opciones terapéuticas cada vez más importantes para los pacientes con insuficiencia cardíaca moderada y grave.
Indicaciones [ editar ]
La indicación clave para la TRC es el bloqueo de la rama izquierda (LBB) del corazón, una anomalía cardíaca que conduce a una contracción retardada del ventrículo izquierdo. El LBBB causa una prolongación de QRS de> 120 ms en el electrocardiograma , lo que contribuye a una mala coordinación del ventrículo izquierdo y una función sistólica reducida, lo que reduce la fracción de eyección (<35 font="" nbsp="">Esta reducción en la fracción de eyección es lo que consideramos insuficiencia cardíaca. [2]
Los pacientes con insuficiencia cardíaca generalmente se consideran si en la clase II o III la insuficiencia cardíaca , con las pautas actuales que indican que la TRC es inadecuada para la insuficiencia cardíaca de clase IV. [4]
Método [ editar ]
La TRC requiere la colocación de un dispositivo eléctrico para la estimulación biventricular, junto con la colocación de (al menos) dos derivaciones de estimulación, para facilitar la estimulación estable del ventrículo izquierdo y del ventrículo derecho. Para todos los elementos, la primera etapa del proceso es la anestesia local seguida de una incisión para permitir el abordaje desde la vena apropiada. Desde aquí, se pueden insertar los cables y el dispositivo. [1]
Derecho colocación de un electrodo ventricular [ editar ]
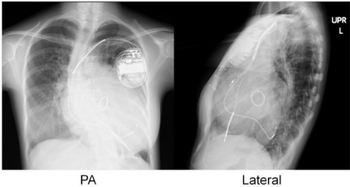
Se realiza una punción venosa y se inserta un cable guía en la vena, donde se guía, con el uso de imágenes de rayos X en tiempo real , hasta el ventrículo derecho. Luego, el cable guía se usa para ayudar a colocar el cable del electrodo, que viaja a través del sistema venoso hacia el ventrículo derecho donde está incrustado el electrodo. [1]
Colocación de un electrodo ventricular izquierda [ editar ]
Esto generalmente se realiza después de la colocación del cable VD, y el cable RV proporciona una copia de seguridad en caso de daño accidental a las fibras eléctricas del corazón , causando un evento asistólico . Al igual que con el cable RV, primero se inserta un cable guía, lo que permite la inserción de un catéter de administración múltiple . El catéter se maniobra posteriormente hacia la abertura del seno coronario en la aurícula derecha. Desde aquí se inyecta un medio de contraste que permite al equipo quirúrgico obtener un fleobograma del seno coronario para dirigir la colocación de la derivación hacia la vena coronaria más adecuada . [1]
Una vez que se ha obtenido el flebograma, el catéter de administración múltiple se utiliza para guiar el cable, desde la vena de entrada elegida, hacia la aurícula derecha, a través del seno coronario y hacia la vena cardíaca correspondiente. [1]
La colocación del cable ventricular izquierdo es el elemento más complicado y potencialmente peligroso de la operación, debido a la significativa variabilidad de la estructura venosa coronaria. Las alteraciones en la estructura del corazón, depósitos de grasa, válvulas y variaciones naturales causan complicaciones adicionales en el proceso de canulación. [1]
Colocación del dispositivo [ editar ]
El dispositivo se inserta en un bolsillo subcutáneo creado por el cirujano; la elección del lado izquierdo o derecho de la pared torácica está determinada principalmente por la preferencia del paciente o la ubicación del dispositivo preexistente. El dispositivo, similar al de un marcapasos tradicional , generalmente no es más grande que un reloj de bolsillo y tiene insertos para los electrodos. [1]
Complicaciones [ editar ]
Las complicaciones clave incluyen: [2]
- Disección o perforación del seno coronario que a su vez puede causar derrame pericárdico
- Incapacidad para canular el seno coronario (aproximadamente el 5% de los pacientes)
- Perforación miocárdica , neumotórax e infección , todos los cuales tienen una incidencia inferior al 1%.
Tecnología [ editar ]
Varios trabajos de investigación [6] [7] han propuesto plataformas de software para planificar y guiar la implantación de dispositivos CRT. Esta investigación propone utilizar imágenes preoperatorias para caracterizar la activación del tejido y el ventrículo izquierdo para identificar posibles regiones objetivo para el despliegue de los cables CRT.
No hay comentarios:
Publicar un comentario