En fisiología , un potencial de acción se produce cuando el potencial de membrana de una ubicación específica del axón aumenta y disminuye rápidamente: [1] esta despolarización hace que las ubicaciones adyacentes se despolaricen de manera similar. Los potenciales de acción se producen en varios tipos de células animales , llamadas células excitables , que incluyen neuronas , células musculares , células endocrinas y en algunas células vegetales .
En las neuronas, los potenciales de acción desempeñan un papel central en la comunicación célula a célula al proporcionar, o con respecto a la conducción saltatoria , ayudar a la propagación de señales a lo largo del axón de la neurona hacia los botones sinápticos situados en los extremos de un axón; estas señales pueden conectarse con otras neuronas en sinapsis, o con células motoras o glándulas. En otros tipos de células, su función principal es activar procesos intracelulares. En las células musculares, por ejemplo, un potencial de acción es el primer paso en la cadena de eventos que conducen a la contracción. En las células beta del páncreas , provocan la liberación de insulina . [una]Los potenciales de acción en las neuronas también se conocen como " impulsos nerviosos " o "picos", y la secuencia temporal de los potenciales de acción generados por una neurona se llama " tren de picos ". Una neurona que emite un potencial de acción, o impulso nervioso, a menudo se dice que "dispara".
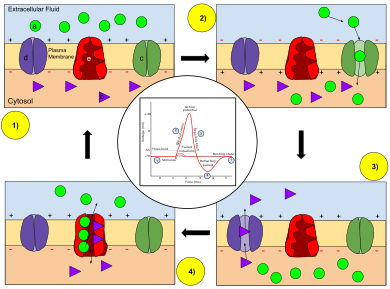
Los potenciales de acción son generados por tipos especiales de canales iónicos activados por voltajeincrustados en la membrana plasmática de una célula . [b] Estos canales se cierran cuando el potencial de membrana está cerca del potencial de reposo (negativo) de la célula, pero comienzan a abrirse rápidamente si el potencial de membrana aumenta hasta una tensión de umbral definida con precisión, despolarizando el potencial transmembrana. [b] Cuando los canales se abren, permiten un flujo interno de sodioiones, que cambia el gradiente electroquímico, que a su vez produce un aumento adicional en el potencial de membrana. Esto hace que se abran más canales, lo que produce una mayor corriente eléctrica a través de la membrana celular y así sucesivamente. El proceso avanza de forma explosiva hasta que todos los canales de iones disponibles están abiertos, lo que resulta en un gran aumento en el potencial de la membrana. La rápida entrada de iones de sodio hace que la polaridad de la membrana plasmática se invierta, y los canales iónicos se inactivan rápidamente. A medida que los canales de sodio se cierran, los iones de sodio ya no pueden ingresar a la neurona, y luego son transportados activamente de vuelta a la membrana plasmática. Potasiolos canales se activan y hay una corriente externa de iones de potasio que devuelve el gradiente electroquímico al estado de reposo. Después de que se haya producido un potencial de acción, se produce un cambio negativo transitorio, denominado pospolarización posterior .
En las células animales, hay dos tipos principales de potenciales de acción. Un tipo es generado por canales de sodio regulados por voltaje, el otro por canales de calcio regulados por voltaje . Los potenciales de acción basados en sodio usualmente duran menos de un milisegundo, pero los potenciales de acción basados en calcio pueden durar 100 milisegundos o más. [2] En algunos tipos de neuronas, los picos de calcio lentos proporcionan la fuerza motriz para una explosión prolongada de picos de sodio de emisión rápida. En las células musculares cardíacas, por otro lado, una espiga inicial de sodio rápida proporciona un "cebador" para provocar el rápido inicio de una espiga de calcio, que luego produce contracción muscular. [2]
En el modelo de capacitancia de membrana de Hodgkin-Huxley , la velocidad de transmisión de un potencial de acción no estaba definida y se asumió que las áreas adyacentes se despolarizaron debido a la interferencia de iones liberados con los canales vecinos. Las mediciones de la difusión de iones y los radios han demostrado que esto no es posible. Además, las mediciones contradictorias de los cambios de entropía y el tiempo disputaron que el modelo de capacitancia actuaba solo.
Descripción general [ editar ]
Casi todas las membranas celulares en animales, plantas y hongos mantienen una diferencia de voltaje entre el exterior y el interior de la célula, llamado potencial de membrana . Un voltaje típico a través de la membrana de una célula animal es −70 mV. Esto significa que el interior de la celda tiene un voltaje negativo de aproximadamente una decimoquinta parte de un voltio en relación con el exterior. En la mayoría de los tipos de células, el potencial de membrana generalmente permanece bastante constante. Sin embargo, algunos tipos de células son eléctricamente activas en el sentido de que sus voltajes fluctúan con el tiempo. En algunos tipos de células eléctricamente activas, incluidas las neuronasy en las células musculares, las fluctuaciones de voltaje frecuentemente toman la forma de un rápido aumento ascendente seguido de una rápida caída. Estos ciclos de subida y bajada se conocen como potenciales de acción . En algunos tipos de neuronas, todo el ciclo de altibajos tiene lugar en unas pocas milésimas de segundo. En las células musculares, un potencial de acción típico dura aproximadamente una quinta parte de un segundo. En algunos otros tipos de células, y también en plantas, un potencial de acción puede durar tres segundos o más.
Las propiedades eléctricas de una célula están determinadas por la estructura de la membrana que la rodea. Una membrana celular consiste en una bicapa lipídica de moléculas en las que están incrustadas moléculas de proteínas más grandes. La bicapa lipídica es altamente resistente al movimiento de iones cargados eléctricamente, por lo que funciona como un aislante. Las grandes proteínas integradas en la membrana, en contraste, proporcionan canales a través de los cuales los iones pueden pasar a través de la membrana. Los potenciales de acción son impulsados por proteínas de canal cuya configuración cambia entre estados cerrados y abiertos en función de la diferencia de voltaje entre el interior y el exterior de la celda. Estas proteínas sensibles al voltaje son conocidas como canales iónicos dependientes de voltaje .
Proceso en una neurona típica [ editar ]
Todas las células en los tejidos del cuerpo animal están polarizadas eléctricamente ; en otras palabras, mantienen una diferencia de voltaje a través de la membrana plasmática de la célula , conocida como potencial de membrana . Esta polarización eléctrica resulta de una interacción compleja entre las estructuras de proteínas incrustadas en la membrana llamadas bombas de iones y canales de iones . En las neuronas, los tipos de canales iónicos en la membrana por lo general varían a lo largo de diferentes partes de la célula, lo que proporciona dendritas , axones y cuerpos celulares.Diferentes propiedades eléctricas. Como resultado, algunas partes de la membrana de una neurona pueden ser excitables (capaces de generar potenciales de acción), mientras que otras no lo son. Estudios recientes [ cita requerida ] han demostrado que la parte más excitable de una neurona es la parte posterior a la colina del axón (el punto donde el axón abandona el cuerpo celular), que se denomina segmento inicial, pero el axón y el cuerpo celular también son Excitable en la mayoría de los casos.
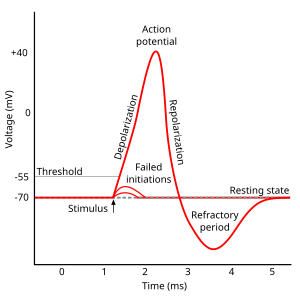
Cada parche de membrana excitable tiene dos niveles importantes de potencial de membrana: el potencial de reposo , que es el valor que mantiene el potencial de membrana siempre que nada perturbe la célula, y un valor más alto llamado potencial de umbral . En el montículo de axones de una neurona típica, el potencial de reposo es de alrededor de –70 milivoltios (mV) y el potencial de umbral es de alrededor de –55 mV. Las entradas sinápticas a una neurona hacen que la membrana se despolarice o hiperpolarice; es decir, hacen que el potencial de membrana aumente o disminuya. Los potenciales de acción se activan cuando se acumula suficiente despolarización para llevar el potencial de la membrana al umbral. Cuando se dispara un potencial de acción, el potencial de membrana se dispara abruptamente hacia arriba y luego se dispara hacia atrás de manera igualmente abrupta, a menudo terminando por debajo del nivel de reposo, donde permanece durante un período de tiempo. La forma del potencial de acción es estereotipada; esto significa que el aumento y la caída suelen tener aproximadamente la misma amplitud y curso de tiempo para todos los potenciales de acción en una celda determinada. (Las excepciones se discuten más adelante en el artículo). En la mayoría de las neuronas, todo el proceso tiene lugar en aproximadamente una milésima de segundo. Muchos tipos de neuronas emiten potenciales de acción constantemente a velocidades de hasta 10–100 por segundo. Sin embargo, algunos tipos son mucho más silenciosos,
Base biofísica [ editar ]
Esta sección necesita citas adicionales para su verificación . ( febrero de 2014 ) ( Aprenda cómo y cuándo eliminar este mensaje de plantilla )
|
Los potenciales de acción resultan de la presencia en la membrana de una célula de tipos especiales de canales iónicos regulados por voltaje . [3] Un canal de iones regulado por voltaje es un grupo de proteínas incrustadas en la membrana que tiene tres propiedades clave:
- Es capaz de asumir más de una conformación.
- Al menos una de las conformaciones crea un canal a través de la membrana que es permeable a tipos específicos de iones.
- La transición entre conformaciones está influenciada por el potencial de membrana.
Por lo tanto, un canal de iones dependiente de voltaje tiende a estar abierto para algunos valores del potencial de membrana, y cerrado para otros. En la mayoría de los casos, sin embargo, la relación entre el potencial de membrana y el estado del canal es probabilística e implica un retraso de tiempo. Los canales iónicos cambian entre conformaciones en momentos impredecibles: el potencial de membrana determina la velocidad de las transiciones y la probabilidad por unidad de tiempo de cada tipo de transición.
Los canales iónicos controlados por voltaje son capaces de producir potenciales de acción porque pueden dar lugar a una retroalimentación positivabucles: el potencial de membrana controla el estado de los canales iónicos, pero el estado de los canales de iones controla el potencial de membrana. Por lo tanto, en algunas situaciones, un aumento en el potencial de membrana puede hacer que los canales iónicos se abran, causando así un aumento adicional en el potencial de membrana. Un potencial de acción ocurre cuando este ciclo de retroalimentación positiva procede de manera explosiva. El tiempo y la trayectoria de amplitud del potencial de acción están determinados por las propiedades biofísicas de los canales iónicos activados por voltaje que lo producen. Existen varios tipos de canales capaces de producir la retroalimentación positiva necesaria para generar un potencial de acción. Los canales de sodio dependientes del voltaje son responsables de los potenciales de acción rápidos involucrados en la conducción nerviosa. Los canales de calcio dependientes de voltaje generan potenciales de acción más lentos en las células musculares y algunos tipos de neuronas. Cada uno de estos tipos viene en múltiples variantes, con diferentes sensibilidades de voltaje y diferentes dinámicas temporales.
El tipo más estudiado de canales iónicos dependientes de voltaje comprende los canales de sodio involucrados en la conducción nerviosa rápida. Estos son a veces conocidos como canales de sodio Hodgkin-Huxley porque se caracterizaron por primera vez por Alan Hodgkin y Andrew Huxley en sus estudios ganadores del Premio Nobel de la biofísica de potencial de acción, pero puede más convenientemente ser referidos como Na V canales. (La "V" significa "voltaje".) Un canal de Na V tiene tres estados posibles, conocidos como desactivado , activado e inactivo . El canal es permeable solo a los iones de sodio cuando está en el activadoestado. Cuando el potencial de membrana es bajo, el canal pasa la mayor parte de su tiempo en el estado desactivado (cerrado). Si el potencial de membrana se eleva por encima de un cierto nivel, el canal muestra una mayor probabilidad de transición al estado activado (abierto). Cuanto mayor sea el potencial de membrana, mayor será la probabilidad de activación. Una vez que un canal se ha activado, eventualmente pasará al estado inactivado (cerrado). Por lo tanto, tiende a permanecer inactivo durante algún tiempo, pero, si el potencial de la membrana vuelve a ser bajo, el canal finalmente volverá al estado desactivado . Durante un potencial de acción, la mayoría de los canales de este tipo pasan por un ciclo desactivado → activado→ inactivado → desactivado . Sin embargo, este es solo el comportamiento promedio de la población: un canal individual puede, en principio, realizar cualquier transición en cualquier momento. Sin embargo, la probabilidad de que un canal pase del estado inactivado directamente al estado activado es muy baja: un canal en el estado inactivo es refractario hasta que haya pasado de nuevo al estado desactivado .
El resultado de todo esto es que la cinética de los canales de Na V se rige por una matriz de transición cuyas velocidades dependen de la tensión de una manera complicada. Dado que estos canales juegan un papel importante en la determinación del voltaje, la dinámica global del sistema puede ser bastante difícil de resolver. Hodgkin y Huxley abordaron el problema desarrollando un conjunto de ecuaciones diferenciales para los parámetros que gobiernan los estados del canal iónico, conocidas como ecuaciones de Hodgkin-Huxley . Estas ecuaciones han sido modificadas ampliamente por investigaciones posteriores, pero constituyen el punto de partida para la mayoría de los estudios teóricos de biofísica del potencial de acción.
A medida que aumenta el potencial de membrana, los canales de iones de sodio seabren, lo que permite la entrada de iones de sodio en la célula. A esto le sigue la apertura de los canales de iones de potasio que permiten la salida de los iones de potasio de la célula. El flujo de entrada de iones de sodio aumenta la concentración de cationescargados positivamente en la célula y causa despolarización, donde el potencial de la célula es más alto que el potencial de reposode la célula.. Los canales de sodio se cierran en el pico del potencial de acción, mientras que el potasio continúa saliendo de la célula. El flujo de iones de potasio disminuye el potencial de membrana o hiperpolariza la célula. Para pequeños aumentos de voltaje desde el reposo, la corriente de potasio excede la corriente de sodio y el voltaje regresa a su valor de reposo normal, generalmente de −70 mV. [4] [5] [6] Sin embargo, si el voltaje aumenta más allá de un umbral crítico, típicamente 15 mV más alto que el valor de reposo, la corriente de sodio domina. Esto resulta en una condición fuera de control por la cual la retroalimentación positiva de la corriente de sodio activa aún más canales de sodio. Así, la célula dispara , produciendo un potencial de acción. [4] [7] [8][nota 1] La frecuencia con la que una neurona provoca potenciales de acción se suele denominar velocidad de disparo ovelocidad de disparo neural .
Las corrientes producidas por la apertura de canales activados por voltaje en el curso de un potencial de acción son típicamente significativamente más grandes que la corriente estimulante inicial. Por lo tanto, la amplitud, la duración y la forma del potencial de acción están determinadas en gran medida por las propiedades de la membrana excitable y no por la amplitud o la duración del estímulo. Esta propiedad de todo o nada del potencial de acción lo diferencia de los potenciales graduados , como los potenciales de los receptores , los potenciales electrotónicos y los potenciales sinápticos , que se escalan con la magnitud del estímulo. Existe una variedad de tipos de potenciales de acción en muchos tipos de celdas y compartimientos de celdas, según lo determinado por los tipos de canales dependientes de voltaje,Canales de fugas , distribuciones de canales, concentraciones iónicas, capacitancia de la membrana, temperatura y otros factores.
Los principales iones involucrados en un potencial de acción son los cationes de sodio y potasio; Los iones de sodio entran en la célula, y los iones de potasio se van, restaurando el equilibrio. Relativamente pocos iones necesitan cruzar la membrana para que el voltaje de la membrana cambie drásticamente. Los iones intercambiados durante un potencial de acción, por lo tanto, hacen un cambio insignificante en las concentraciones iónicas interiores y exteriores. Los pocos iones que se cruzan son bombeados nuevamente por la acción continua de la bomba de sodio-potasio , que, junto con otros transportadores de iones , mantiene la proporción normal de concentraciones de iones a través de la membrana. Los cationes de calcio y los aniones de cloruro están involucrados en algunos tipos de potenciales de acción, como elEl potencial de acción cardíaco y el potencial de acción en el Acetabularia de alga unicelular , respectivamente.
Aunque los potenciales de acción se generan localmente en parches de membrana excitable, las corrientes resultantes pueden desencadenar potenciales de acción en tramos vecinos de membrana, precipitando una propagación similar al dominó. En contraste con la propagación pasiva de los potenciales eléctricos (potencial electrotónico ), los potenciales de acción se generan nuevamente a lo largo de tramos excitables de membrana y se propagan sin decaer. [9] Las secciones mielinizadas de los axones no son excitables y no producen potenciales de acción y la señal se propaga pasivamente como potencial electrotónico . Los parches no mielinizados espaciados regularmente, llamados nodos de Ranvier , generan potenciales de acción para aumentar la señal. Conocido como conducción saltatoria., este tipo de propagación de señal proporciona una compensación favorable de la velocidad de la señal y el diámetro del axón. La despolarización de los terminales de los axones , en general, desencadena la liberación del neurotransmisor en la hendidura sináptica . Además, se han registrado potenciales de acción de propagación hacia atrás en las dendritas de las neuronas piramidales , que son ubicuas en la neocorteza. [c] Se cree que estos tienen un papel en la plasticidad dependiente del tiempo de espiga .




No hay comentarios:
Publicar un comentario