 | ||||||||||||||||
| Bromo | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Pronunciación | / B r oʊ m i n , | |||||||||||||||
| Apariencia | Marrón rojizo | |||||||||||||||
| Peso atómico estándar A r, std (Br) | [ 79.901 , 79.907 ] convencional: 79.904 | |||||||||||||||
| El bromo en la tabla periódica. | ||||||||||||||||
| ||||||||||||||||
| Número atómico ( z ) | 35 | |||||||||||||||
| Grupo | grupo 17 (halógenos) | |||||||||||||||
| Período | periodo 4 | |||||||||||||||
| Bloquear | bloque p | |||||||||||||||
| Categoría de elemento | no metal reactivo | |||||||||||||||
| Configuración electronica | [ Ar ] 3d 10 4s 2 4p 5 | |||||||||||||||
Electrones por concha
| 2, 8, 18, 7 | |||||||||||||||
| Propiedades físicas | ||||||||||||||||
| Fase en STP | líquido | |||||||||||||||
| Punto de fusion | 265.8 K (−7.2 ° C, 19 ° F) | |||||||||||||||
| Punto de ebullición | 332.0 K (58.8 ° C, 137.8 ° F) | |||||||||||||||
| Densidad (cerca de rt ) | Br 2 , líquido: 3.1028 g / cm 3 | |||||||||||||||
| Triple punto | 265.90 K, 5.8 kPa [1] | |||||||||||||||
| Punto crítico | 588 K, 10.34 MPa [1] | |||||||||||||||
| Calor de fusión | (Br 2 ) 10.571 kJ / mol | |||||||||||||||
| Calor de vaporización. | (Br 2 ) 29.96 kJ / mol | |||||||||||||||
| Capacidad de calor molar | (Br 2 ) 75.69 J / (mol · K) | |||||||||||||||
Presión de vapor
| ||||||||||||||||
| Propiedades atómicas | ||||||||||||||||
| Estados de oxidación | −1 , +1 , +3 , +4, +5 , +7 (unóxidofuertementeácido ) | |||||||||||||||
| Electronegatividad | Escala de Pauling: 2.96 | |||||||||||||||
| Energías de ionización |
| |||||||||||||||
| Radio atómico | empírico: 120 hs. | |||||||||||||||
| Radio covalente | 120 ± 3 pm | |||||||||||||||
| Radio de van der waals | 185 pm | |||||||||||||||
| Lineas espectrales de bromo. | ||||||||||||||||
| Otras propiedades | ||||||||||||||||
| Natural occurrence | primordial | |||||||||||||||
| Crystal structure | orthorhombic | |||||||||||||||
| Speed of sound | 206 m/s (at 20 °C) | |||||||||||||||
| Thermal conductivity | 0.122 W/(m·K) | |||||||||||||||
| Electrical resistivity | 7.8×1010 Ω·m (at 20 °C) | |||||||||||||||
| Magnetic ordering | diamagnetic[2] | |||||||||||||||
| Magnetic susceptibility | −56.4·10−6 cm3/mol[3] | |||||||||||||||
| CAS Number | 7726-95-6 | |||||||||||||||
| History | ||||||||||||||||
| Discovery and first isolation | Antoine Jérôme Balardand Carl Jacob Löwig(1825) | |||||||||||||||
| Main isotopes of bromine | ||||||||||||||||
| ||||||||||||||||
El bromo es un elemento químico con el símbolo Br y el número atómico 35. Es el tercer halógeno más ligero , y es un líquidohumeante con un color rojo intenso. A temperatura ambiente, el bromo se evapora fácilmente para formar un gas de color rojo a ámbar [4] . Las propiedades del bromo son intermedias entre las del cloro y el yodo . Aislado de manera independiente por dos químicos, Carl Jacob Löwig (en 1825) y Antoine Jérôme Balard(en 1826), su nombre se deriva del griego antiguo βρῶμος ("hedor"), que hace referencia a su olor agudo y desagradable.
El bromo elemental es muy reactivo y, por lo tanto, no se encuentra libre en la naturaleza, pero en sales de haluro mineral cristalino soluble incoloro , análogo a la sal de mesa . Si bien es bastante raro en la corteza terrestre, la alta solubilidad del ion bromuro (Br - ) ha causado su acumulación en los océanos. Comercialmente, el elemento se extrae fácilmente de las reservas de salmuera , principalmente en los Estados Unidos, Israel y China. La masa de bromo en los océanos es aproximadamente una tres centésima parte del cloro.
A altas temperaturas, los compuestos de organobromina se disocian fácilmente para producir átomos de bromo libres, un proceso que detiene las reacciones químicas en cadena de los radicales libres . Este efecto hace que los compuestos de organobromina sean útiles como retardantes del fuego , y más de la mitad del bromo producido en todo el mundo cada año se destina a este propósito. La misma propiedad hace que la luz solar ultravioleta disocie los compuestos volátiles de organobromina en la atmósfera para producir átomos de bromo libres, lo que causa el agotamiento del ozono . Como resultado, muchos compuestos organobromuro, como el pesticida bromuro de metilo, ya no se utilizan. Los compuestos de bromo todavía se utilizan en Perforación de fluidos de pozos , en película fotográfica, y como intermediario en la fabricación de productos químicos orgánicos .
Grandes cantidades de sales de bromuro son tóxicas por la acción del ion bromuro soluble, causando bromismo . Sin embargo, recientemente se ha dilucidado un claro papel biológico para el ion bromuro y el ácido hipobromoso, y ahora parece que el bromo es un oligoelemento esencial en los seres humanos. El papel de los compuestos orgánicos de organobromina en la vida marina, como las algas, se conoce desde hace mucho tiempo. Como producto farmacéutico , el ion bromuro simple (Br - ) tiene efectos inhibidores sobre el sistema nervioso central, y las sales de bromuro fueron una vez un sedante médico importante, antes de ser reemplazadas por medicamentos de acción más corta. Conservan usos de nicho como antiepilépticos .
Historia [ editar ]
Bromine fue descubierto independientemente por dos químicos, Carl Jacob Löwig [5] y Antoine Balard , [6] [7] en 1825 y 1826, respectivamente. [8]
Löwig aisló bromo de una fuente de agua mineral de su ciudad natal, Bad Kreuznach, en 1825. Löwig utilizó una solución de la sal mineral saturada con cloro y extrajo el bromo con éter dietílico . Después de la evaporación del éter quedó un líquido marrón. Con este líquido como muestra de su trabajo, solicitó un puesto en el laboratorio de Leopold Gmelin en Heidelberg . La publicación de los resultados se retrasó y Balard publicó sus resultados primero. [9]
Balard encontró sustancias químicas de bromo en las cenizas de algas marinas de las salinas de Montpellier . Las algas se utilizaron para producir yodo, pero también contenían bromo. Balard destiló el bromo de una solución de ceniza de algas saturada con cloro. Las propiedades de la sustancia resultante fueron intermedias entre las de cloro y yodo; por lo tanto, intentó probar que la sustancia era monocloruro de yodo (ICl), pero después de no hacerlo, estuvo seguro de haber encontrado un nuevo elemento, y lo llamó muride, derivado de la palabra latina muria para salmuera. [7]
Después de los químicos franceses Louis Nicolas Vauquelin , Louis Jacques Thénard y Joseph-Louis Gay-Lussac aprobaran los experimentos del joven farmacéutico Balard, los resultados se presentaron en una conferencia de la Académie des Sciences y se publicaron en Annales de Chimie et Physique . [6] En su publicación, Balard afirma que cambió el nombre de muride a brôme a propuesta de M. Anglada. Brôme (bromo) deriva del griego βρωμος (hedor). [6] [10] Otras fuentes afirman que el químico y físico francés Joseph-Louis Gay-LussacSugirió el nombre brôme para el olor característico de los vapores. [11] [12] El bromo no se produjo en grandes cantidades hasta 1858, cuando el descubrimiento de depósitos de sal en Stassfurt permitió su producción como un subproducto de la potasa. [13]
Aparte de algunas aplicaciones médicas menores, el primer uso comercial fue el daguerrotipo . En 1840, se descubrió que el bromo tenía algunas ventajas sobre el vapor de yodo utilizado anteriormente para crear la capa de haluro de plata sensible a la luz en daguerrotipo. [14]
Se utilizaron bromuro de potasio y bromuro de sodio como anticonvulsivos y sedantes. a fines del siglo XIX y principios del XX, pero fueron reemplazados gradualmente por hidrato de cloral y luego por barbitúricos . [15] En los primeros años de la Primera Guerra Mundial , se utilizaron compuestos de bromo como el bromuro de xililocomo gas venenoso . [dieciséis]
Propiedades [ editar ]
El bromo es el tercer halógeno , siendo un no metal en el grupo 17 de la tabla periódica. Sus propiedades son similares a las del flúor , el cloro y el yodo , y tienden a ser intermedias entre las de los dos halógenos vecinos, el cloro y el yodo. El bromo tiene la configuración electrónica [Ar] 3d 10 4s 2 4p 5 , con los siete electrones en la cuarta capa y la capa más externa que actúan como sus electrones de valencia . Como todos los halógenos, es por lo tanto un electrón por debajo de un octeto completo, y por lo tanto es un agente oxidante fuerte, que reacciona con muchos elementos para completar su capa exterior. [17]Correspondiente a las tendencias periódicas , es intermedia en electronegatividad entre el cloro y el yodo (F: 3.98, Cl: 3.16, Br: 2.96, I: 2.66), y es menos reactiva que el cloro y más reactiva que el yodo. También es un agente oxidante más débil que el cloro, pero más fuerte que el yodo. A la inversa, el ion bromuro es un agente reductor más débil que el yoduro, pero más fuerte que el cloruro. [17] Estas similitudes llevaron a que el cloro, el bromo y el yodo se clasificaran como una de las tríadas originales de Johann Wolfgang Döbereiner , cuyo trabajo prefiguró la ley periódica de los elementos químicos. [18] [19] Es intermedio enradio atómico entre el cloro y el yodo, y esto hace que muchas de sus propiedades atómicas tengan un valor intermedio similar entre el cloro y el yodo, como la primera energía de ionización , la afinidad electrónica , la entalpía de disociación de la molécula X 2 (X = Cl, Br, I), radio iónico y longitud de enlace X – X. [17] La volatilidad del bromo acentúa su olor muy penetrante, asfixiante y desagradable. [20]
Los cuatro halógenos estables experimentan fuerzas de atracción intermoleculares de van der Waals , y su fuerza aumenta junto con el número de electrones entre todas las moléculas de halógeno diatómicas homonucleares. Por lo tanto, los puntos de fusión y ebullición del bromo son intermedios entre los del cloro y el yodo. Como resultado del aumento del peso molecular de los halógenos en el grupo, la densidad y los calores de fusión y vaporización del bromo son nuevamente intermedios entre los del cloro y el yodo, aunque todos sus calores de vaporización son bastante bajos (lo que lleva a una alta volatilidad) Gracias a su estructura molecular diatómica. [17]Los halógenos se oscurecen a medida que el grupo desciende: el flúor es un gas amarillo muy pálido, el cloro es amarillo verdoso y el bromo es un líquido volátil de color marrón rojizo que se funde a -7.2 ° C y hierve a 58.8 ° C. (El yodo es un sólido negro brillante). Esta tendencia se produce porque las longitudes de onda de la luz visible absorbida por los halógenos aumentan en el grupo. [17] Específicamente, el color de un halógeno, como el bromo, es el resultado de la transición electrónica entre el antígeno más ocupado ocupado πorbital molecular g dey el orbital molecular de anti-enlace vacante más bajo σ u . [21] El color se desvanece a bajas temperaturas, de modo que el bromo sólido a −195 ° C es amarillo pálido.[17]
Al igual que el cloro sólido y el yodo, el bromo sólido se cristaliza en el sistema de cristal ortorrómbico , en una red de capas de moléculas de Br 2 . La distancia Br – Br es 227 pm (cerca de la distancia Br – Br gaseosa de 228 pm) y la distancia Br ··· Br entre moléculas es 331 pm dentro de una capa y 399 pm entre capas (compare el radio de van der Waals de bromo, 195 pm). Esta estructura significa que el bromo es un conductor de electricidad muy pobre, con una conductividad de alrededor de 5 × 10 −13 Ω −1 cm −1 justo por debajo del punto de fusión, aunque es mejor que la conductividad esencialmente indetectable del cloro. [17]
A una presión de 55. GPa (aproximadamente 540,000 veces la presión atmosférica), el bromo sufre una transición de aislante a metal. A 75 GPa, cambia a una estructura ortorrómbica centrada en la cara. A 100 GPa, cambia a una forma monoatómica ortorrómbica centrada en el cuerpo. [22]
Isótopos [ editar ]
El bromo tiene dos isótopos estables, 79 Br y 81 Br. Estos son sus dos únicos isótopos naturales, con 79 Br que representan el 51% de bromo natural y 81 Br el 49% restante. Ambos tienen espín nuclear 3 / 2− y, por lo tanto, pueden usarse para resonancia magnética nuclear , aunque 81 Br es más favorable. La distribución relativa 1: 1 de los dos isótopos en la naturaleza es útil en la identificación de compuestos que contienen bromo utilizando espectroscopia de masas. Otros isótopos de bromo son todos radiactivos, con vidas medias demasiado cortas para ocurrir en la naturaleza. De estos, los más importantes son 80 Br ( t 1/2 = 17.7 min), 80mBr ( t 1/2 = 4.421 h) y 82 Br ( criptón ; y 80 Br pueden decaer en cualquiera de los dos modos para estabilizar 80 Se ot 1/2 = 35.28 h), que puede producirse a partir de la activación de neutrones del bromo natural. [17] El radioisótopo de bromo más estable es 77 Br ( t 1/2 = 57.04 h). El modo de decaimiento primario de los isótopos más livianos que 79 Br es la captura de electrones a los isótopos de selenio ; la de los isótopos más pesados que 81 Br es la desintegración beta de los isótopos de 80 Kr.[23]
Química y compuestos [ editar ]
| X | XX | HX | BX3 | Alx3 | CX4 |
|---|---|---|---|---|---|
| F | 159 | 574 | 645 | 582 | 456 |
| Cl | 243 | 428 | 444 | 427 | 327 |
| Br | 193 | 363 | 368 | 360 | 272 |
| yo | 151 | 294 | 272 | 285 | 239 |
El bromo tiene una reactividad intermedia entre el cloro y el yodo, y es uno de los elementos más reactivos. Las energías de enlace al bromo tienden a ser más bajas que las del cloro pero más altas que las del yodo, y el bromo es un agente oxidante más débil que el cloro pero más fuerte que el yodo. Esto se puede ver en los potenciales de electrodo estándar de las parejas X 2 / X - (F, +2.866 V; Cl, +1.395 V; Br, +1.087 V; I, +0.615 V; At, aproximadamente +0.3 V). La bromación a menudo conduce a estados de oxidación más altos que la yodación, pero estados de oxidación más bajos o iguales a la cloración. El bromo tiende a reaccionar con compuestos que incluyen enlaces M – M, M – H o M – C para formar enlaces M – Br. [21]
Bromuro de hidrógeno [ editar ]
El compuesto más simple de bromo es bromuro de hidrógeno , HBr. Se utiliza principalmente en la producción de bromuros inorgánicos y bromuros de alquilo , y como catalizador para muchas reacciones en química orgánica. Industrialmente, se produce principalmente por la reacción de hidrógeno gas con gas bromo a 200-400 ° C con un catalizador de platino . Sin embargo, la reducción de bromo con fósforo rojo es una forma más práctica de producir bromuro de hidrógeno en el laboratorio: [24]
- 2 P + 6 H 2 O + 3 Br 2 → 6 HBr + 2 H 3 PO 3
- H 3 PO 3 + H 2 O + Br 2 → 2 HBr + H 3 PO 4
A temperatura ambiente, el bromuro de hidrógeno es un gas incoloro, como todos los haluros de hidrógeno , aparte del fluoruro de hidrógeno , ya que el hidrógeno no puede formar enlaces de hidrógeno fuertes al átomo de bromo grande y solo ligeramente electronegativo; sin embargo, el enlace de hidrógeno débil está presente en bromuro de hidrógeno cristalino sólido a bajas temperaturas, similar a la estructura de fluoruro de hidrógeno, antes de que el desorden comience a prevalecer a medida que aumenta la temperatura. [24] El bromuro de hidrógeno acuoso se conoce como ácido bromhídrico , que es un ácido fuerte (p K a = -9) porque los enlaces de hidrógeno al bromo son demasiado débiles para inhibir la disociación. El sistema HBr / H 2 O también involucra muchos hidratos HBr · nH 2 O para n= 1, 2, 3, 4 y 6, que son esencialmente sales de aniones bromo y cationes hidronio . El ácido bromhídrico forma un azeótropo con un punto de ebullición de 124.3 ° C a 47.63 g de HBr por 100 g de solución; por lo tanto, el ácido bromhídrico no se puede concentrar más allá de este punto por destilación. [25]
A diferencia de fluoruro de hidrógeno, bromuro de hidrógeno líquido anhidro es difícil trabajar con como disolvente, debido a que su punto de ebullición es bajo, tiene una pequeña gama líquido, su constante dieléctricaes baja y no se disocia apreciablemente en H 2 Br + y HBr -
2 iones: estos últimos, en cualquier caso, son mucho menos estables que los iones bifluoruro ( HF -
2 ) debido a la muy débil unión del hidrógeno entre el hidrógeno y el bromo, aunque sus sales tienen cationes muy grandes y débilmente polarizantes, como Cs + y NR +
4 (R = Me , Et, Bu n ) todavía puede estar aislado. El bromuro de hidrógeno anhidro es un disolvente pobre, que solo puede disolver pequeños compuestos moleculares como el cloruro de nitrosilo y el fenol , o sales con muy poca energía de la red , como los haluros de tetraalquilamonio. [25]
2 iones: estos últimos, en cualquier caso, son mucho menos estables que los iones bifluoruro ( HF -
2 ) debido a la muy débil unión del hidrógeno entre el hidrógeno y el bromo, aunque sus sales tienen cationes muy grandes y débilmente polarizantes, como Cs + y NR +
4 (R = Me , Et, Bu n ) todavía puede estar aislado. El bromuro de hidrógeno anhidro es un disolvente pobre, que solo puede disolver pequeños compuestos moleculares como el cloruro de nitrosilo y el fenol , o sales con muy poca energía de la red , como los haluros de tetraalquilamonio. [25]
Otros bromuros binarios [ editar ]
Casi todos los elementos en la tabla periódica forman bromuros binarios. Las excepciones están decididamente en la minoría y se derivan en cada caso de una de tres causas: inercia extrema y renuencia a participar en reacciones químicas (los gases nobles , con la excepción del xenón en el muy inestable XeBr 2 ); la extrema inestabilidad nuclear dificulta la investigación química antes de la descomposición y la transmutación (muchos de los elementos más pesados más allá del bismuto ); y que tiene una electronegatividad superior a la del bromo ( oxígeno , nitrógeno , flúor y cloro).), de modo que los compuestos binarios resultantes no son formalmente bromuros, sino más bien óxidos, nitruros, fluoruros o cloruros de bromo. (No obstante, el tribromuro de nitrógeno se denomina bromuro ya que es análogo a los otros trihaluros de nitrógeno). [26]
La bromación de metales con Br 2 tiende a producir estados de oxidación más bajos que la cloración con Cl 2cuando se dispone de una variedad de estados de oxidación. Los bromuros se pueden producir mediante la reacción de un elemento o su óxido, hidróxido o carbonato con ácido bromhídrico, y luego se deshidratan con temperaturas ligeramente altas combinadas con gas bromuro de hidrógeno anhidro o de baja presión. Estos métodos funcionan mejor cuando el producto de bromuro es estable a la hidrólisis; de lo contrario, las posibilidades incluyen la bromación oxidativa a alta temperatura del elemento con bromo o bromuro de hidrógeno, la bromación a alta temperatura de un óxido metálico u otro haluro por bromo, un bromuro metálico volátil, tetrabromuro de carbono o un bromuro orgánico. Por ejemplo, óxido de niobio (V)reacciona con tetrabromuro de carbono a 370 ° C para formar bromuro de niobio (V) . [26] Otro método es el intercambio de halógenos en presencia de exceso de "reactivo de halogenación", por ejemplo: [26]
- FeCl 3 + BBr 3 (exceso) → Febr 3 + Bcl 3
Cuando se desea un bromuro inferior, se puede reducir un haluro superior utilizando hidrógeno o un metal como agente reductor, o se puede usar la descomposición térmica o desproporción , como sigue: [26]
- 3 WBr 5 + gradiente térmico Al →475 ° C → 240 ° C 3 WBr 4 + AlBr 3
- EuBr 3 + 12 H 2 → EuBr 2 + HBr
- 2 TaBr 4 500 ° C→ TaBr 3 + TaBr 5
La mayoría de los bromuros de los metales de pre-transición (grupos 1, 2 y 3, junto con los lantánidos y actínidosen los estados de oxidación +2 y +3) son en su mayoría iónicos, mientras que los no metales tienden a formar bromuros moleculares covalentes, al igual que Metales en estados de alta oxidación desde +3 y superiores. El bromuro de plata es muy insoluble en agua y, por lo tanto, a menudo se utiliza como prueba cualitativa para el bromo. [26]
Haluros de bromo [ editar ]
Los halógenos forman muchos compuestos halogenados bivalentes , diamagnéticos con estequiometrías XY, XY 3 , XY 5 y XY 7 (donde X es más pesado que Y), y el bromo no es una excepción. El bromo forma un monofluoruro y monocloruro, así como un trifluoruro y pentafluoruro. También se caracterizan algunos derivados catiónicos y aniónicos, como BrF -2 , BrCl -2 , BrF +2 , BrF +4 y BrF +6 . Aparte de estos, también se conocenalgunos pseudohaluros , como
bromuro de cianógeno (BrCN), bromotiocianato (BrSCN), y bromo azida (BRN 3 ). [27]
bromuro de cianógeno (BrCN), bromotiocianato (BrSCN), y bromo azida (BRN 3 ). [27]
El monofluoruro de bromo de color marrón pálido (BrF) es inestable a temperatura ambiente, desproporcionándose rápida e irreversiblemente en bromo, trifluoruro de bromo y pentafluoruro de bromo. Por lo tanto, no se puede obtener puro. Puede sintetizarse mediante la reacción directa de los elementos o mediante la constitución de bromo y trifluoruro de bromo a altas temperaturas. [27] El monocloruro de bromo (BrCl), un gas de color marrón rojizo, se disocia fácilmente de manera reversible en bromo y cloro a temperatura ambiente y, por lo tanto, tampoco puede obtenerse puro, aunque puede producirse por la reacción directa reversible de sus elementos en el gas. Fase o en tetracloruro de carbono . [26] Monofluoruro de bromo en etanol.fácilmente conduce a la monobromación de los compuestos aromáticos PhX (la para -brominación se produce para X = Me, Bu t , OMe, Br; la meta- bromación se produce para la desactivación de X = –CO 2 Et, –CHO, –NO 2 ); esto se debe a la fisión heterolítica del enlace Br – F, que conduce a una rápida bromación electrofílica por Br + . [26]
A temperatura ambiente, el trifluoruro de bromo (BrF 3 ) es un líquido de color pajizo. Puede formarse fluorando directamente el bromo a temperatura ambiente y se purifica por destilación. Reacciona explosivamente con agua e hidrocarburos, pero es un reactivo fluorante menos violento que el trifluoruro de cloro . Reacciona vigorosamente con boro , carbono , silicio , arsénico , antimonio , yodo y azufre para producir fluoruros, y también reacciona con la mayoría de los metales y sus óxidos: como tal, se utiliza para oxidar uranio a hexafluoruro de uranioEn la industria nuclear. Óxidos refractarios tienden a estar fluorados sólo parcialmente, pero aquí los derivados KBrF 4 y BRF 2 SbF 6 permanecen reactiva. El trifluoruro de bromo es un disolvente ionizante no acuoso útil, ya que se disocia fácilmente para formar BrF +
2 y BrF -
4 y, por lo tanto, conduce la electricidad. [28]
2 y BrF -
4 y, por lo tanto, conduce la electricidad. [28]
El pentafluoruro de bromo (BrF 5 ) se sintetizó por primera vez en 1930. Se produce a gran escala por reacción directa de bromo con exceso de flúor a temperaturas superiores a 150 ° C, y en pequeña escala mediante fluoración de bromuro de potasio a 25 ° C . Es un agente fluorante muy vigoroso, aunque el trifluoruro de cloro es aún más violento. El pentafluoruro de bromo explota por reacción con agua y silicatos fluorados a 450 ° C. [29]
Compuestos Polybromine [ editar ]
Aunque la dibromina es un agente oxidante fuerte con una alta energía de primera ionización, los oxidantes muy fuertes como el fluoruro de peroxidisulfurilo (S 2 O 6 F 2 ) pueden oxidarla para formar el catión Br +
2 rojo cereza . Se conocen algunos otros cationes de bromo, a saber, el Br +
3 marrón y el Br +
5 marrón oscuro . [30] El anión tribromuro, Br -
3 , también se ha caracterizado; Es análogo al triyoduro . [27]
2 rojo cereza . Se conocen algunos otros cationes de bromo, a saber, el Br +
3 marrón y el Br +
5 marrón oscuro . [30] El anión tribromuro, Br -
3 , también se ha caracterizado; Es análogo al triyoduro . [27]
Oxidos y oxoácidos de bromo [ editar ]
| E ° (pareja) | a (H + ) = 1 (ácido) | E ° (pareja) | a (OH - ) = 1 (base) |
|---|---|---|---|
| Br 2 / Br - | +1.052 | Br 2 / Br - | +1.065 |
| HOBr / Br - | +1.341 | BrO - / Br - | +0.760 |
| BrO - 3 / Br - | +1.399 | BrO - 3 / Br - | +0.584 |
| HOBr / Br 2 | +1.604 | BrO - / Br 2 | +0.455 |
| BrO - 3 / Br 2 | +1.478 | BrO - 3 / Br 2 | +0.485 |
| BrO - 3 / HOBr | +1.447 | BrO - 3 / BrO- | +0.492 |
| BrO - 4 /BrO - 3 | +1.853 | BrO - 4 /BrO - 3 | +1.025 |
Los óxidos de bromo no están tan bien caracterizados como los óxidos de cloro u óxidos de yodo , ya que son bastante inestables: una vez se pensó que no podían existir en absoluto. El monóxido de dibromina es un sólido de color marrón oscuro que, aunque es razonablemente estable a -60 ° C, se descompone en su punto de fusión de -17.5 ° C; es útil en las reacciones de bromación [32] y se puede realizar a partir de la descomposición a baja temperatura del dióxido de bromo en el vacío. Oxida el yodo a pentóxido de yodo y el benceno a 1,4-benzoquinona ; En soluciones alcalinas, da el anión hipobromita . [33]
El llamado " dióxido de bromo ", un sólido cristalino amarillo pálido, puede ser mejor formulado como bromo perbromato , BrOBrO 3 . Es térmicamente inestable por encima de −40 ° C, descomponiéndose violentamente a sus elementos a 0 ° C. El trióxido de dibromina , syn -BrOBrO 2 , también se conoce; Es el anhídrido del ácido hipobromoso y del ácido bromico . Es un sólido cristalino de color naranja que se descompone por encima de -40 ° C; Si se calienta demasiado rápido, explota alrededor de 0 ° C. También se conocen algunos otros óxidos radicales inestables, como algunos óxidos mal caracterizados, como el pentóxido de dibromina, el octoóxido de tribromina y el trióxido de bromo. [33]
Los cuatro oxoácidos , el ácido hipobromoso (HOBr), el ácido bromoso (HOBrO), el ácido bromico (HOBrO 2 ) y el ácido perbromico (HOBrO 3 ), se estudian mejor debido a su mayor estabilidad, aunque solo lo están en solución acuosa. Cuando el bromo se disuelve en una solución acuosa, ocurren las siguientes reacciones: [31]
Br 2 + H 2 O ⇌ HOBr + H + + Br - K ac = 7.2 × 10 −9 mol 2 l −2 Br 2 + 2 OH - ⇌ OBr - + H 2 O + Br - K alk = 2 × 10 8 mol −1 l
El ácido hipobromoso es inestable a la desproporción. Los iones de hipobromito se formaron así desproporcionadamente fácilmente para dar bromuro y bromato: [31]
3 BrO - ⇌ 2 Br - + BrO -
3K = 10 15
Los ácidos bromos y los bromitos son muy inestables, aunque los bromitos de estroncio y bario son conocidos. [34] Más importantes son los bromatos , que se preparan a pequeña escala mediante la oxidación del bromuro con hipoclorito acuoso , y son agentes oxidantes fuertes. A diferencia de los cloratos, que son muy lentamente desproporcionados con el cloruro y el perclorato, el anión bromato es estable a la desproporción en soluciones tanto ácidas como acuosas. El ácido bromico es un ácido fuerte. Los bromuros y bromatos pueden comprender el bromo de la siguiente manera: [34]
- BrO -
3 + 5 Br - + 6 H + → 3 Br 2 + 3 H 2 O
Había muchos intentos fallidos para obtener perbromatos y ácido perbrómico, llevando a algunos racionalizaciones de por qué no deben existir, hasta 1968 cuando el anión se sintetizó primero desde el radiactivo desintegración beta de inestable 83
SeO 2−
4 . Hoy en día, los perbromatos se producen por la oxidación de soluciones de bromato alcalino por el gas de flúor. El exceso de bromato y fluoruro se precipita como bromato de plata y fluoruro de calcio , y la solución de ácido perbromico se puede purificar. El ión perbromato es bastante inerte a temperatura ambiente pero es extremadamente oxidante termodinámicamente, con agentes oxidantes extremadamente fuertes necesarios para producirlo, como flúor o difluoruro de xenón . El enlace Br – O en BrO -
4es bastante débil, lo que corresponde a la reticencia general de los elementos 4p (especialmente arsénico , selenio, y bromo) para alcanzar su máximo estado de oxidación posible, ya que se producen después de la contracción del escándalo caracterizada por el escaso blindaje provisto por los orbitales 3d sin nodos radiales. [35]
SeO 2−
4 . Hoy en día, los perbromatos se producen por la oxidación de soluciones de bromato alcalino por el gas de flúor. El exceso de bromato y fluoruro se precipita como bromato de plata y fluoruro de calcio , y la solución de ácido perbromico se puede purificar. El ión perbromato es bastante inerte a temperatura ambiente pero es extremadamente oxidante termodinámicamente, con agentes oxidantes extremadamente fuertes necesarios para producirlo, como flúor o difluoruro de xenón . El enlace Br – O en BrO -
4es bastante débil, lo que corresponde a la reticencia general de los elementos 4p (especialmente arsénico , selenio, y bromo) para alcanzar su máximo estado de oxidación posible, ya que se producen después de la contracción del escándalo caracterizada por el escaso blindaje provisto por los orbitales 3d sin nodos radiales. [35]
Compuestos orgánicos de bromo [ editar ]
Al igual que los otros enlaces carbono-halógeno, el enlace C-Br es un grupo funcional común que forma parte de la química orgánica del núcleo . Formalmente, los compuestos con este grupo funcional pueden considerarse derivados orgánicos del anión bromuro. Debido a la diferencia de electronegatividad entre el bromo (2.96) y el carbono (2.55), el carbono en un enlace C-Br es deficiente en electrones y, por lo tanto, electrofílico . La reactividad de los compuestos de organobromina se parece, pero es intermedia entre la reactividad de los compuestos de organocloro y organoiodo . Para muchas aplicaciones, los organobromuros representan un compromiso de reactividad y costo. [36]
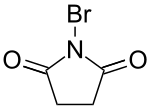
Los organobromuros se producen típicamente mediante bromación aditiva o sustitutiva de otros precursores orgánicos. Se puede usar el bromo en sí mismo, pero debido a su toxicidad y volatilidad, normalmente se usan reactivos de bromación más seguros, como la N-bromosuccinimida . Las principales reacciones para los organobromuros incluyen la deshidrobromación , las reacciones de Grignard , el acoplamiento reductivo y la sustitución nucleofílica . [36]
Los organobromuros son los organohaluros más comunes en la naturaleza, aunque la concentración de bromuro es solo 0.3% de la del cloruro en el agua de mar, debido a la fácil oxidación del bromuro al equivalente de Br + , un potente electrófilo. La enzima bromoperoxidasa cataliza esta reacción. [37] Se estima que los océanos liberan 1 a 2 millones de toneladas de bromoformo y 56,000 toneladas de bromometano al año. [38]
Una antigua prueba cualitativa de la presencia del grupo funcional alqueno es que los alquenos se vuelven incoloros en soluciones de bromo acuosas de color marrón, formando una bromohidrina con algo del dibromoalcano también producido. La reacción pasa a través de un intermedio de bromonio fuertemente electrófilo de corta duración . Este es un ejemplo de una reacción de adición de halógeno . [39]
Ocurrencia y la producción [ editar ]
El bromo es significativamente menos abundante en la corteza que el flúor o el cloro, y comprende solo 2,5 partes por millón de las rocas de la corteza terrestre, y solo como sales de bromuro. Es el cuadragésimo sexto elemento más abundante en la corteza terrestre. Es significativamente más abundante en los océanos, como resultado de la lixiviación a largo plazo . Allí, compone 65 partes por millón, lo que corresponde a una relación de aproximadamente un átomo de bromo por cada 660 átomos de cloro. Los lagos de sal y los pozos de salmuera pueden tener mayores concentraciones de bromo: por ejemplo, el Mar Muertocontiene un 0,4% de iones de bromuro. [40] Es de estas fuentes que la extracción de bromo es en su mayor parte económicamente viable. [41] [42] [43]
Las principales fuentes de bromo se encuentran en los Estados Unidos e Israel . El elemento se libera por intercambio de halógenos, utilizando gas de cloro para oxidar Br - a Br 2 . Luego se elimina con un chorro de vapor o aire, y luego se condensa y se purifica. Hoy en día, el bromo se transporta en tambores de metal de gran capacidad o tanques revestidos de plomo que pueden contener cientos de kilogramos o incluso toneladas de bromo. La industria del bromo es aproximadamente una centésima parte del tamaño de la industria del cloro. La producción de laboratorio es innecesaria porque el bromo está disponible comercialmente y tiene una larga vida útil. [44]
Aplicaciones [ editar ]
Una amplia variedad de compuestos de organobromina se utilizan en la industria . Algunos se preparan a partir de bromo y otros se preparan a partir de bromuro de hidrógeno , que se obtiene quemando hidrógeno en bromo. [45]
Retardantes de llama [ editar ]
Los retardantes de llama bromados representan un producto de creciente importancia y constituyen el mayor uso comercial de bromo. Cuando se quema el material bromado, el retardante de llama produce ácido bromhídrico que interfiere en la reacción en cadena radical de la reacción de oxidación del fuego. El mecanismo es que los radicales de hidrógeno altamente reactivos, los radicales de oxígeno y los radicales hidroxi reaccionan con el ácido bromhídrico para formar radicales de bromo menos reactivos (es decir, átomos de bromo libres). Los átomos de bromo también pueden reaccionar directamente con otros radicales para ayudar a terminar las reacciones en cadena de los radicales libres que caracterizan la combustión. [46] [47]
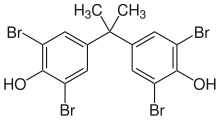
Para hacer polímeros y plásticos bromados, se pueden incorporar compuestos que contienen bromo en el polímero durante la polimerización . Un método es incluir una cantidad relativamente pequeña de monómero bromado durante el proceso de polimerización. Por ejemplo, el bromuro de vinilo se puede utilizar en la producción de polietileno , cloruro de polivinilo o polipropileno . También se pueden agregar moléculas específicas altamente bromadas que participan en el proceso de polimerización. Por ejemplo, el tetrabromobisfenol A se puede agregar a los poliésteres o resinas epoxi, donde se convierte en parte del polímero. Epóxicos utilizados en placas de circuito impreso.normalmente están hechas de tales resinasretardantes de llama, indicado por el FR en la abreviatura de los productos ( FR-4 y FR-2 ). En algunos casos, el compuesto que contiene bromo se puede añadir después de la polimerización. Por ejemplo, se puede agregar decabromodifenil éter a los polímeros finales. [48]
Un número de compuestos de halometano bromados gaseosos o altamente volátiles no son tóxicos y se convierten en agentes supresores de incendios superiores por este mismo mecanismo, y son particularmente efectivos en espacios cerrados como submarinos, aviones y naves espaciales. Sin embargo, son caros y su producción y uso se han reducido considerablemente debido a su efecto como agentes que agotan la capa de ozono. Ya no se utilizan en extintores de incendios de rutina, pero conservan usos específicos en aplicaciones aeroespaciales y militares de extinción de incendios automática. Incluyen bromoclorometano (Halon 1011, CH 2BrCl), bromoclorodifluorometano (Halon 1211, CBrClF 2 ) y bromotrifluorometano (Halon 1301, CBrF 3).).[49]
Otros usos [ editar ]
El bromuro de plata se usa solo o en combinación con cloruro de plata y yoduro de plata , como el componente sensible a la luz de las emulsiones fotográficas. [44]
Bromuro de etileno era un aditivo en las gasolinas que contienen anti-plomo detonación del motor agentes. Elimina el plomo formando bromuro de plomo volátil, que se agota del motor. Esta aplicación representó el 77% del uso de bromo en 1966 en los Estados Unidos. Esta aplicación ha disminuido desde la década de 1970 debido a las regulaciones ambientales (ver más abajo). [50]
El bromometano venenoso se usó ampliamente como pesticida para fumigar el suelo y para fumigar la vivienda, por el método de la carpa. El bromuro de etileno se usó de manera similar. [51] Estos compuestos volátiles de organobromina ahora están regulados comoagentes de agotamiento de ozono . El Protocolo de Montreal sobre sustancias que agotan la capa de ozono programó la eliminación de la sustancia química que agota la capa de ozono para 2005, y ya no se utilizan pesticidas organobromuro (en la fumigación de viviendas se han reemplazado por compuestos tales como el fluoruro de sulfurilo)., que no contienen ni el cloro ni el bromo que dañan el ozono). Antes del protocolo de Montreal en 1991 (por ejemplo), se utilizaron aproximadamente 35,000 toneladas de la sustancia química para controlar nematodos , hongos , malezas y otras enfermedades transmitidas por el suelo. [52] [53]
En farmacología , los compuestos de bromuro inorgánico , especialmente el bromuro de potasio , se utilizaron con frecuencia como sedantes generales en el siglo XIX y principios del XX. Los bromuros en forma de sales simples todavía se usan como anticonvulsivos en la medicina veterinaria y humana, aunque el último uso varía de un país a otro. Por ejemplo, la Administración de Drogas y Alimentos de los Estados Unidos (FDA, por sus siglas en inglés) no aprueba el bromuro para el tratamiento de ninguna enfermedad, y se eliminó de los productos sedantes de venta libre como Bromo-Seltzer , en 1975. [54] Productos farmacéuticos de organobromina disponibles comercialmente Incluye el vasodilatador nicergolina , el brotizolam sedante., el agente anticancerígeno pipobroman y el merbromin antiséptico . De lo contrario, los compuestos de organobromina rara vez son farmacéuticamente útiles, en contraste con la situación de los compuestos de organofluorina . Se producen varios fármacos como las sales de bromuro (o equivalentes, hidrobromuro), pero en tales casos el bromuro sirve como un contraión inocuo sin importancia biológica. [36]
Otros usos de los compuestos de organobromina incluyen los fluidos de perforación de alta densidad, los colorantes (como el púrpura de Tyrian y el indicador de azul de bromotimol ) y los productos farmacéuticos. El bromo en sí, al igual que algunos de sus compuestos, se utilizan en el tratamiento del agua y es el precursor de una variedad de compuestos inorgánicos con una enorme cantidad de aplicaciones (por ejemplo, bromuro de plata para fotografía). [44] Las baterías de zinc-bromo son baterías de flujo híbrido que se usan para almacenamiento y respaldo de energía eléctrica estacionaria; De la escala doméstica a la escala industrial.
Papel biológico y la toxicidad [ editar ]
| Peligros | |
|---|---|
| Pictogramas GHS |    |
| Palabra de señal GHS | Peligro |
| H314 , H330 , H400 | |
| P260 , P273 , P280 , P284 ,P305 + 351 + 338 , P310 [55] | |
| NFPA 704 | |
Un estudio de 2014 sugiere que el bromo (en forma de ion bromuro) es un cofactor necesario en la biosíntesis del colágeno IV , lo que hace que el elemento sea esencial para la arquitectura de la membrana basal y el desarrollo de tejidos en los animales. [57] Sin embargo, no se han documentado síntomas claros de privación o síndromes. [58] En otras funciones biológicas, el bromo puede ser no esencial pero aún así ser beneficioso cuando ocupa el lugar del cloro. Por ejemplo, en presencia de peróxido de hidrógeno, H 2 O 2, formado por el eosinófilo., y ya sea iones cloruro o bromuro, la peroxidasa eosinófila proporciona un potente mecanismo por el cual los eosinófilos matan a los parásitos multicelulares (como, por ejemplo, los gusanos nematodos involucrados en la filariasis ) y algunas bacterias (como las bacterias de la tuberculosis ). La peroxidasa de eosinófilos es una haloperoxidasa que utiliza preferentemente bromuro sobre cloruro para este propósito, generando hipobromito ( ácido hipobromoso ), aunque es posible el uso de cloruro. [59]
Aunque generalmente se piensa que los α-haloésteres son altamente reactivos y, por lo tanto, los intermedios tóxicos en la síntesis orgánica, los mamíferos, incluidos los humanos, los gatos y las ratas, parecen biosintetizar trazas de un α-bromoéster, 2-octilo 4-bromo-3- El oxobutanoato, que se encuentra en su líquido cefalorraquídeo y parece desempeñar un papel aún no aclarado en la inducción del sueño REM. [60] Los neutrófilos humanos usan mieloperoxidasa, H2O2 y Br (-) para brominizar la desoxicitidina, que es un mutágeno, por lo que las reacciones de deshalogenación con bromo pueden ser responsables de algunos cánceres humanos.[61]Los organismos marinos son la principal fuente de compuestos de organobromina, y es en estos organismos que la esencialidad del bromo se encuentra en un terreno mucho más firme. Más de 1600 tales compuestos orgánicos de bromo se identificaron por 1999. El más abundante es el bromuro de metilo (CH 3 Br), de los cuales un estimado de 56.000 toneladas es producido por algas marinas cada año. [62] El aceite esencial del alga hawaiana Asparagopsis taxiformis consiste en 80% de bromoformo . [63]La mayoría de estos compuestos de organobromina en el mar están hechos por la acción de una enzima algal única, la bromoperoxidasa de vanadio . [64]
El anión bromuro no es muy tóxico: una ingesta diaria normal es de 2 a 8 miligramos. [58] Sin embargo, los niveles altos de bromuro dañan crónicamente la membrana de las neuronas, lo que deteriora progresivamente la transmisión neuronal, lo que lleva a una toxicidad, conocida como bromismo . El bromuro tiene una vida media de eliminación de 9 a 12 días, lo que puede llevar a una acumulación excesiva. Las dosis de 0.5 a 1 gramo por día de bromuro pueden llevar a bromismo. Históricamente, la dosis terapéutica de bromuro es de aproximadamente 3 a 5 gramos de bromuro, lo que explica por qué una vez fue tan común la toxicidad crónica (bromismo). Si bien se producen alteraciones significativas y, a veces, graves, en las funciones neurológicas, psiquiátricas, dermatológicas y gastrointestinales, la muerte por bromismo es rara. [sesenta y cinco]El bromismo es causado por un efecto neurotóxico en el cerebro que produce somnolencia , psicosis , convulsiones y delirio . [66]
El bromo elemental es tóxico y causa quemaduras químicas en la carne humana. La inhalación de gas bromo produce una irritación similar del tracto respiratorio, causando tos, ahogo y falta de aire, y la muerte si se inhala en cantidades suficientemente grandes. La exposición crónica puede conducir a infecciones bronquiales frecuentes y un deterioro general de la salud. Como un agente oxidante fuerte, el bromo es incompatible con la mayoría de los compuestos orgánicos e inorgánicos. [67] Se requiere precaución al transportar bromo; Es comúnmente transportado en tanques de acero revestidos con plomo, soportados por fuertes marcos de metal. [44] La Administración de Seguridad y Salud Ocupacional (OSHA) de los Estados Unidos ha establecido un límite de exposición permisible.(PEL) para bromo en un promedio ponderado en el tiempo (TWA) de 0.1 ppm. El Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH) ha establecido un límite de exposición recomendado (REL) de TWA 0.1 ppm y un límite a corto plazo de 0.3 ppm. La exposición al bromo inmediatamente peligrosa para la vida y la salud (IDLH) es de 3 ppm. [68] El bromo está clasificado como una sustancia extremadamente peligrosa en los Estados Unidos según lo definido en la Sección 302 de la Ley de Planificación de Emergencias y Derecho a la Información de la Comunidad de los Estados Unidos (42 USC 11002), y está sujeto a estrictos requisitos de notificación por parte de las instalaciones que producen , almacénelo, o utilícelo en cantidades significativas.




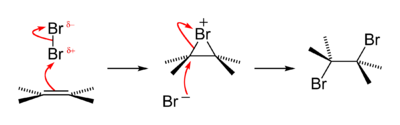


No hay comentarios:
Publicar un comentario