El alocortex (también conocido como corteza heterogenética ) es uno de los dos tipos de corteza cerebral , el otro es la neocorteza . Se caracteriza por tener solo tres o cuatro capas celulares , en contraste con las seis capas de la neocorteza, y ocupa un área mucho más pequeña que la neocorteza. Hay tres subtipos de alocortex: el paleocortex , el archicortex y el periallocortex , una zona de transición entre el neocortex y el alocortex. [1]
Las regiones específicas del cerebro que generalmente se describen como pertenecientes al alocortex son el sistema olfativo y el hipocampo .
La alocorteza se denomina corteza heterogenética, porque durante el desarrollo nunca tiene la arquitectura de seis capas de la neocorteza homogenética. Se diferencia de la corteza heterotípica, un tipo de corteza cerebral, que durante el desarrollo prenatal, pasa por una etapa de seis capas para tener menos capas, como en el área 4 de Brodmann que carece de células granulares . [2]
Estructura [ editar ]
El alocortex tiene tres o cuatro capas de cuerpos celulares neuronales , en contraste con las seis capas de la neocorteza. Hay tres subtipos de alocorteza, la paleocorteza, la arquicorteza y la periallocorteza. [3]
Paleocortex es un tipo de tejido cortical delgado y primitivo que consta de tres láminas corticales (capas de cuerpos celulares neuronales ). [4] [5] Las dos capas granulares II y IV de la neocorteza están ausentes en la paleocorteza. Las principales áreas de paleocorteza son el bulbo olfatorio , el tubérculo olfatorio y la corteza piriforme .
Archicortex es un tipo de tejido cortical que consta de cuatro láminas (capas de cuerpos celulares neuronales ). [6] Las áreas principales de archicortex son el hipocampo y la circunvolución dentada .
Periallocortex es una forma de transición entre neocortex y paleo o archi-corteza. Por lo tanto, puede ser peripaleocortex (corteza insular anterior) o periarchicortex ( corteza entorrinal , corteza presubicular, áreas retrosplenial, supracallosal y subgenual).
Debido a que la cantidad de láminas que componen un tipo de tejido cortical parece ser directamente proporcional tanto a las capacidades de procesamiento de información de ese tejido como a su edad filogenética, y también porque la olfato es una modalidad sensorial importante en animales filogenéticamente tempranos, se cree que la paleocorteza Ser la forma más primitiva de corteza.
Las neuronas motoras alfa ( α ) (también llamadas motoneuronas alfa ) son neuronas motoras inferiores multipolaresgrandes del tronco encefálico y la médula espinal . Inervan las fibras musculares extrafusal de músculo esquelético y son directamente responsables de iniciar su contracción . Las neuronas motoras alfa son distintas de las neuronas motoras gamma , que inervan las fibras musculares intrafusales de los husos musculares .
Si bien sus cuerpos celulares se encuentran en el sistema nervioso central (SNC), las neuronas motoras α también se consideran parte del sistema nervioso somático, una rama del sistema nervioso periférico (SNP), porque sus axones se extienden hacia la periferia para inervar los músculos esqueléticos. .
Una neurona motora alfa y las fibras musculares que inerva es una unidad motora . Un grupo de neuronas motoras contiene los cuerpos celulares de todas las neuronas motoras alfa involucradas en la contracción de un solo músculo.
Ubicación [ editar ]
Las neuronas motoras alfa (α-MN) que inervan la cabeza y el cuello se encuentran en el tronco encefálico ; los α-MN restantes inervan el resto del cuerpo y se encuentran en la médula espinal . Hay más α-MN en la médula espinal que en el tronco encefálico, ya que la cantidad de α-MN es directamente proporcional a la cantidad de control motor fino en ese músculo. Por ejemplo, los músculos de un solo dedo tienen más α-MN por fibra, y más α-MN en total, que los músculos del cuádriceps , lo que permite un control más preciso de la fuerza que aplica un dedo.
En general, los α-MN en un lado del tronco encefálico o la médula espinal inervan los músculos en el mismo lado del cuerpo. Una excepción es el núcleo troclear en el tronco encefálico, que inerva el músculo oblicuo superiordel ojo en el lado opuesto de la cara.
Tronco encefálico [ editar ]
En el tronco encefálico, los α-MN y otras neuronas residen dentro de grupos de células llamadas núcleos , algunos de los cuales contienen los cuerpos celulares de las neuronas que pertenecen a los nervios craneales . No todos los núcleos del nervio craneal contienen α-MN; los que lo hacen son núcleos motores , mientras que otros son núcleos sensoriales . Los núcleos motores se encuentran en todo el tronco encefálico ( médula , protuberancia y mesencéfalo) y por razones de desarrollo se encuentran cerca de la línea media del tronco encefálico.
En general, los núcleos motores que se encuentran más arriba en el tronco encefálico (es decir, más rostral) inervan los músculos que están más arriba en la cara. Por ejemplo, el núcleo oculomotor contiene α-MN que inervan los músculos del ojo y se encuentra en el mesencéfalo, el componente del tronco encefálico más rostral. Por el contrario, el núcleo hipogloso , que contiene α-MN que inervan la lengua, se encuentra en la médula, la más caudal (es decir, hacia el fondo) de las estructuras del tronco encefálico.
Médula espinal [ editar ]
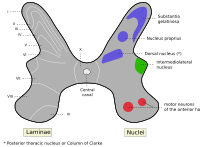
En la médula espinal, los α-MN se encuentran dentro de la materia gris que forma el asta ventral . Estos α-MN proporcionan el componente motor de los nervios espinales que inervan los músculos del cuerpo.
Al igual que en el tronco encefálico, los segmentos superiores de la médula espinal contienen α-MN que inervan los músculos más altos del cuerpo. Por ejemplo, el músculo bíceps braquial , un músculo del brazo, está inervado por α-MN en los segmentos de la médula espinal C5, C6 y C7, que se encuentran rostralmente en la médula espinal. Por otro lado, el músculo gastrocnemio , uno de los músculos de la pierna, está inervado por α-MN dentro de los segmentos S1 y S2, que se encuentran caudalmente en la médula espinal.
Las neuronas motoras alfa se encuentran en una región específica de la materia gris de la médula espinal. Esta región se denomina lámina IX en el sistema de láminas Rexed , que clasifica las regiones de materia gris en función de su citoarquitectura . La lámina IX se encuentra predominantemente en el aspecto medial del asta ventral, aunque hay alguna contribución a la lámina IX de una colección de neuronas motoras ubicadas más lateralmente. Al igual que otras regiones de la médula espinal, las células de esta lámina son somatotópicamente.organizado, lo que significa que la posición de las neuronas dentro de la médula espinal está asociada con qué músculos inervan. En particular, los α-MN en la zona medial de la lámina IX tienden a inervar los músculos proximales del cuerpo, mientras que los de la zona lateral tienden a inervar más músculos distales. Hay una somatotopía similar asociada con los α-MN que inervan los músculos flexores y extensores: los α-MN que inervan los flexorestienden a ubicarse en la porción dorsal de la lámina IX; los que inervan los extensores tienden a ubicarse más ventralmente.
Desarrollo [ editar ]
Las neuronas motoras alfa se originan en la placa basal , la porción ventral del tubo neural en el embrión en desarrollo . Sonic hedgehog(Shh) es secretado por el notocordio cercano y otras estructuras ventrales (por ejemplo, la placa del piso ), estableciendo un gradiente de Shh altamente concentrado en la placa basal y Shh menos concentrado en la placa alar . Bajo la influencia de Shh y otros factores, algunas neuronas de la placa basal se diferencian en α-MN.
Al igual que otras neuronas, los α-MN envían proyecciones axonales para alcanzar sus fibras musculares extrafusales objetivo a través de la guía del axón , un proceso regulado en parte por factores neurotróficos liberados por las fibras musculares objetivo. Los factores neurotróficos también aseguran que cada fibra muscular esté inervada por el número apropiado de α-MN. Como con la mayoría de los tipos de neuronas en el sistema nervioso , los α-MN son más numerosos en el desarrollo temprano que en la edad adulta. Las fibras musculares secretan una cantidad limitada de factores neurotróficos capaces de sostener solo una fracción de los α-MN que inicialmente se proyectan a la fibra muscular. Aquellos α-MN que no reciben suficientes factores neurotróficos sufrirán apoptosis , una forma demuerte celular programada .
Debido a que inervan muchos músculos, algunos grupos de α-MN reciben altas concentraciones de factores neurotróficos y sobreviven a esta etapa de poda neuronal. Esto es cierto para los α-MN que inervan las extremidades superiores e inferiores: estos α-MN forman grandes columnas celulares que contribuyen al agrandamiento cervical y lumbar de la médula espinal. Además de recibir factores neurotróficos de los músculos, los α-MN también secretan una serie de factores tróficos para soportar las fibras musculares que inervan. Los niveles reducidos de factores tróficos contribuyen a la atrofia muscular que sigue a una lesión de α-MN.
Conectividad [ editar ]
Al igual que otras neuronas, las neuronas motoras inferiores tienen conexiones aferentes (entrantes) y eferentes (salientes). Las neuronas motoras alfa reciben información de varias fuentes, incluidas las neuronas motoras superiores , las neuronas sensoriales y las interneuronas . La salida primaria de los α-MN es a las fibras musculares extrafusales . Esta conectividad aferente y eferente es necesaria para lograr una actividad muscular coordinada.
Entrada aferente [ editar ]
| Origen UMN | objetivo α-MN | Nombre del tracto |
|---|---|---|
| Corteza cerebral | Tronco encefálico | Tracto corticonuclear |
| Corteza cerebral | Médula espinal | Tracto corticoespinal |
| Núcleo rojo | Médula espinal | Tracto rubrospinal |
| Núcleos vestibulares | Médula espinal | Tracto vestibuloespinal |
| Tectum del mesencéfalo | Médula espinal | Tracto tectospinal |
| Formación reticular | Médula espinal | Tracto retículoespinal |
Las neuronas motoras superiores (UMN) envían información a los α-MN a través de varias vías, que incluyen (entre otras) las vías corticonucleares , corticoespinales y rubrospinales . Los tractos corticonucleares y corticoespinales se encuentran comúnmente en estudios de conectividad de neuronas motoras superiores e inferiores en el control de movimientos voluntarios.
El tracto corticonuclear se llama así porque conecta la corteza cerebral con los núcleos de los nervios craneales . (El tracto corticonuclear también se llama tracto corticobulbar , ya que el tronco encefálico a veces se llama el "bulbo" del cerebro). Es a través de esta vía que las neuronas motoras superiores de la corteza descienden de la corteza y sinapsis en los α-MN del tronco encefálico De manera similar, los UMN de la corteza cerebral controlan directamente los α-MN de la médula espinal a través de los tractos corticoespinales lateral y ventral .
El aporte sensorial a los α-MN es extenso y tiene su origen en los órganos del tendón de Golgi , los husos musculares , los mecanorreceptores , los termorreceptores y otras neuronas sensoriales en la periferia. Estas conexiones proporcionan la estructura para los circuitos neuronales que subyacen a los reflejos . Existen varios tipos de circuitos reflejos, el más simple consiste en una sinapsis única entre una neurona sensorial y un α-MN. El reflejo instintivo es un ejemplo de tal reflejo monosináptico.
El aporte más extenso a los α-MN proviene de las interneuronas locales , que son el tipo de neurona más numeroso en la médula espinal . Entre sus muchos roles, las interneuronas hacen sinapsis en α-MN para crear circuitos reflejos más complejos. Un tipo de interneurona es la célula Renshaw , que se analiza más adelante.
Salida diferente [ editar ]
Las neuronas motoras alfa envían fibras que principalmente hacen sinapsis en fibras musculares extrafusales . Otras fibras de α-MN sinapsis en células Renshaw , es decir, interneuronas inhibidoras que sinapsis en el α-MN y limitan su actividad para prevenir el daño muscular.
Señalización [ editar ]
Al igual que otras neuronas, los α-MN transmiten señales como potenciales de acción , cambios rápidos en la actividad eléctrica que se propagan desde el cuerpo celular hasta el extremo del axón . Para aumentar la velocidad a la que viajan los potenciales de acción, los axones α-MN tienen diámetros grandes y están fuertemente mielinizados por los oligodendrocitos y las células de Schwann . Los oligodendrocitos mielinizan la parte del axón α-MN que se encuentra en el sistema nervioso central (SNC), mientras que las células de Schwann mielinizan la parte que se encuentra en el sistema nervioso periférico (SNP). La transición entre el SNC y el SNP se produce a nivel de la piamadre., la capa más interna y delicada de tejido meníngeo que rodea los componentes del SNC.
El axón de un α-MN se conecta con su fibra muscular extrafusal a través de una unión neuromuscular , un tipo especializado de sinapsis química que difiere tanto en estructura como en función de las sinapsis químicas que conectan las neuronas entre sí. Ambos tipos de sinapsis dependen de neurotransmisores para transducir la señal eléctrica en una señal química y viceversa. Una forma en que difieren es que las sinapsis entre las neuronas generalmente usan glutamato o GABA como sus neurotransmisores, mientras que la unión neuromuscular usa exclusivamente acetilcolina . La acetilcolina es detectada por los receptores nicotínicos de acetilcolina. en fibras musculares extrafusales, causando su contracción.
Al igual que otras neuronas motoras, los α-MN reciben su nombre de las propiedades de sus axones . Las neuronas motoras alfa tienen axones Aα , que son fibras muy mielinizadas de gran calibre que conducen potenciales de acción rápidamente. Por el contrario, las neuronas motoras gamma tienen axones Aγ , que son fibras delgadas y ligeramente mielinizadas que se conducen con menos rapidez.
Importancia clínica [ editar ]
La lesión de los α-MN es el tipo más común de lesión de la neurona motora inferior . El daño puede ser causado por trauma , isquemia e infección , entre otros. Además, ciertas enfermedades están asociadas con la pérdida selectiva de α-MN. Por ejemplo, la poliomielitis es causada por un virus que ataca específicamente y mata las neuronas motoras en el asta ventral de la médula espinal. La esclerosis lateral amiotrópica también se asocia con la pérdida selectiva de neuronas motoras.
La parálisis es uno de los efectos más pronunciados del daño a los α-MN. Debido a que los α-MN proporcionan la única inervación voluntaria a las fibras musculares extrafusales , la pérdida de α-MN efectivamente corta la conexión entre el tronco encefálico y la médula espinal y los músculos que inervan. Sin esta conexión, el control muscular voluntario e involuntario (reflejo) es imposible. El control muscular voluntario se pierde porque los α-MN transmiten señales voluntarias desde las neuronas motoras superiores a las fibras musculares. La pérdida del control involuntario resulta de la interrupción de los circuitos reflejos , como el reflejo de estiramiento tónico . Una consecuencia de la interrupción refleja es que el tono muscular se reduce, lo que resulta en paresia flácida. Otra consecuencia es la depresión de los reflejos tendinosos profundos, causando hiporreflexia .
La debilidad muscular y la atrofia también son consecuencias inevitables de las lesiones α-MN. Debido a que el tamaño y la fuerza muscular están relacionados con el alcance de su uso, los músculos desnervados son propensos a atrofiarse. Una causa secundaria de atrofia muscular es que los músculos desnervados ya no reciben factores tróficos de los α-MN que los inervan. Las lesiones de la neurona motora alfa también producen potenciales EMG anormales (p. Ej., Potenciales de fibrilación ) y fasciculaciones , siendo estas últimas contracciones musculares espontáneas e involuntarias.
Las enfermedades que deterioran la señalización entre los α-MN y las fibras musculares extrafusales, es decir, las enfermedades de la unión neuromuscular tienen signos similares a los que ocurren con la enfermedad de α-MN. Por ejemplo, la miastenia gravis es una enfermedad autoinmune que evita la señalización a través de la unión neuromuscular , lo que resulta en la denervación funcional del músculo.


No hay comentarios:
Publicar un comentario